首都医科大学附属北京友谊医院柳柯教授、清华大学尹斓教授 ACS Nano:中耳递送载药水凝胶 - 一针治愈噪声性聋
2024-02-14 来源:高分子科技
噪声性听力损失是感音神经性聋的主要形式之一,世界卫生组织估计全球有数亿人口正在遭受噪声性聋的困扰。未来十年,噪声暴露所导致的听力损害人群数量将会大幅上升。长期以来,噪声性听力损失的治疗始终是临床上难以解决的棘手问题,其中最重要的痛点是药物无法通过常规给药方式穿越血迷路屏障进入内耳发挥治疗作用。而通过中耳递送的局部给药方式可能为感音神经性聋的治疗带来新的希望。

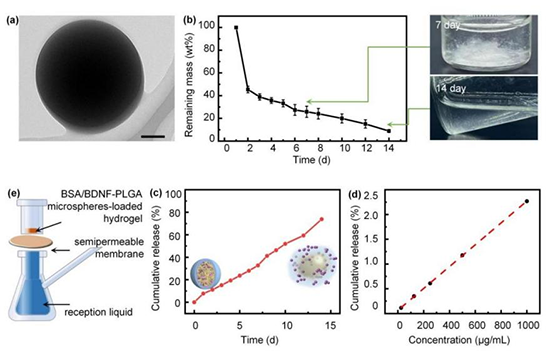
接下来,研究人员观察了注射进入中耳的药载水凝胶在2周时间内向内耳释放BDNF的效果。本研究中,科研人员利用带有绿色荧光的C6染料来评估凝胶缓释药物进入内耳的情况。他们发现,经过凝胶缓释进入内耳的药物浓度和剂量均显著高于单纯药物中耳注射组,仅稍低于经半规管手术直接导入药物的观察组。该研究结果显示了这种专门设计的温敏药载水凝胶进入中耳后具有十分优异的内耳缓释效果。进一步,研究发现经过中耳递送进入内耳的BDNF有效地激活了TRKB信号通路(图2),从而发挥了对耳蜗带状突触损害的修复作用。
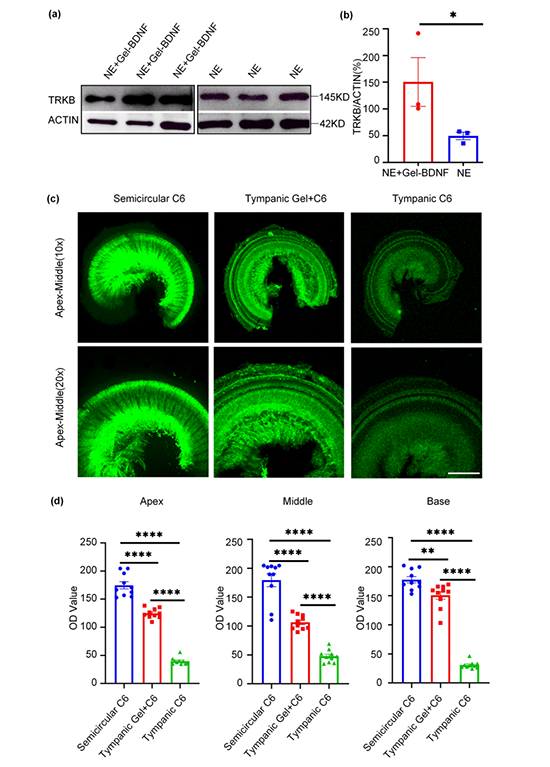
在此之后,研究人员对噪声诱导听力损失和带状突触损害的小鼠进行药载温敏水凝胶鼓室注射,并在注射后第2天、第7天和第14天分别检测小鼠听力的变化情况。研究结果表明,负载BDNF的水凝胶注射后第7天即可在小鼠中观察到听力恢复现象,至注射后第14天,小鼠听力得到了完全的恢复:即与未经过噪声暴露的正常对照组小鼠相比,两组小鼠的听力阈值已无显著差别(图3)。

此外,这项研究还展示了药载温敏水凝胶在‘鼓室注射-中耳驻留-排出体外’这个过程中的动态变化情况。为了便于观察,研究人员利用食品添加剂(SUGARMAN)将注射水凝胶调成墨绿色,利用高分辨内窥镜系统对整个操作及变化过程采集图像。实验结果表明,在鼓室注射后水凝胶即充满中耳腔,至注射后第14天,通过8-12小时的变温调节作用,中耳内驻留水凝胶再次变为液态并经咽鼓管全部排出体外(图4)。这个实验显示,这种中耳载药温敏水凝胶的递送系统具有微创、可控、可排出及无残留等特点。
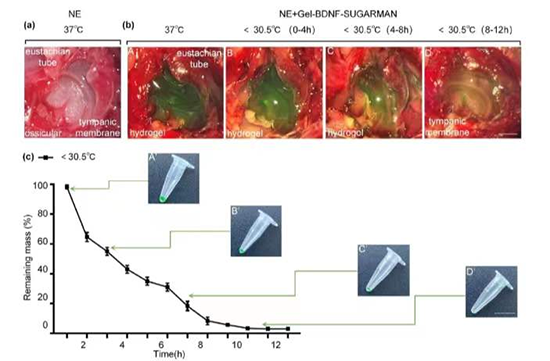
总体说来,该研究发现了温敏水凝胶注射进入中耳的最适指标,使其可在‘液态-半固态’之间进行可控切换,并可与内耳圆窗膜牢固贴附,从而实现药物向内耳持续高浓度缓释的目标。该研究设计的中耳递送给药体系包括温敏水凝胶、纳米缓释微球和药物(BDNF)三个部分,这些要素与鼓室注射操作相结合,共同组成了一种理想的中耳局部给药系统,该系统在本研究中展现了高效、可控、微创、无残留以及单次操作等诸多优良特性(图5)。该研究在动物实验水平上证明了‘一针治愈耳聋’是可以实现的干预目标,因此有望引领未来感音神经性聋治疗方式的新变革,并可能具有重要的临床转化前景。
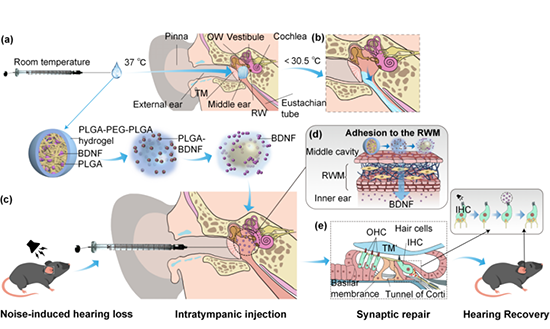
图5.研究总体策略、机制及流程示意图
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.3c11049
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 华科大罗志强教授团队《Nat. Commun.》:可注射导电水凝胶实现无线、微创深部脑神经调控 2026-02-10
- 长春应化所陈学思院士/宋万通研究员团队《Adv. Sci.》:免疫微创凝胶用于肝癌和胃癌的局部免疫治疗 2024-08-17
- 深圳先进院赵晓丽、潘浩波/天大刘文广等《Nat. Commun.》:适用于微创植入的4D打印水凝胶支架 2024-02-24
- 天津大学王彬教授 Angew:温度梯度辅助解聚实现 7/14 元环碳酸酯选择性合成及高性能脂肪族聚碳酸酯可控制备 2026-05-22
- 哈工程刘天亿、复旦大学孔彪 ACS Nano:非对称聚合物半导体纳米机器人的可控合成与感染皮肤创面治疗 2026-04-16
- 长春应化所陶友华研究员团队 JACS:阴离子结合催化实现聚(1,3-二氧戊环)的可控合成 2026-03-27
- 苏州大学冯良珠教授、刘庄教授团队 AFM:温敏催化水凝胶助力酶触“破膜+氧化应激”级联肿瘤消融新策略 2025-12-04
