放射性皮炎作为癌症放疗最常见的并发症之一,困扰着约95%的放疗患者。这种损伤往往始于轻微红斑和干性脱屑,伴随着难以忍受的瘙痒;随着辐射剂量累积,病情可能急转直下,发展为湿性脱屑、渗出甚至出血结痂,最严重者可出现难以愈合的溃疡与坏死。在这一病理过程中,线粒体因其特殊的生物学特性,缺乏组蛋白保护且DNA修复能力有限,成为了辐射损伤的首要靶点。电离辐射不仅直接导致线粒体DNA双链及单链断裂,更会引发活性氧(ROS)爆发性生成,这种氧化应激的恶性循环会进一步破坏线粒体功能、扰乱能量代谢、打破细胞稳态,最终诱发剧烈的炎症反应和细胞凋亡,推动放射性皮炎不断恶化。面对这一临床难题,开发能够精准调控氧化应激、维护线粒体稳态的新型放射防护策略显得尤为迫切。
针对这一重大临床需求,浙江大学周民教授团队独辟蹊径,从天然螺旋藻(Spirulina platensis, SP)中分离出具有天然生物相容性的细胞外囊泡(EVs),并创新性地将强效抗氧化剂虾青素(astaxanthin, AST)负载其中,成功构建了工程化微藻细胞外囊泡递送系统(SP-EVs@AST)。这一精巧的设计不仅完整保留了EVs的结构与生物活性,更巧妙地解决了AST水溶性差、稳定性不佳的瓶颈问题,实现了载体与药物的完美协同。研究结果表明,SP-EVs@AST能够高效清除辐射诱导的过量ROS,修复受损的线粒体功能,显著抑制炎症因子的释放,从而为细胞构筑起一道抵御放射损伤的坚固防线。为了进一步提升治疗效果,研究团队还将这一递送系统封装于由醛基化透明质酸(HA-CHO)与羧甲基壳聚糖(CMCS)通过动态共价交联形成的水凝胶网络中,开发出具有智能缓释特性的皮肤防护敷料。这种敷料不仅能长期维持囊泡活性,实现药物的可控释放,还在动物模型中展现出卓越的放射防护效果和长期的生物安全性。
这项研究不仅证实了工程化微藻细胞外囊泡作为难溶性药物载体的巨大潜力,更开拓了其在精准医学领域应用的新视野。相关成果以《Engineered Microalgal Extracellular Vesicles for Enhancing Mitochondrial Homeostasis in Radiodermatitis Prevention》为题,近期发表在材料科学领域的顶级期刊《ACS Nano》上(https://doi.org/10.1021/acsnano.5c07135),为放射性皮炎的临床防治提供了创新性的解决方案。
1.SP-EVs@AST的制备与表征
该研究采用差速离心结合超速离心的分离纯化方法,成功从螺旋藻(SP)培养上清液中提取出微藻源细胞外囊泡(SP-EVs)。随后,通过优化超声共孵育工艺,将具有强效抗氧化活性的虾青素(AST)高效装载入囊泡内部,成功构建了工程化递送系统SP-EVs@AST。该制备工艺在确保囊泡膜结构完整性的同时,显著改善了AST的水溶性和制剂稳定性。透射电镜(TEM)和动态光散射(DLS)表征结果显示,SP-EVs@AST呈现典型的球状囊泡形态,粒径分布在200-300 nm范围内,这一尺寸特性有利于其经皮渗透和递送。该递送系统的成功构建,不仅为亲脂性药物提供了高效的递送解决方案,显著提高了药物的生物利用度和治疗效果,同时也为微藻源细胞外囊泡在生物医学领域的创新应用开辟了新途径。
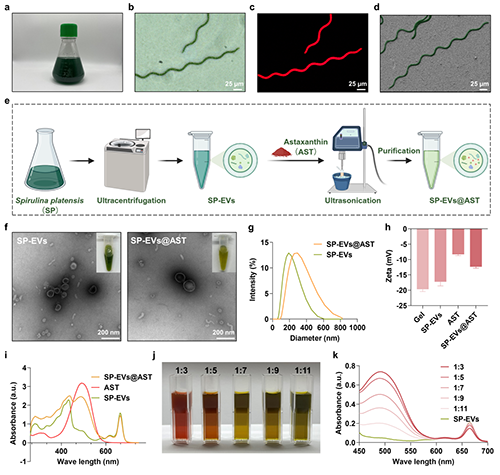
图1 SP-EVs@AST的制备与表征
2.SP-EVs@AST水凝胶的制备与表征
为实现高效的经皮药物递送,该研究将SP-EVs@AST封装于醛基化透明质酸(HA-CHO)/羧甲基壳聚糖(CMCS)自组装水凝胶中,二者通过席夫碱反应交联形成水凝胶,SP-EVs@AST均匀分布其中。设置不同浓度HA-CHO/CMCS来筛选最佳性能的水凝胶。结果显示,5%(HA-CHO/CMCS 1:1)为最佳浓度,黏附性突出,可在成胶过程中实现瞬时附着并承重500?g。该凝胶适配0°–90°弯曲关节及不规则表面,并可塑形成多种形态,原位成胶于小鼠皮肤后,能在小鼠活动过程中稳定附着。储能模量与损耗模量测试结果表明,该水凝胶在55?s内完成快速成胶,适于创面即时固定。溶胀实验显示,水凝胶在8?h内达到平衡并保持稳定结构。模拟皮肤创面微环境的药物释放实验表明,在酸性条件下,水凝胶中的席夫碱键易断裂,加速降解与药物释放;在中性至微碱性环境中,药物释放平稳,24?h基本达到最大释放量。综上,该研究构建的SP-EVs@AST水凝胶兼具高效药物负载、稳定递送及优异的皮肤适应性,展现出工程化微藻细胞外囊泡水凝胶在局部治疗及精准药物递送中的应用潜力。

图2 SP-EVs@AST水凝胶的制备与表征
3.SP-EVs@AST水凝胶恢复细胞增殖与迁移
共聚焦显微镜观察显示,SP-EVs@AST的细胞摄取呈现时间依赖性,4?h出现明显内化,8?h以上可确保充分摄取。CCK-8检测结果表明,SP-EVs、水凝胶及AST(≤25?μg/mL)对细胞无明显毒性,SP-EVs@AST在不同浓度梯度下也表现出良好的安全性。进一步实验发现,SP-EVs@AST水凝胶可显著促进受辐照HaCaT细胞的增殖,恢复其克隆形成能力,提升细胞存活率并减少辐射诱导的凋亡。划痕愈合实验与Transwell实验结果表明,该水凝胶有效恢复受辐照细胞的迁移能力。研究结果提示,SP-EVs@AST水凝胶具有良好的体外生物相容性及促进辐照皮肤创面修复的潜力。

图3 SP-EVs@AST水凝胶恢复细胞增殖与迁移
4.SP-EVs@AST水凝胶调节线粒体稳态
线粒体作为细胞的主要能量工厂,极易受到辐射损伤。过量ROS的生成会进一步加剧线粒体功能障碍。DCFH-DA荧光探针检测结果表明,SP-EVs@AST水凝胶显著抑制了辐射诱导的ROS生成,这一结果与流式分析结果一致。JC-1染色实验表明,该水凝胶能有效防止辐射导致的线粒体膜电位下降,并减少细胞色素C(Cyt-C)的外泄。TEM结果进一步证实,SP-EVs@AST水凝胶能够维持线粒体嵴及结构的完整性。除了直接DNA损伤外,氧化应激也是辐射引起DNA双链断裂的重要因素。γ-H2AX免疫荧光检测结果表明,SP-EVs@AST水凝胶显著抑制了辐射引起的DNA损伤。综上所述,这些发现证实了SP-EVs@AST水凝胶在维持线粒体稳态中的作用。

图4 SP-EVs@AST水凝胶调节线粒体稳态
5.SP-EVs@AST水凝胶保护小鼠免受辐射诱导的皮肤损伤
为验证SP-EVs@AST水凝胶的体内辐射防护作用,该研究建立了小鼠放射性皮炎模型(50?Gy X射线照射背部皮肤)。实验分为四组,分别使用空白凝胶、SP-EVs凝胶、AST凝胶及SP-EVs@AST水凝胶进行处理,并在照射前进行适应性给药。以照射次日为第1天,分别在第1、4、8、12天更换新凝胶,并于第8天(n=4)及第16天(n=6)处死小鼠取材,同时记录第1至16天的皮肤损伤进展。实验结果表明,SP-EVs@AST水凝胶显著减轻了放射性皮肤损伤:第1天急性损伤面积较小,第4天未见干性脱屑,第8天无明显红斑与水肿;第12天开始出现痂皮脱落,提示皮肤更新;第16天可见毛发生长及修复迹象。相比之下,辐照组表现为严重渗出、溃疡及出血。RTOG评分结果进一步证实,SP-EVs@AST水凝胶显著延缓了皮炎的发生,促进了创面愈合与皮肤再生,与其他处理组相比,表现出更优的体内辐射防护与修复效果。

图5 SP-EVs@AST水凝胶保护小鼠免受辐射诱导的皮肤损伤
6.SP-EVs@AST水凝胶减轻异常皮肤组织学变化
为探究SP-EVs@AST水凝胶对放射性皮肤组织损伤的修复作用,对小鼠背部皮肤进行组织学分析。H&E染色显示,中期时SP-EVs@AST水凝胶组表皮状况明显优于辐照组;末期时,SP-EVs@AST水凝胶组表皮结构完整,而辐照组、空白水凝胶组、SP-EVs凝胶组及AST凝胶组均表现出相对严重的损伤与溃疡。Masson及Picrosirius Red染色提示,SP-EVs@AST水凝胶组胶原纤维排列有序,区别于其他组紊乱结构。激光散斑成像结果表明,该组维持良好皮下血流,而辐照组存在明显血流不足。进一步检测显示,SP-EVs@AST水凝胶降低了辐射诱导的I型胶原(COLI)过度沉积,并显著上调表皮干细胞标志物整合素α6(Itgα6)及增殖相关标志物Ki67的表达,促进干细胞增殖迁移及表皮再生。综上,SP-EVs@AST水凝胶通过改善微循环、抑制胶原沉积并保护干细胞的增殖活性,加速了辐射性皮炎的组织修复与再生。

图6 SP-EVs@AST水凝胶减轻异常皮肤组织学变化
7.SP-EVs@AST 水凝胶抑制氧化损伤,减轻炎症,并维持线粒体稳态
该研究进一步验证了SP-EVs@AST水凝胶在辐射性皮肤损伤中的抗氧化和抗炎作用。体内实验表明,SP-EVs@AST水凝胶显著降低了脂质过氧化产物丙二醛(MDA)的水平,同时提升了超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)的活性,从而增强了抗氧化防御能力。RT-qPCR和ELISA结果显示,该水凝胶有效降低了促炎细胞因子IL-6、TNF-α和IL-1β的表达,同时上调了抗炎因子IL-10和转化生长因子β(TGF-β),表明其具有调节免疫炎症反应的能力。免疫组化和免疫荧光染色进一步证实了上述炎症因子的表达变化。此外,中性粒细胞浸润指标髓过氧化物酶(MPO)的水平在SP-EVs@AST组保持正常,而在辐射组显著升高。更重要的是,透射电子显微镜观察发现,SP-EVs@AST水凝胶有效缓解了辐射引起的线粒体嵴结构破坏及肿胀,维持了线粒体稳态。综上所述,SP-EVs@AST水凝胶通过抑制氧化损伤和炎症反应,保护线粒体功能,表现出显著的放射性皮肤防护效果。

图7 SP-EVs@AST 水凝胶抑制氧化损伤,减轻炎症,并维持线粒体稳态
8.SP-EVs@AST水凝胶干预下放射性皮炎基因表达的综合分析
为评估SP-EVs@AST水凝胶对放射性皮炎的基因调控作用,对第16天的对照组、辐照组及SP-EVs@AST水凝胶组的皮肤样本进行了RNA测序分析。结果显示,辐照组与SP-EVs@AST水凝胶组之间存在1173个差异基因,其中914个基因上调,259个基因下调。通过GO富集分析,发现这些差异基因主要涉及角质包被层、脂肪酸代谢、胶原相关细胞外基质及膜结构等生物学功能。KEGG分析进一步显示,差异基因在ECM-受体相互作用、细胞黏附分子、蛋白消化吸收、Th1/Th2分化、金黄色葡萄球菌感染及炎症性肠病等代谢通路中显著富集。这些生物学过程与放射性皮炎的多种病理特征相吻合。基于这些结果,选择了部分基因集进行目标基因聚类分析,结果表明SP-EVs@AST水凝胶组上调了与细胞迁移相关的基因(如Dab1、Adtrp、Thbs4、Enpep),促进了细胞增殖、血管生成与修复;同时,该组还上调了角质细胞相关的LCE家族基因,有助于维持皮肤屏障功能。相比之下,辐照组中白细胞相关基因(如Jaml、Cd177)显著上调,提示炎症反应加剧。

图8 SP-EVs@AST水凝胶干预下放射性皮炎基因表达的综合分析
9.SP-EVs@AST 水凝胶通过调控Nrf2/Keap1/HO-1/NQO1通路促进机体抗氧化功能
为探究SP-EVs@AST水凝胶缓解辐射诱导氧化应激的机制,该研究从氧化应激、氧化应激凋亡和活性氧产生三个方面对差异基因进行分析。结果显示,SP-EVs@AST水凝胶干预显著调控了Pparg、Nrf2、Keap1等氧化应激相关基因的表达,这些基因主要富集于Nrf2/Keap1/HO-1/NQO1抗氧化信号通路。该通路通过调节抗氧化酶的表达来维持细胞内氧化还原平衡。RT-qPCR和免疫荧光结果显示,与辐照组相比,SP-EVs@AST水凝胶组中Nrf2、HO-1及NQO1的表达显著上调,而Keap1的表达则下调,表明其具有更强的抗氧化能力。Western blot结果进一步证实了这些变化。当使用Nrf2特异性抑制剂ML385处理后,SP-EVs@AST水凝胶组中Nrf2、HO-1及NQO1的表达下降,而Keap1的表达无明显改变,这进一步表明其抗氧化作用依赖于Nrf2通路。综上,该研究证实SP-EVs@AST水凝胶通过调节Nrf2/Keap1/HO-1/NQO1信号通路来增强辐照细胞的抗氧化能力,从而保护线粒体免受氧化损伤。此外,Nrf2的激活还可以促进线粒体的生物发生和修复机制,进一步维持线粒体的完整性。

图9 SP-EVs@AST水凝胶调控Nrf2/Keap1/HO-1/NQO1通路
10.生物安全性评估
为评估SP-EVs@AST水凝胶的生物安全性,该研究进行了体内外毒理学分析。体外红细胞溶血实验结果表明,SP-EVs@AST水凝胶及其各组分的溶血率均低于1.5%,未观察到明显溶血现象。在体内实验中,小鼠每隔4天接受一次不同水凝胶处理,持续28天,随后采集血液及主要脏器(包括心、肝、脾、肺、肾和皮肤)进行毒性评估。血常规及血生化检测结果显示,SP-EVs@AST水凝胶对血细胞、肝功能(AST、ALT)和肾功能(BUN)均无显著影响。主要脏器的H&E染色未见组织损伤,皮肤组织的H&E、Masson及Picrosirius Red染色也未发现不良改变。上述结果表明,SP-EVs@AST水凝胶具有良好的生物相容性和长期使用安全性,符合放射性皮炎皮肤防护制剂的基础安全要求。

图10 生物安全性评估
研究总结
该研究构建了负载虾青素(AST)的工程化微藻细胞外囊泡(SP-EVs@AST),显著提升了AST的溶解性与稳定性,同时保持了SP-EVs的结构完整性与生物活性,协同缓解了辐射诱导的氧化应激、线粒体损伤及炎症反应。为实现局部皮肤递送,SP-EVs@AST被封装于由醛基化透明质酸与羧甲基壳聚糖自组装形成的可降解水凝胶中,制得可贴敷的皮肤防护敷料,表现出良好的放射性皮炎预防潜力。该合成策略为SP-EVs递药提供了通用方法,有望扩展为可负载多类治疗剂(包括亲水/疏水小分子、核酸及蛋白质)的多功能递送平台。与复杂的内源性载药策略不同,该体系利用超声介导包封,无需对母细胞进行复杂遗传改造,具备工艺简便、可规模化的优势。

图 11 工程化微藻细胞外囊泡(SP-EVs@AST)通过调控线粒体稳态预防放射性皮炎
论文第一作者为浙江大学博士生崔家榕和浙江大学爱丁堡大学联合学院博士后董佳,浙江大学周民教授为论文的通讯作者。上述研究得到了浙江大学鄂尔多斯鄂托克生物医药联合研究中心项目、国家重点研发计划、国家自然科学基金,以及浙江大学国际校区博士后"潮涌计划"专项支持等基金项目的大力支持。
全文链接 https://pubs.acs.org/doi/10.1021/acsnano.5c07135
- 南华大学刘阳团队 IJBM:一种单宁酸交联的基于苯硼酸改性羧甲基壳聚糖的多功能水凝胶 2025-02-23
- 中国农科院植保所农药创新中心 CEJ:利用农药分子噁霉灵诱导海藻酸钠和羧甲基壳聚糖混合水溶液构建性能优异的超分子载药水凝胶 2022-09-20
- 武大周金平教授团队《ACS AMI》:具有自修复性能的羧甲基壳聚糖注射型水凝胶敷料的快速制备 2021-05-25
- 合工大方华高副教授/ 丁运生教授团队 Macromolecules:动态交联的近晶型液晶弹性体结构与性能研究的新进展 2023-09-23
- 北化卢咏来教授团队《Chem. Mater.》:动态共价交联的橡胶基体辅助构筑高度垂直排列取向的BN微观结构用于高性能热界面材料 2023-06-27
- 清华大学徐军课题组《Mater. Horiz.》: 热-紫外调控的动态共价交联弹性体用于光刻转印柔性电路 2022-10-13
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
