相对于传统的电子闭壳层荧光团,阳离子自由基的基态与激发态能级差较小,有望发展为一类新型的红至近红外荧光团,在生物医学领域具有重要的应用潜力。然而目前文献中报道的绝大多数阳离子自由基的荧光量子效率很低,例如:经典的阳离子自由基Wurster''s Blue在室温下的量子效率小于0.1%。另外,阳离子自由基在生理环境下易于发生亲核反应、自由基聚合反应等,严重限制了阳离子自由基在荧光成像中的应用。
近日,香港中文大学(深圳)唐本忠院士、华南理工大学高蒙副研究员、张云娇教授和广西中医药大学刘锴副研究员合作,以2,5-二甲基吡咯为核心骨架,通过修饰锌(II)-二甲基吡啶胺,制备了P-DPA-Zn化合物,进一步通过空气氧化,简便、高效地制备了水相中稳定且深红光发射的阳离子自由基P?+-DPA-Zn,并成功将其用于突变 p53癌症诊疗(图1)。
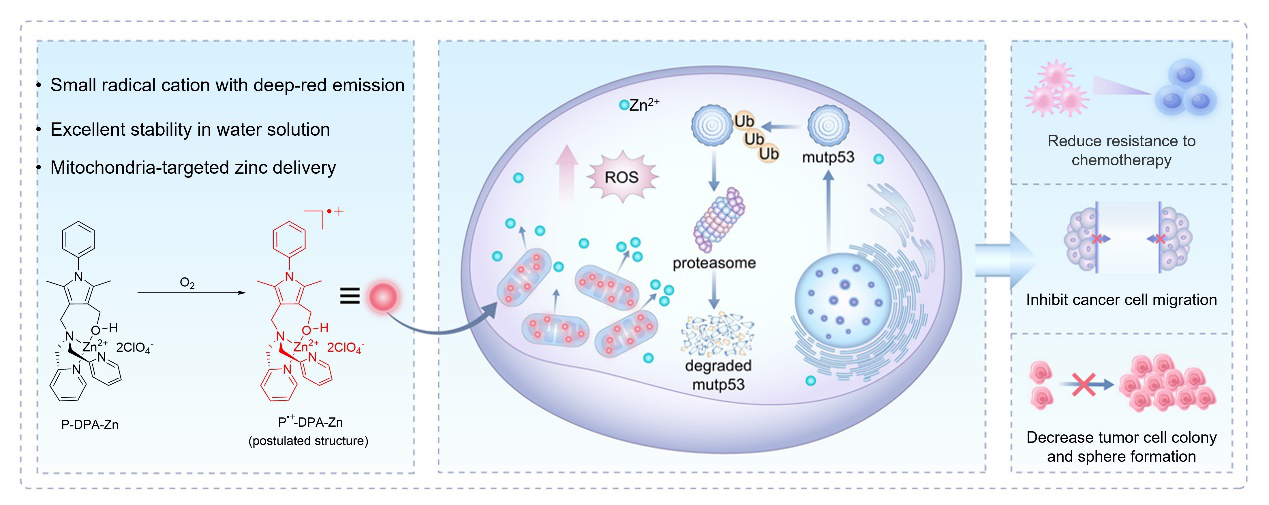
图1发光阳离子自由基P?+-DPA-Zn的制备及突变 p53癌症诊疗
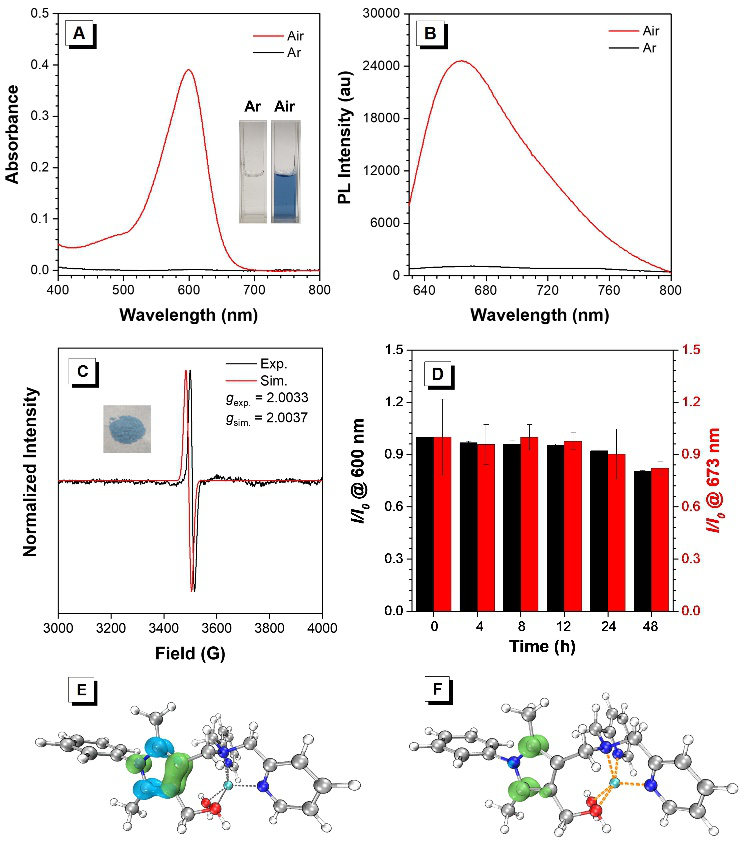
图2 P?+-DPA-Zn的结构及光物理性质表征与理论计算分析
作者发现阳离子自由基P?+-DPA-Zn具有癌细胞线粒体靶向富集能力,不仅可实现线粒体高信噪比荧光成像,还可用于线粒体靶向锌离子递送(图3),诱导线粒体氧化应激生成活性氧,促进突变p53蛋白与锌离子结合,进而通过泛素-蛋白酶体途径降解突变p53蛋白(图4)。相对于正常细胞和野生型p53癌细胞,P?+-DPA-Zn可选择性降低突变p53癌细胞存活率,抑制其增殖与迁移,克服其化疗耐药性,消除突变p53的获得性功能(图5)。

图3 P?+-DPA-Zn的线粒体靶向成像及锌离子递送


图5 P?+-DPA-Zn选择性降低突变p53癌细胞存活率并消除其获得性功能
本研究首次制备了水相中稳定且深红光发射的吡咯阳离子自由基,为发光阳离子自由基的构建及生物诊疗应用提供了一种新策略。
论文信息:
A Water-Stable and Red-Emissive Radical Cation for Mutp53 Cancer Therapy
Zikai Zhou,? Jieying Qian,? Kai Liu,* Yunjiao Zhang,* Meng Gao,* Ben Zhong Tang*
Angewandte Chemie International Edition
DOI: 10.1002/anie.202212671
https://onlinelibrary.wiley.com/doi/10.1002/anie.202212671
