在自然界中,许多生物组织、器官和细胞外基质都是由适应性水凝胶组成的。在这些水凝胶基生物中,一系列的生物聚合物,如多糖、黑色素,被控制合成,并在生物活性中发挥重要作用。受此启发,人工操控聚合物在水凝胶中原位生物合成将是获得可以满足生物需求材料的一个非常重要的途径。然而,由于生物环境及水凝胶体系的高度复杂性,这项任务仍极具挑战性。

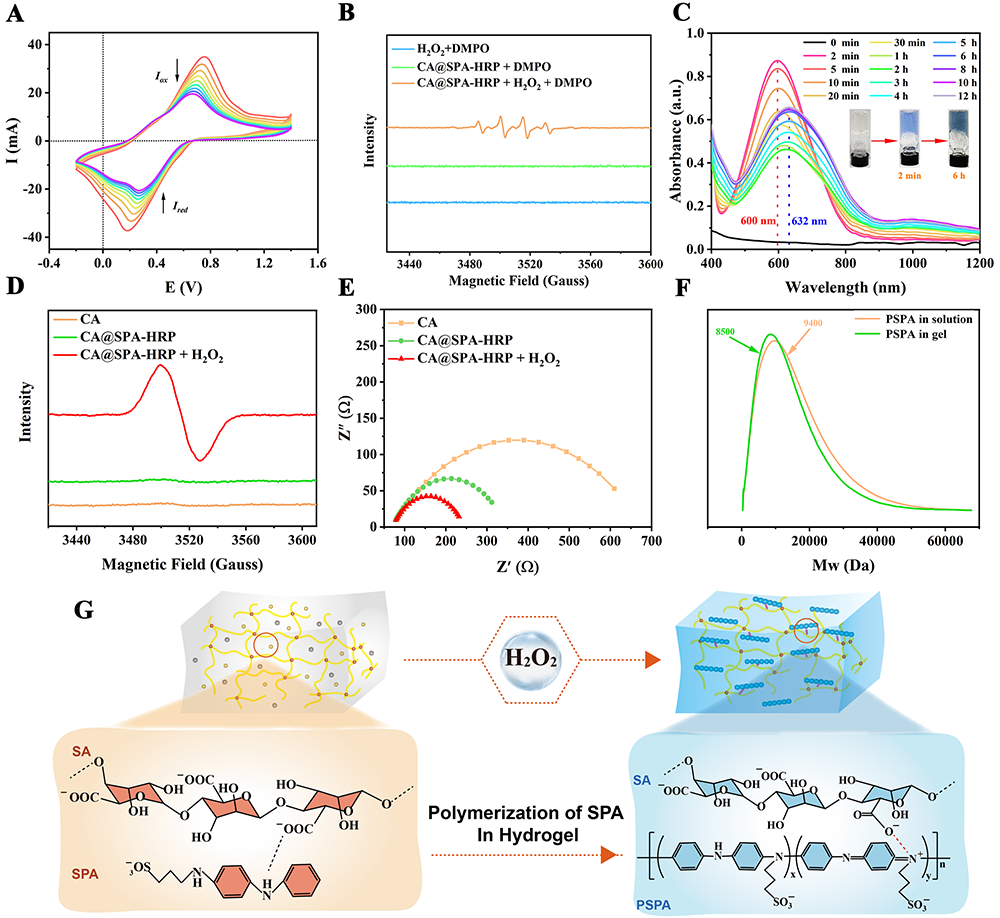
SPA低的氧化还原电位(图2A),以及HRP能够催化H2O2产生?OH(图2B),为CA@SPA-HRP水凝胶中SPA的原位聚合提供了化学基础。此外,EPR、EIS和GPC(图2D、E、F)进一步证实了SPA在水凝胶中的原位聚合生成PSPA。结合?OH生成的结果,表明HRP催化H2O2生成的?OH可以有效地激活SPA单体的原位聚合,获得PSPA。

PSPA优异的NIR吸收能力,赋予了SPA在水凝胶中原位聚可用于H2O2响应的NIR介导的诊疗应用。即使在H2O2浓度为50 mM时(图3B),仍能检测到光声(PA)信号。表明该聚合方法对H2O2具有较高的检测灵敏度,是检测H2O2的一个很好的模型反应。动物实验进一步证实裸眼观察和PA可被用于实时监测伤口感染,感染组织有明显的肉眼可见颜色变化以及PA信号变化。随着粘附时间的增加,PA信号逐渐增强,这与感染创面CA@SPA-HRP水凝胶颜色变化的结果一致(图3C和D)。

通过监测不同治疗组处理后的光密度(OD600),进一步研究了CA@PSPA-HRP水凝胶在不同孵育时间点的抗菌效果(图4A和B)。孵育2 h后,未被杀死的细菌在化学动力学治疗(CDT)组和光热治疗(PTT)组中开始增殖,而PTT/CDT组的细菌即使在孵育24 h后仍受到显著抑制。此外,细菌SEM(图4C)也进一步证明PTT联合后续的CDT比单一治疗更能实现有效的抗菌效果。
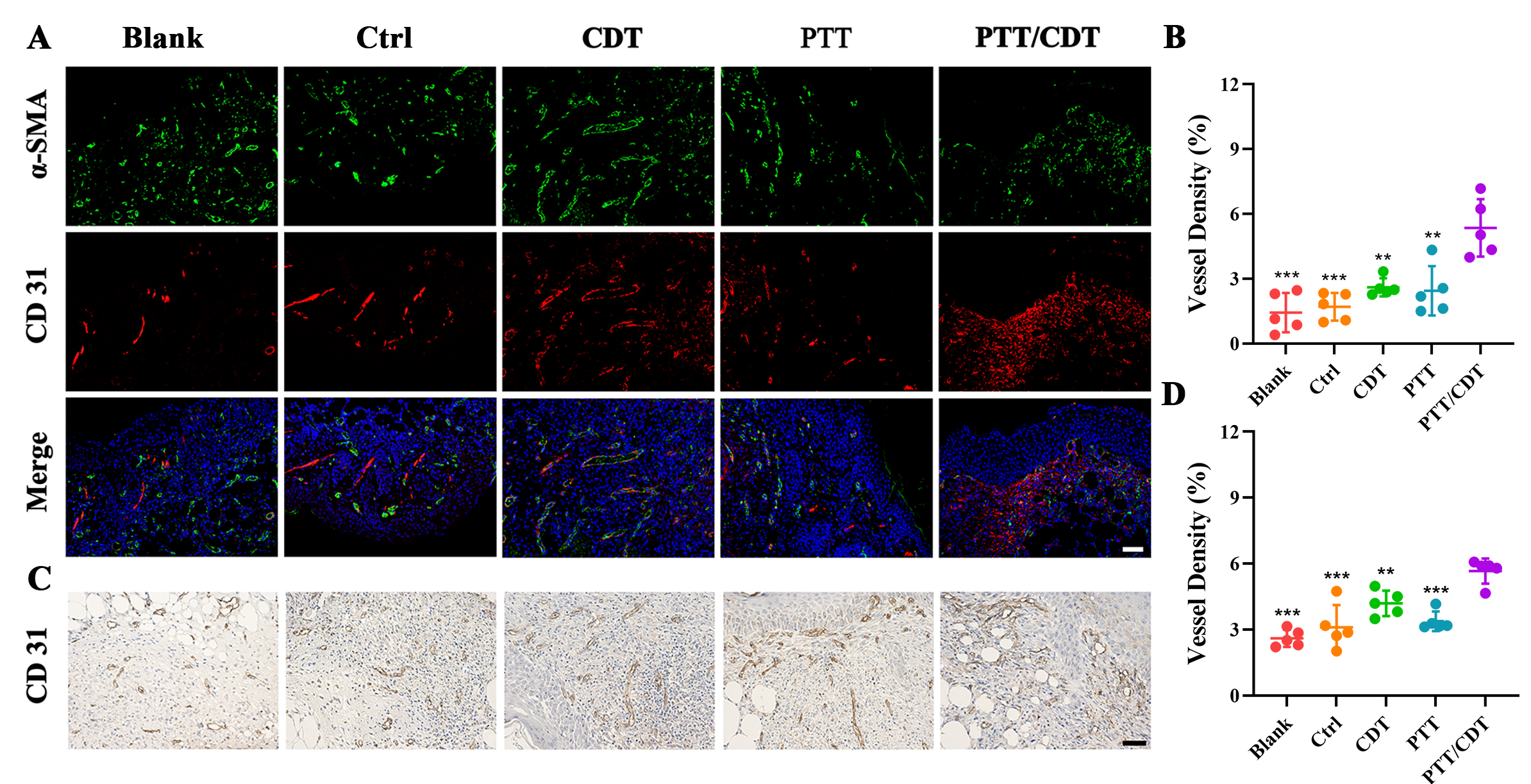
新生血管直接影响伤口中O2和营养物质的运输。CD31是新生血管的标志物,a-SMA是血管平滑肌细胞的标志物,通常用于评估新生血管重塑和伤口愈合。在第7天对创面组织切片进行a-SMA和CD31的双染色,PTT/CDT组的血管密度和成熟指数显著升高,说明具有PTT/CDT协同的CA@PSPA-HRP水凝胶可促进血运重建,从而加速伤口愈合。
该工作以“H2O2-activated in situ polymerization of aniline derivative in hydrogel for real-time monitoring and inhibition of wound bacterial infection ”为题发表在《Biomaterials》上。广西师范大学化学与药学学院博士研究生王瑷辉,硕士研究生樊桂师为该论文第一作者,沈星灿教授和蒋邦平教授为该论文通讯作者。该工作获得了国家自然科学基金项目(21977022,22265004,21671046)和广西自然科学基金项目(2018GXNSFFA281004,2017GXNSFGA198004,AD17129007)的资助。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S0142961222004380
下载:H2O2-activated in situ polymerization of aniline derivative in hydrogel for real-time monitoring and inhibition of wound bacterial infection
- 宁波材料所陈涛/路伟团队 Adv. Mater.:通过盐析后聚合制备具有超长寿命的高温磷光水凝胶 2026-05-17
- 多伦多大学Eugenia Kumacheva团队 AFM:AI赋能多组分复合水凝胶逆向设计-精准定制仿生粘弹性网络 2026-05-14
- 兰州大学吕少瑜 Angew:水驱动相变水凝胶 2026-05-12
- 湖南大学蔡仁教授等《ACS Nano》:用于闭环伤口治疗的Pd@Au Nanoframe水凝胶 2025-04-19
- 广西师大沈星灿教授、蒋邦平教授、梁宏教授团队:二价阴离子驱动溶菌酶凝胶化的普适性策略及其免疫记忆抗糖尿病伤口感染复发 2024-09-09
- 加州理工学院高伟教授团队《Sci. Adv.》: 慢性伤口感染检测和治疗的可穿戴生物电子系统 2023-04-06
- 西安交大陈鑫教授课题组 Small:具有生理响应性光热转换和纳米催化医学能力的智能水凝胶-可综合抑制细菌和炎症、治疗感染性伤口 2024-10-15
