近年来,由于较高的发病率和死亡率,肝衰竭已经对人类的健康构成了严重的威胁。胆红素是肝脏的一项功能指标,肝功能或者代谢障碍的患者往往无法有效结合胆红素,而未结合的胆红素不能被及时排除,因而可能导致黄疸,严重的可进一步导致不可逆的脑损伤,甚至死亡。
基于血液灌流的非生物型人工肝支持系统已经被广泛用于治疗不同类型的肝衰竭。作为原位肝移植的替代疗法,该系统对于在肝脏供体配型期间稳定患者的身体状况具有较高的临床意义。但是,现有血液灌流吸附剂对胆红素的清除效率大多不高,并且还存在着制备工艺复杂等问题。另一方面,这些吸附剂通常血液相容性较差,需要配合血浆分离系统使用,无法进行全血胆红素清除。此外,基于静电作用或离子交换清除胆红素的吸附剂还可能干扰血浆 pH 的稳态,这些都制约了其在临床治疗中的应用。再者,血液灌流过程中为防止凝血注射的水溶性抗凝剂会通过血液循环回到患者体内,可能导致大出血或其它副作用。更糟糕的是,因为凝血因子主要在肝脏中合成,肝衰竭患者可能会出现获得性出血障碍,因此抗凝剂的使用可能会进一步加大出血风险。在这种情况下,如何有效地从全血中直接去除胆红素,同时解决使用抗凝剂带来的相关隐患仍然是一个悬而未决的问题。
为此,四川大学高分子科学与工程学院赵长生教授课题组合成了类肝素生物大分子,利用自牺牲微反应器方法,将其与还原氧化石墨一起引入聚丙烯酰胺共价交联网络,制备了具有高效胆红素吸附能力和良好的血液相容性、特别是优秀的自抗凝血性能的吸附微球来解决上述问题。相关论文近日被Biomarcomolecules(影响因子为6.092)接收。课题组赵伟锋副研究员为本文通讯作者,硕士研究生宋昕、本科生徐滔为本文共同第一作者。
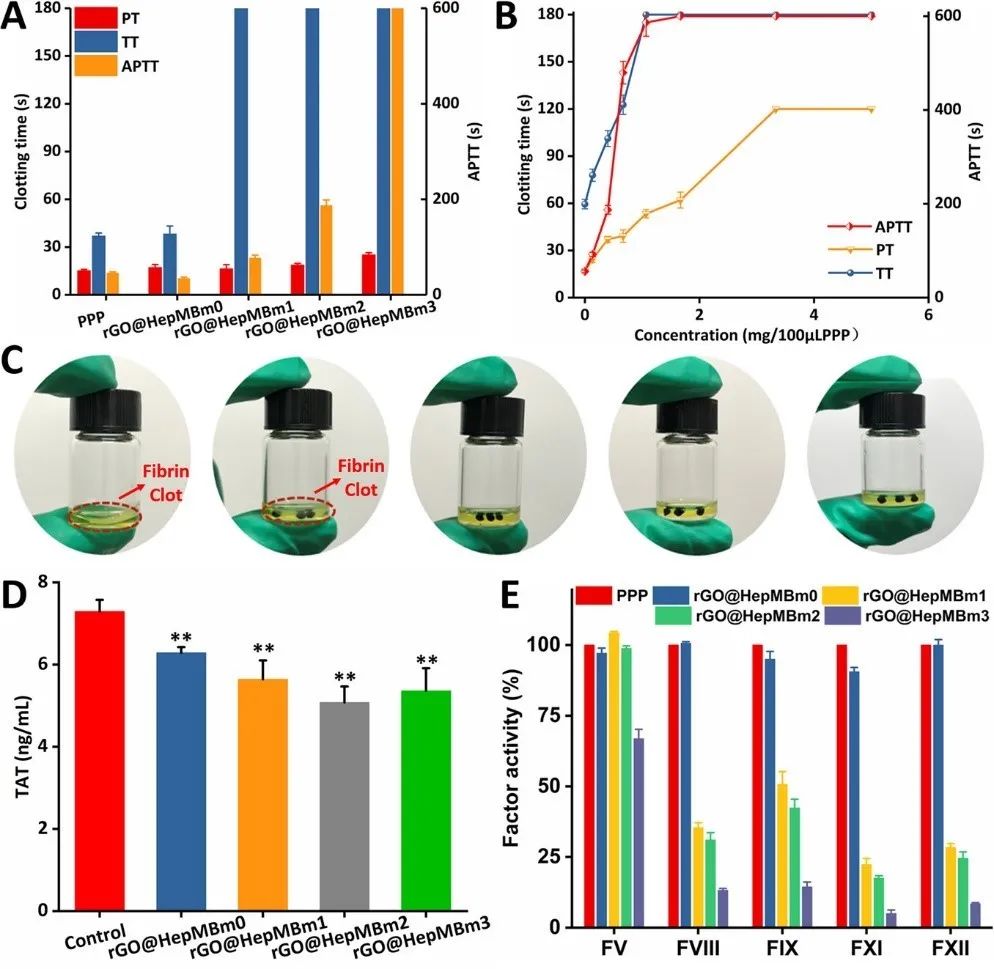
该微球表现出了优秀的抗凝血性能,对于活化部分凝血活酶时间、凝血酶时间和血浆复钙时间均有显著延长,同时对于内源性凝血因子VIII、IX、XI、XII的活性有明显的抑制作用。
该微球不会诱导血小板激活和接触激活,无溶血,对血细胞形貌、体积分布、数量无明显影响,可以抑制补体激活系统和凝血酶-抗凝血酶复合物的产生,并且有优秀的细胞相容性。

通过模拟血液灌流器直接过滤含有高浓度胆红素的全血,胆红素去除率可达 99.69 %。
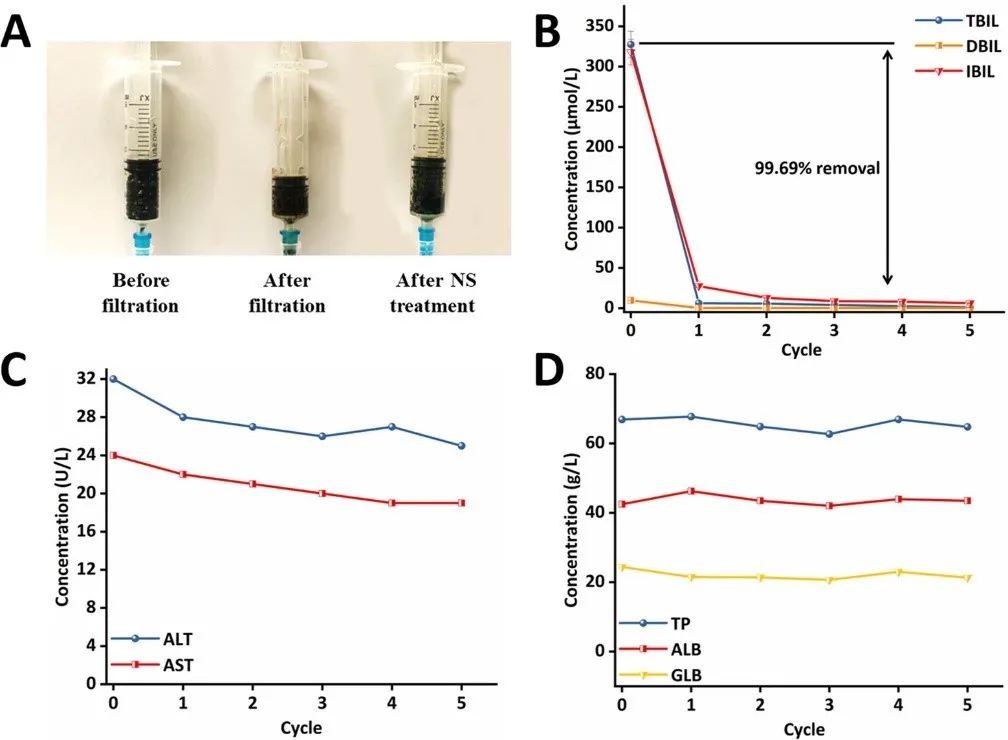
总之,微球的优异的血液相容性、极好的抗凝血性能和强大的胆红素清除能力,既可以避免血液灌流过程中血栓的形成,大大减少抗凝血剂的使用,又可以免去血浆分离的步骤,实现全血直接清除胆红素,该微球为设计新一代非生物人工肝提供了新的契机,也为佩戴式人工肝带来了新的希望,因为摆脱血浆分离系统和肝素泵后,整个非生物人工肝系统可以变得非常轻便,为人的佩戴提供足够的舒适度。
全文链接:https://pubs.acs.org/doi/10.1021/acs.biomac.9b01686
