肿瘤放射治疗是采用电离辐射针对局部肿瘤进行杀伤的临床治疗手段。然而,放疗治疗效果往往受到肿瘤放疗耐受、照射剂量不足以及治疗期间无法实时、快速可视化治疗效果等方面的限制。贵金属纳米材料能高效吸收辐射线沉积的辐射能量,可作为放疗增敏剂用于增强放疗治疗效果。然而,这一策略也面临着肿瘤深部组织渗透的障碍。因此,迫切需要开发能够促进放疗增敏剂肿瘤内渗透,又能实时报告肿瘤放疗效果的新型放疗策略。
最近,来自中国科大生命科学学院的王育才教授团队在ACS Nano上报道了一种能够同时增强主动细胞转运和被动扩散引起肿瘤深部组织渗透增强的放疗增敏剂--金纳米颗粒石榴组装体(RNPs),并能够实现实时、可视化放疗效果的反馈报告。RNPs在中性pH条件下保持稳定的大尺寸以延长血液循环,实现肿瘤部位高效富集;而在肿瘤pH条件下,RNPs内部的酸响应聚合物会发生质子化引起颗粒崩解,释放出大量的表面正电性的超小金颗粒,其可以借助尺寸和正电荷介导的被动扩散和主动细胞转运实现肿瘤深层渗透,显著增敏了肿瘤深部组织的放疗(图1)。根据细胞凋亡过程中caspase-3活化程度,超小金颗粒可释放其表面被淬灭的荧光分子,快速恢复的荧光反馈信号与细胞凋亡成正相关,进而实现实时荧光定量检测报告放疗效果。
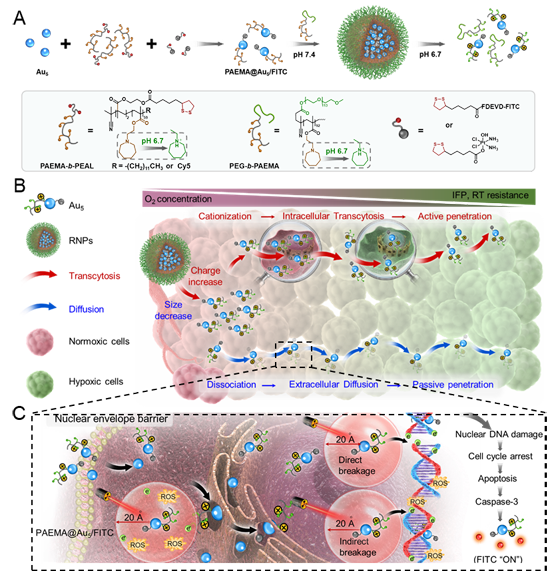
图1、(A)RNPs组装体的制备过程;(B)RNPs在肿瘤部位崩解引起组装体崩解及表面电荷反转,增强金颗粒扩散的同时促进细胞转运。(C)RNPs增敏放疗促进DNA的损伤并报告凋亡。
研究者首先通过RAFT连续聚合成功制备了酸响应聚合物,将其修饰在金颗粒表面。研究发现,通过精准控制聚合物和金颗粒的比例可以得到不同尺寸、均一且稳定的RNPs组装体。该纳米石榴在中性pH条件下保持稳定的大尺寸;而在肿瘤pH条件下,RNPs内部的酸响应聚合物会发生质子化引起颗粒崩解,释放出大量的小尺寸和阳离子表面的 Au5(5 nm金颗粒),这种特性使得纳米石榴具有很长的体内循环和优异肿瘤主动和被动渗透性能。在渗透进入肿瘤深部之后,金颗粒可以有效增加放疗产生的DNA损伤(图2)。
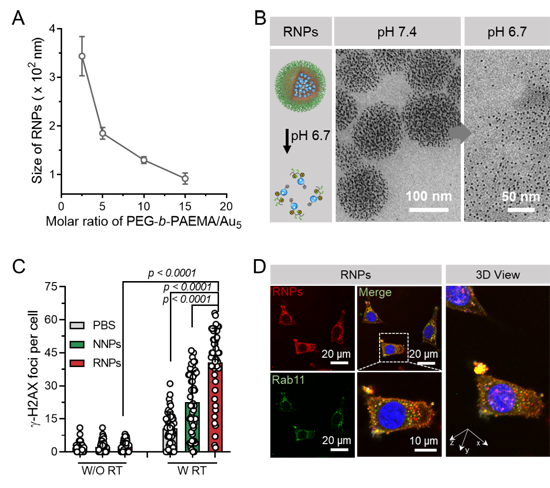
图2、(A)RNPs的尺寸随金颗粒和聚合物比例不同下的变化;(B)RNPs在正常pH下和肿瘤pH下的透射电镜照片;(C)RNPs增敏放疗对细胞产生的DNA损伤程度统计;(D)共聚焦检测RNPs在细胞中和循环内涵体的共定位图像。
该团队将RNPs尾静脉注射进入小鼠体内之后,随着时间的推移,大部分RNPs迅速穿过肿瘤血管,向肿瘤深部组织发生主动细胞转运和被动扩散,并逐渐弥散在整个肿瘤组织(图3)。RNPs的快速渗透一部分是因为其响应肿瘤部位酸度快速崩解后释放出大量小尺寸的颗粒,加速了肿瘤间隙的扩散;与此同时,RNPs发生表面阳离子化,大量的Au5表面带有很高的电荷,能够有效促进细胞转运引起的主动渗透。因此,本工作以肿瘤响应RNPs组装体为平台,促进了放疗增敏剂在肿瘤部位的主动和被动双重渗透,高效增敏了深层肿瘤组织的放疗。
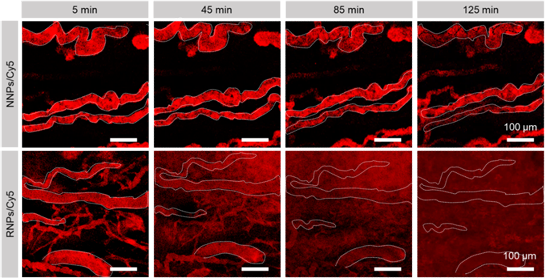
图3、在尾静脉注射RNPs之后,RNPs在肿瘤血管周围的分布随时间变化。
基于5 nm金颗粒与荧光分子FITC之间存在荧光淬灭效应导致荧光强度降低的原理,研究者设计了实时报告原件并进行组装得到报告纳米石榴(RNPs/FITC),通过监测肿瘤部位荧光信号的强度,可表征caspase-3的含量,从而实现肿瘤凋亡的监测。Au5与荧光分子FITC通过caspase-3响应剪切多肽DEVD链接。由于纳米颗粒表面能量转移(NSET)可以响应肿瘤部位caspase-3浓度从而报告肿瘤的凋亡程度。据此,研究者通过监测FITC的荧光强度来判断肿瘤的治疗效果,并可以区分肿瘤的放疗耐受性(图4)。
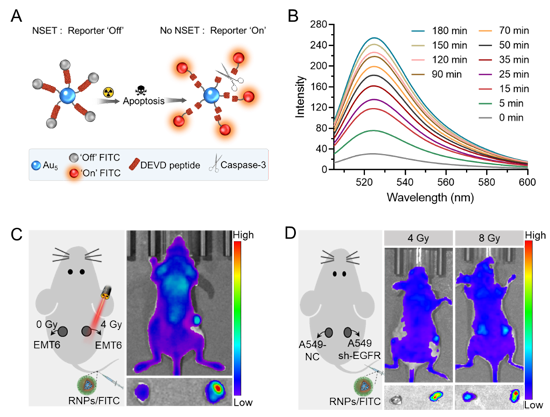
图4、(A)5 nm金颗粒和FITC之间的NSET机理图,在caspase-3条件下,DEVD多肽被剪切,FITC释放之后荧光恢复;(B)RNPs/FITC在和Caspase-3孵育之后不同时间点的荧光光谱;(C)活体显微成像系统检测EMT6肿瘤放疗效果的报告荧光图像;(D)活体显微成像系统检测不同放疗敏感度的肿瘤在不同剂量下的报告荧光图像。
该研究以肿瘤酸响应聚合物和金颗粒为平台,通过精准、可控自组装、搭载可视化报告原件增强肿瘤部位双重渗透并快速检测治疗效果,成功应用于增敏深层次肿瘤组织放疗;也为今后设计和合成纳米放疗增敏剂应用于深层次肿瘤组织放疗提供了新的设计思路。
中国科大王立、蒋为博士与安徽医科大学第一附属医院肖亮医生为本论文共同第一作者。
该工作得到了国家自然科学基金(NOs. 91942310, 51961145109, 51773191),国家重点研发计划(2017YFA0205600)的资助。
论文信息:“Self-Reporting and Splitting Nano-Pomegranates Potentiate Deep Tissue Cancer Radiotherapy via Elevated Diffusion and Transcytosis”
https://doi.org/10.1021/acsnano.0c02674
- 东华大学史向阳教授课题组在树状大分子纳米探针用于T细胞监测上取得新进展 2020-03-29
- 宁波材料所陈涛/乐晓霞团队 Angew:水凝胶中聚合物链缠结的可视化与光编程 2026-05-09
- 太原理工大学张虎林教授 ACS Sensors:一体化可穿戴热电凝胶贴片用于多模态可视化与定量中暑监测 2026-04-05
- 中南民大张道洪教授/姜宇教授团队 Macromolecules:高性能超支化聚氨酯微相分离的原位可视化 2026-02-09
- 澳门大学代云路课题组 AFM:利用金属-多酚纳米递送平台结合可调控的低强度超声实现肿瘤放疗增敏及放疗-声动力联合疗法 2022-07-22
- 浙江大学周民团队、哈佛大学陶伟团队《Nat. Commun.》微藻放疗保护口服药物递送系统用于肿瘤放疗中肠道辐射防护和菌群调节 2022-03-20
