清华大学杜娟娟/军事医学研究院杨益隆合作团队 ACS Nano:一种激活两条天然免疫途径的无佐剂纳米疫苗
2024-03-19 来源:高分子科技
以往研究表明抗原与佐剂的协同递送可以实现抗原递呈与免疫激活的时空协调,但开发复杂的共递送系统对于亚单位疫苗的生产与质控提出了新的挑战。近期,清华大学药学院杜娟娟团队联合军事医学研究院杨益隆副研究员,发现了一种能够同时激活cGAS/STING和TLR9/MyD88两条天然免疫通路的高分子聚合物p(AMPS-co-DMAEMA)。该聚合物与新冠病毒S蛋白RBD结构域或者猴痘病毒抗原M1R蛋白共价偶联后,无需添加商业化佐剂即能在小鼠体内引起强效的体液免疫和细胞免疫应答。该工作以“A Polymer-Based Antigen Carrier Activates Two Innate Immune Pathways for Adjuvant-Free Subunit Vaccines”为题发表在《ACS Nano》上(DOI: 10.1021/acsnano.4c00925)。

针对慢性传染病的亚单位疫苗在临床试验中表现出CD8+ T细胞免疫应答较弱的局限性。为了改善亚单位疫苗的保护效果,佐剂联合的策略被广泛应用于疫苗设计中,但这种复合佐剂的共递送对于疫苗的工业化生产提出了更高的要求。近年来,一些抗原递送载体,如高分子聚合物PC7A(Luo et al., 2017)、F-PEI(Xu et al., 2020)、PEI4BImi(Zhao et al., 2022)等,表现出激活天然免疫的特性,这说明聚合物可以同时发挥佐剂和递送载体的双重作用,从而简化亚单位疫苗的组分。

图1. 体外筛选具有DC激活能力的聚合物单体组合 (Jia 2023)
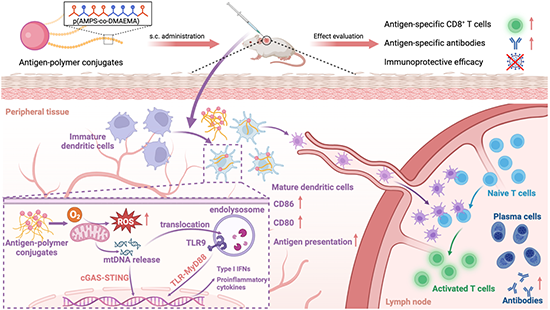
图2. 抗原-聚合物偶联物作为无佐剂纳米疫苗递送载体
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c00925
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 中科大张世武/伯明翰大学唐诗杨/伍伦贡大学李卫华《Sci. Adv.》:可主动调节刚度/电导率的导电弹性体 2023-02-04
- 西南交大朱旻昊、樊小强等 Adv. Colloid Interfac.:Ti3C2Tx MXene增强聚合物用于磨蚀防护研究进展 2022-10-13
- 东华大学武培怡/焦玉聪团队《Adv. Sci.》:凝胶电解质官能团助力锌金属(002)晶面成核 2022-01-20
- 东华大学沈明武/史向阳团队 Bioact. Mater.:基于纳米凝胶的治疗型纳米疫苗通过全周期免疫调节实现肿瘤的预防及直接治疗 2024-09-25
- 上海交大刘尽尧团队 Small:双抗原展示纳米疫苗 2023-12-08
- 天津大学王汉杰/刘培源 Biomaterials:工程菌在体可控生产释放肿瘤纳米疫苗 2023-05-18
- 中科大王育才/李敏团队 Nat. Biomed. Eng.: 设计低免疫原性mRNA递送载体在体内重编程耐受性APC 2025-04-01
