皮肤、粘膜或器官组织的伤口会给患者带来剧烈疼痛,甚至引发严重感染。如果缺乏适当护理,伤口极易被病原体侵入,阻碍愈合,迁延不愈。严重情况下,甚至可能会引发败血症等一系列并发疾患,进而危及生命。因此,对于伤口的及时监测和抗感染治疗也就具有了非常重要的临床意义。目前常用的智能伤口敷料,则往往仅局限于药物的自发释放,这类缓释策略常因缺乏对伤口感染状况相关参数如温度、pH及尿酸等的实时监控,因而难以满足按需给药、精准治疗的现实需求。因此,基于柔性电子穿戴式贴皮检测与无线无源技术,开发一种既能实现伤口原位实时监测,又能精确控制药物递送,进行相关的抗感染治疗,建立起一个贴皮式一体化的闭环反馈治疗系统,对于该类疾病的检测和治疗无疑具有重要意义。
为了实现闭环的伤口监测和药物递送治疗系统,刘清君教授团队采用柔性电子加工技术构建了一种智能伤口敷料,通过集成温度、pH、尿酸传感器以及聚吡咯(PPy)包裹头孢唑林钠的药物缓释电极,结合近场通信技术(near field communication,NFC)实现了无线无源的伤口原位多参数实时监测以及电控抗生素释放治疗。
在该智能伤口敷料的设计中,采用了正反双层结构以减小敷料尺寸。上层是集成有NFC模块的柔性电路板,可以实现无线能量收集、多种电化学传感方法、信号收集与处理,温度传感和药物释放控制等功能;下层为传感电极和药物控释电极,用于实施伤口pH和尿酸的检测,以及药物释放。采用带有NFC模块的智能手机靠近该贴片即可给伤口敷料无线供电、获取检测结果并根据检测到的感染数据来控制药物释放,形成闭环。

图1 无线无源的柔性闭环智能伤口敷料
电极阵列基于超薄柔性的polyimide(PI)基底构建而成,集成了尿酸、pH电化学传感电极以及药物缓释电极。为了赋予电极阵列可拉伸性能,电极与金属触点之间的导线部分采用了可拉伸蛇纹形设计,并使用生物相容的PDMS(Polydimethylsiloxane)封装。因此,电极阵列可以实现拉伸、弯折和扭曲等各种不同的形变,从而可以适应人体柔软的皮肤界面,提供与伤口表面的舒适接触。

图2 柔性电极阵列的构建和修饰
通过进一步测试,表征了该智能伤口敷料的传感特性,如图3所示。分别通过差分脉冲伏安法和开路电势法检测了尿酸、pH传感器响应随浓度变化曲线。针对伤口渗出液存在的干扰物质的特异性测试以及线性拟合结果表明,两种传感器均具有良好的灵敏度及选择性,其中尿酸检测下限为3.11 μM;pH灵敏度为60.34 mV/decade,接近能斯特响应理论值。此外,集成的温度传感器能够实时检测伤口温度变化,精度高达0.1℃。并同时研究了pH、温度变化对尿酸检测的影响,作为实际伤口尿酸监测的标定曲线。
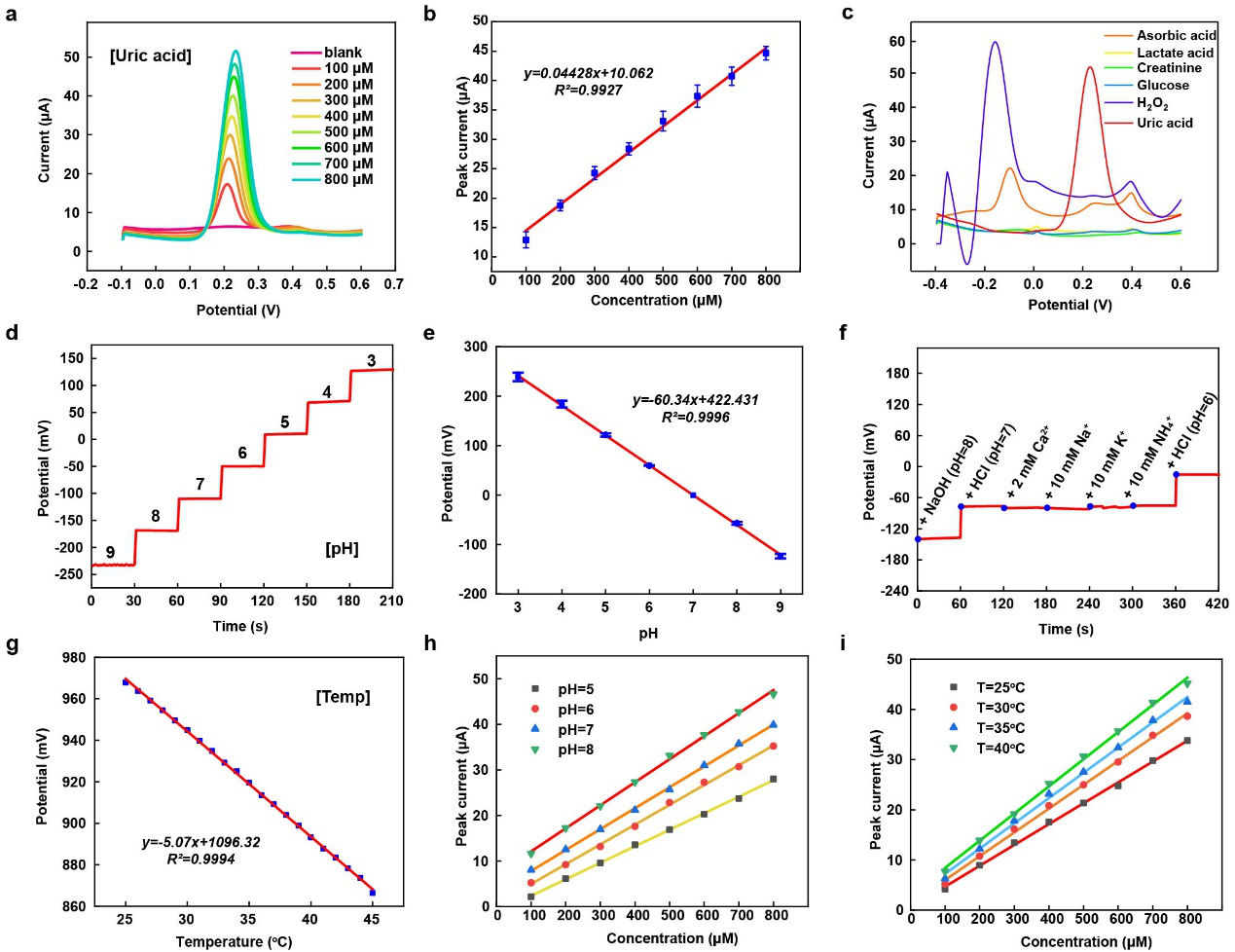
图3 尿酸、pH值和温度传感器的体外表征
电控药物释放模块是利用带正电的PPy膜包裹带负电的药物分子,当电极上施加负电激励时,药物分子会从PPy膜的主链上解离,并且在电场力和扩散作用下释放到伤口渗出液中,达到治疗伤口的目的。为了定量分析电控药物释放量,实验采用荧光素钠模拟电控药物释放过程,确定并选取-0.5 V作为电控药物释放的最佳电位。电控释放抗生素类药物头孢唑林钠实验表明,100秒内电控释放的头孢唑林累积剂量约为自然药物释放量的5倍,证实了按需电控给药的可行性。同时,通过体外的抑菌环实验表明,电控药物释放的抑菌效果接近直接给药,远高于无电控对照组。

图4 电控药物缓释
实验通过金黄色葡萄球菌在小鼠体表接种感染,形成感染伤口动物模型,用于评估智能伤口敷料在实际伤口监测与药物治疗中的应用。如图5所示,在9天的试验周期之后,接受治疗的实验组伤口平均闭合率显著高于对照组的伤口平均闭合率。同时,伤口的温度、pH和尿酸监测结果也表明,给与电控药物治疗的大鼠其伤口感染参数恢复也更好。组织切片染色结果表明,实验组的皮肤组织再生结痂更少而肉芽组织层更厚,证实了该智能伤口敷料对伤口恢复的积极促进作用。
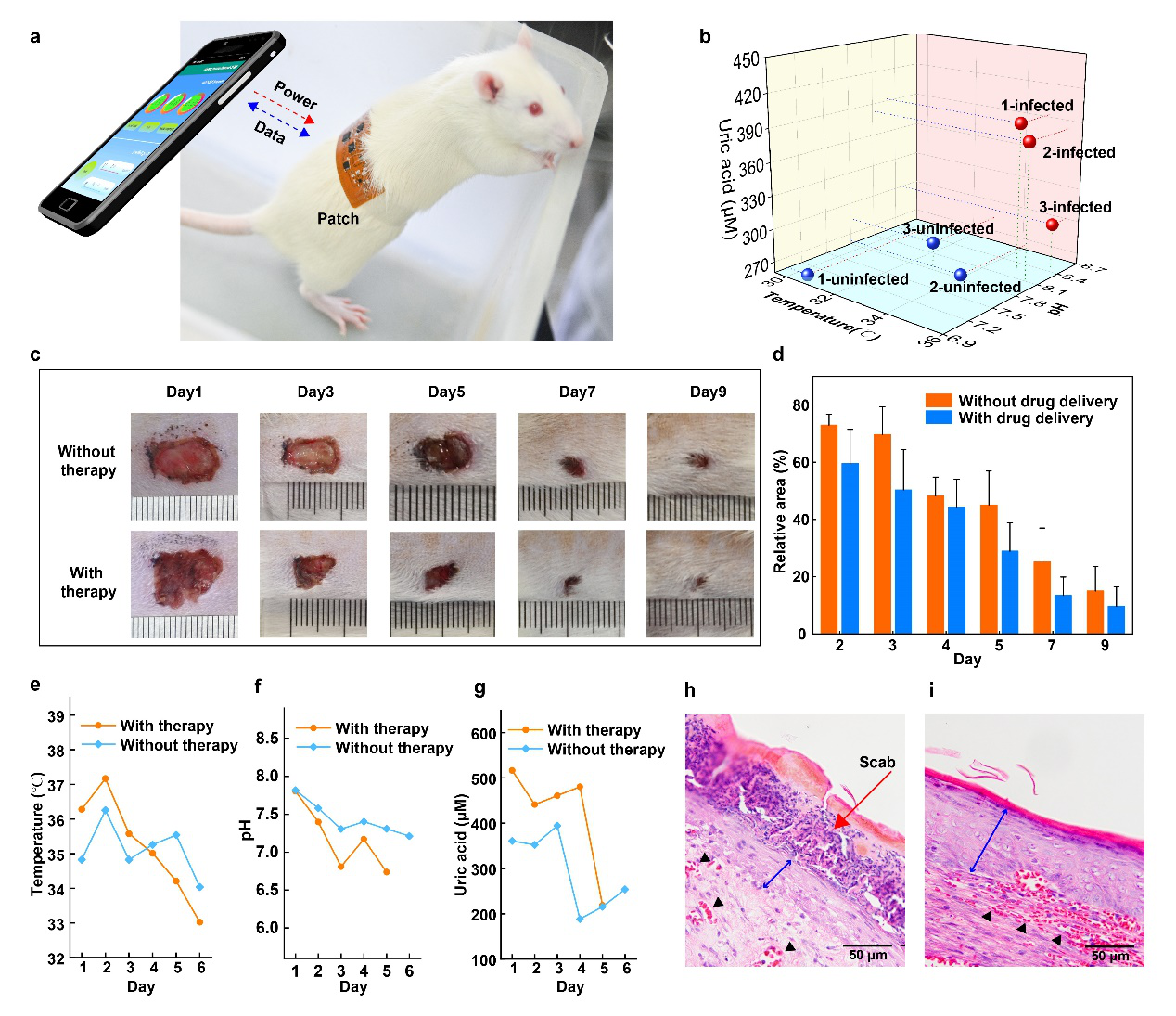
图5 伤口监测和感染治疗的在体动物实验研究
本研究提出了一种用于伤口监测与电控药物释放的闭环系统,其中多参数伤口检测的结果不仅可以作为伤口轻重程度的有效评价手段,也可作为电控药物释放的有效指导,作为药物治疗结果的反馈评估。所建立的无线无源智能伤口敷料,为临床智能传感检测与按需给药反馈治疗的一体化设计,提供了一个基于柔性电子的集成化设计范例。该基于近场通讯的无线无源即时方法,对于糖尿病坏疽、下肢静脉溃疡、压疮、严重烧烫伤等慢性伤口的穿戴式监测管理和精准治疗具有重要临床价值。
该研究成果以“Battery-Free and Wireless Smart Wound Dressing for Wound Infection Monitoring and Electrically Controlled On-Demand Drug Delivery”为题发表在期刊《Advanced Functional Materials》上。浙江大学博士许刚和浙江大学博士后卢妍利为共同第一作者,浙江大学刘清君教授为通讯作者。
原文链接:https://doi.org/10.1002/adfm.202100852
- 福州大学杨建民、石贤爱课题组 Acta Biomater.:具有细菌原位检测与清除功能的智能伤口敷料 2023-12-18
- 香港中文大学(深圳)唐本忠院士团队 Matter:基于AIEgen的真菌感染伤口监测和按需光动力治疗智能系统 2023-07-22
- 科学家即将设计出智能伤口敷料 2015-12-09
- 西安交大郭保林教授团队 Adv. Mater.:自适应伤口敷料用于伤口愈合与修复 2025-12-25
- 香港中文大学(深圳)唐本忠院士团队 AFM:自上而下法制备AIE/柔性木基伤口敷料 - 助力耐药菌感染伤口快速愈合 2025-02-13
- 烟台大学任春光团队本科生一作 IJBM:载PDRN多功能水凝胶伤口敷料促进伤口愈合 2025-02-10
- 东华大学陈志钢教授团队 AFM: 仿生设计碳纤维/二氧化钛@聚吡咯光热-电热织物用于全天候海水蒸发 2025-02-15
