生物体内可激活的级联生物反应在肿瘤治疗领域已经引起了广泛的关注。其中,芬顿或类芬顿反应能够在金属催化剂(如:Fe,Mn,Co,Cu 和 Ag等)存在的条件下催化双氧水产生高毒性的羟基自由基(?OH),是一类重要的生物级联反应,在化学动力学治疗领域扮演着非常重要的角色。有机-无机杂化材料是一类被广泛应用的级联反应载体,引入的有机组分能够提高无机纳米材料的生物相容性,丰富无机纳米材料的功能。但目前大多数该类纳米载体的构筑大多都涉及到复杂的合成或修饰过程。因此,发展一类更为高效的有机-无机杂化纳米载体构筑策略目前是该领域亟待解决的重要问题之一。
近日,山东大学郝京诚教授、崔基炜教授和深圳大学黄鹏教授团队联合开发了一种新型聚多肽-无机纳米粒子复合纳米载体(图1)。该工作通过静电自组装的方式实现了四氧化三铁纳米粒子及顺铂药物分子在聚多肽纳米载体中的快速、有效的封装。并且每个聚多肽纳米载体中的四氧化三铁数目可以通过改变初始四氧化三铁纳米颗粒的浓度进行调控(图2a-c)。在肿瘤细内涵体胞和溶酶体酸性环境中,治疗剂铂药分子和铁离子(Fe2+/3+)被释放出来,引发细胞内一系列级联反应,产生?OH进而触发铁死亡。除此之外,释放的铂药分子可以进入细胞核与DNA发生作用,诱导细胞凋亡。同时,封装的Fe3O4纳米颗粒可用于肿瘤部位T2磁共振成像的造影剂。更重要的是,这种静电自组装的方法还可以用于封装其它的功能性无机纳米材料,如金纳米颗粒、CdSeS/ZnS量子点和碳量子点等(图2d-f)。
细胞实验证明了细胞内级联生物反应的产生以及化疗与铁死亡治疗的联合治疗效果。此外,在皮下脑胶质瘤模型中,与自由药物组以及无级联生物反应组相比,化疗与铁死亡治疗的联合治疗组表现出了更优异的肿瘤抑制效果(图2g)。同时,免疫组化的结果表明该纳米载体能够显著降低自由药物分子的毒副作用,具有较高的生物安全性(图2h)。该研究针对目前有机-无机杂化纳米载体构筑过程复杂等问题,发展了一步法构筑静电自组装的普适性策略,实现了杂化纳米载体的快速有效构筑,并在肿瘤联合治疗以及诊疗一体化方面表现出了潜在的应用价值。
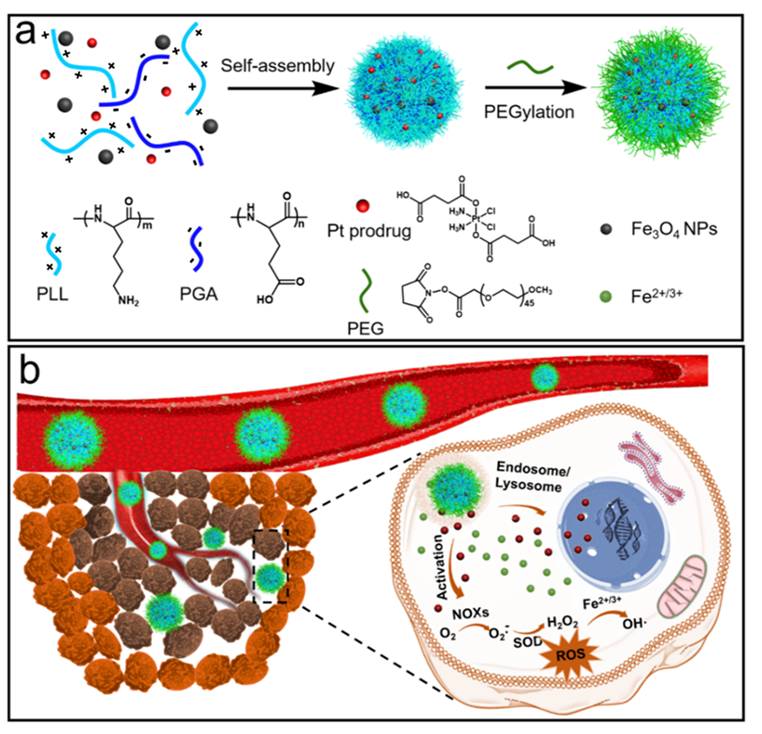
图1. 聚多肽纳米药物载体的制备及在肿瘤诊疗一体化方面的应用示意图。
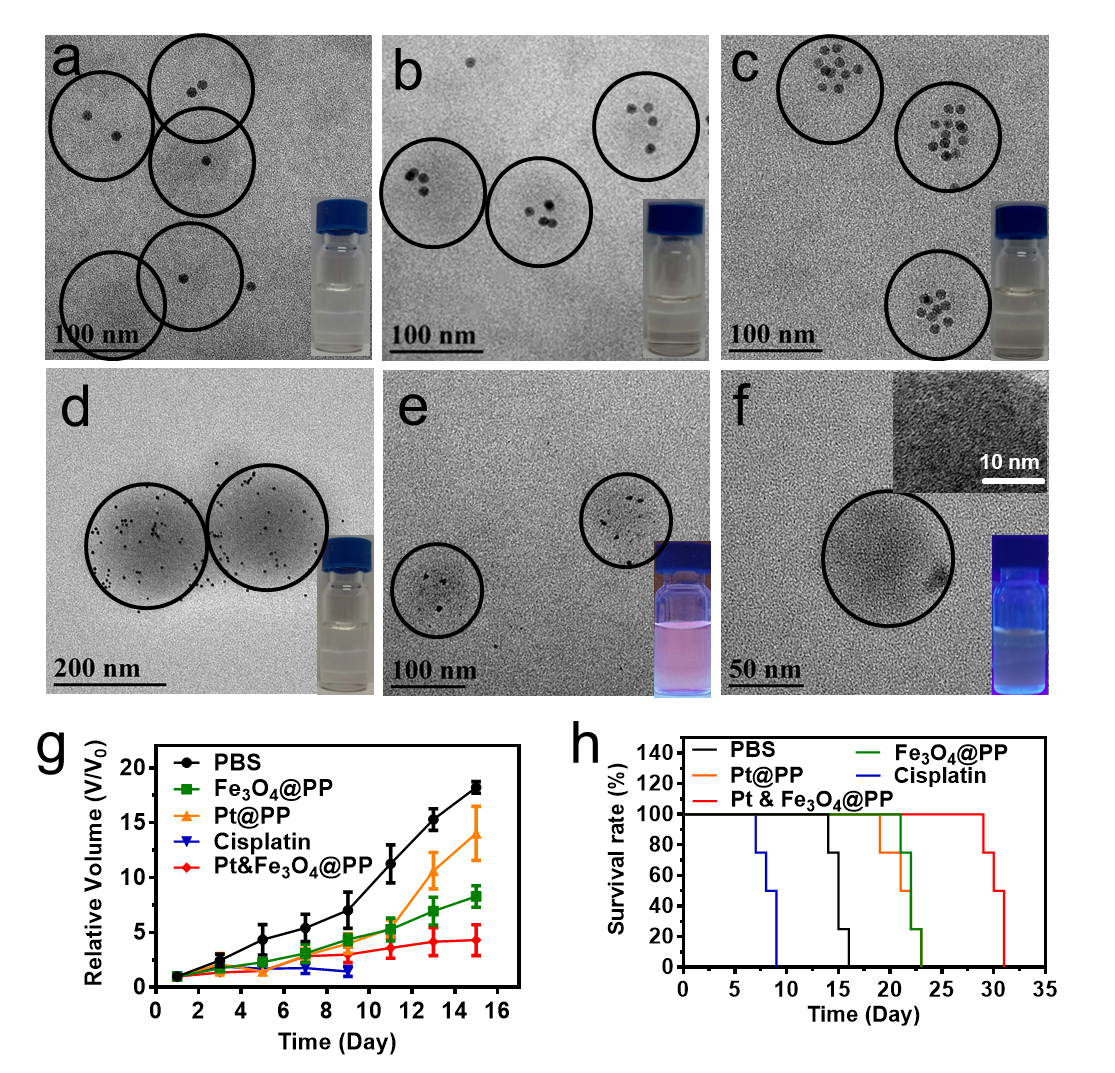
图2. (a-c)封装不同Fe3O4数量的聚多肽纳米载体。Fe3O4纳米颗粒的组装浓度分别为(a)0.1 mg mL-1,(b)0.5 mg mL-1,(c)1.0 mg mL-1。分别封装(d) 金纳米颗粒,(e)CdSeS/ZnS量子点,(f)碳量子点的聚多肽纳米载体。不同治疗组的(g)肿瘤体积监测曲线和(h)小鼠存活率曲线。
以上研究结果近期以Polypeptide-Based Theranostics with Tumor-Microenvironment-Activatable Cascade Reaction for Chemo-ferroptosis Combination Therapy为题发表于ACS Appl. Mater. Interface (2020, DOI: 10.1021/acsami.0c03748)。论文的共同第一作者为山东大学博士研究生高至亮和深圳大学贺婷博士,共同通讯作者为山东大学化学与化工学院崔基炜教授、郝京诚教授和深圳大学生物医学工程学院黄鹏教授。上述研究工作得到了国家自然科学基金委等项目的支持。
参考文献:Zhiliang Gao, Ting He, Peiyu Zhang, Xiaoyu Li, Yinling Zhang, Jing Lin, Jingcheng Hao, Peng Huang, and Jiwei Cui. Polypeptide-Based Theranostics with Tumor-Microenvironment-Activatable Cascade Reaction for Chemo-ferroptosis Combination Therapy, ACS Appl. Mater. Interface, 2020, DOI: 10.1021/acsami.0c03748.
论文链接:https://pubs.acs.org/doi/10.1021/acsami.0c03748
- 香港中文大学(深圳)唐本忠团队 Nat. Commun.:均聚多肽自组装体系圆偏振室温磷光 2026-02-24
- 大连理工大学郑楠课题组 Chem. Sci.:基于多组分反应开发二级结构可调控的N-磺酰脒基聚多肽响应肿瘤微环境 2023-12-26
- 香港中文大学(深圳)唐本忠院士团队 JACS:均聚多肽自组装诱导的水相圆偏振发光纳米材料 2023-12-14
- 上海理工大学宋文良/余灯广:聚苯丙氨酸与聚(3,4-二羟基-L-苯丙氨酸)- 用于构建刺激响应纳米载体的潜在生物医学材料 2024-09-18
- 青大胡浩、于冰/北化徐福建团队 Biomaterials:负载多聚脱氧核糖核苷酸纳米载体的近红外响应水凝胶用于增强慢性伤口愈合 2024-09-04
- Daniel Siegwart/董一洲/陶伟教授 Nature Reviews:基于纳米技术的mRNA疫苗 2023-09-08
