可注射生物材料通过微创手术实现损伤区域组织原位再生,具有创伤小、恢复快、操作方便、应用安全等优势,在医美领域也极具应用前景。细胞外基质(ECM)水凝胶和聚合物多孔微球可以通过微创注射用于组织修复。然而,ECM水凝胶降解快难以为组织生长提供空间,大多数聚合物微球生物惰性、易碎、可注射性能差,这限制了两类材料促再生效果和应用。

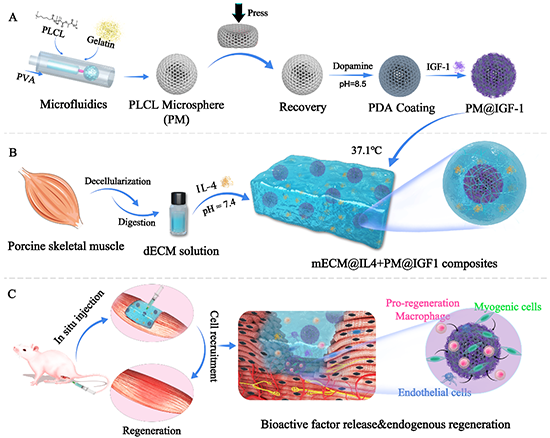
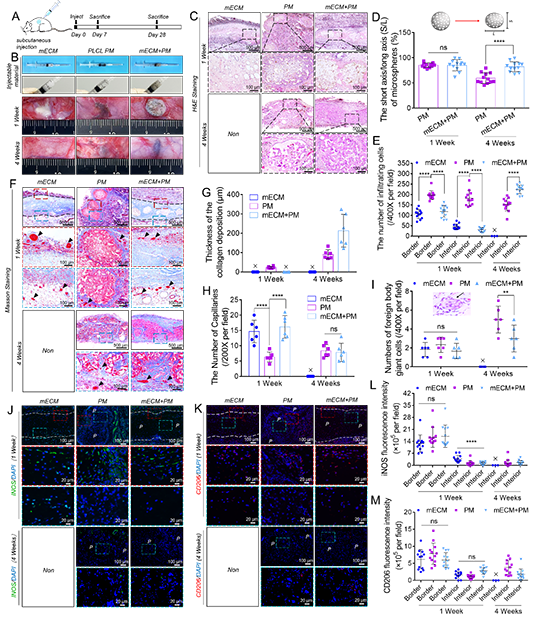
该改工作通过微流控、模板沥滤和去细胞化技术相结合构建了一种由弹性聚(l-丙交酯-co-ε-己内酯)(PLCL)多孔微球和肌肉细胞外基质(mECM)组成的复合材料,同时在不同材料分别装载活性因子白介素-4(IL-4)和胰岛素样生长因子-1(IGF-1),得到了可注射功能复合材料体系(图1)。与传统的聚乳酸-羟基乙酸共聚物(PLGA)、聚己内酯(PCL)多孔微球相比,弹性PLCL多孔微球在注射过程或压缩载荷下能够迅速恢复形变,显著减少微球坍塌(图2)。此外,该复合体系能够实现两种材料优势互补,ECM水凝胶提供生物相容性,聚合物微球提供必要的机械强度和多孔结构来引导组织再生。在大鼠皮下注射实验中,复合材料展现出了良好的可注射性和组织相容性,不引起机体免疫排斥反应(图3)。为了验证复合材料促再生性能,研究者将其注射到大鼠胫前肌大体积缺失模型中,负载双因子的功能复合材料体系(mECM@IL4+PM@IGF1)能够通过调控损伤区巨噬细胞和肌源性细胞行为,显著促进新生肌纤维形成、血管化和神经化(图4)。这项研究为可注射功能复合材料设计和构建提供了新策略和新思路,在外科微创治疗和组织修复材料领域具有良好转化前景。


原文链接:https://www.nature.com/articles/s41467-024-45764-4
- 港中大(深圳)唐本忠院士团队 ACS Nano:可注射NIR-II水凝胶实现荧光成像引导的肥胖局部精准治疗 2026-05-24
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 复旦大学俞麟教授 AFM:可注射的热疗水凝胶通过调节炎症和细胞外基质代谢来抑制椎间盘退变 2026-04-05
- 中国科大公泽/姜洪源教授团队《Commun. Phys.》:揭示了钙离子跨膜运输增强癌细胞伪足振荡生长 2025-08-28
- 华南理工大学边黎明教授团队Nature Chemistry:可模拟细胞外基质液液相分离介导的组装及生物物理特征的简约模型 2025-06-10
- 上科大郑宜君教授课题组 Nat. Commun.: 构建具有可见光响应的时空动态粘弹性水凝胶用于探究癌细胞与细胞外基质相互作用 2025-02-07
