NJIT许晓阳教授、上海交大章雪晴教授 AFM: 脂质体-聚合物杂化纳米结构基因递送平台用于可冷冻保存的DNA、mRNA新冠疫苗
2022-07-24 来源:高分子科技
新冠疫情导致全球性大流行病,对公共卫生和全球经济造成灾难性影响已感染超过 5 亿人,导致全球超过 610 万人死亡(根据世界卫生组织于 2022 年 4 月的数据)。通过各方不懈的研究与合作,新一代的核酸疫苗以创纪录的方式被研发出来并及时地部署接种, 其中包括由Pfizer-BioNTech和Moderna开发的两款mRNA脂质体纳米粒(mRNA-LNP)新冠疫苗。这两款mRNA-LNP疫苗能够引发高水平的中和抗体滴度并且有着高达 95%的疫苗有效性,在预防 COVID-19上显示出巨大潜力。尽管如此,这两款mRNA-LNP新冠疫苗受到有限保存期和缺乏稳定性的限制,需要将它们保存在 -60 °C 至 -80 °C,以及 -15 °C 至-25°C的环境中,并且同时需要高成本的超冷链的运输条件。目前,冷冻干燥技术已被应用于延长包括小分子药物、疫苗和基于蛋白质的药物在内的多种药剂的保质期。在冷冻保护剂的作用下,冷冻干燥能够溶剂对疫苗的水解作用并且能够使其以干粉形式下长期储存。由于目前的 mRNA-LNP 新冠疫苗全部都是储存在水相溶液中的,因此,这增加了 mRNA 和 LNP 水解的作用从而导致疫苗的不稳定而失效。

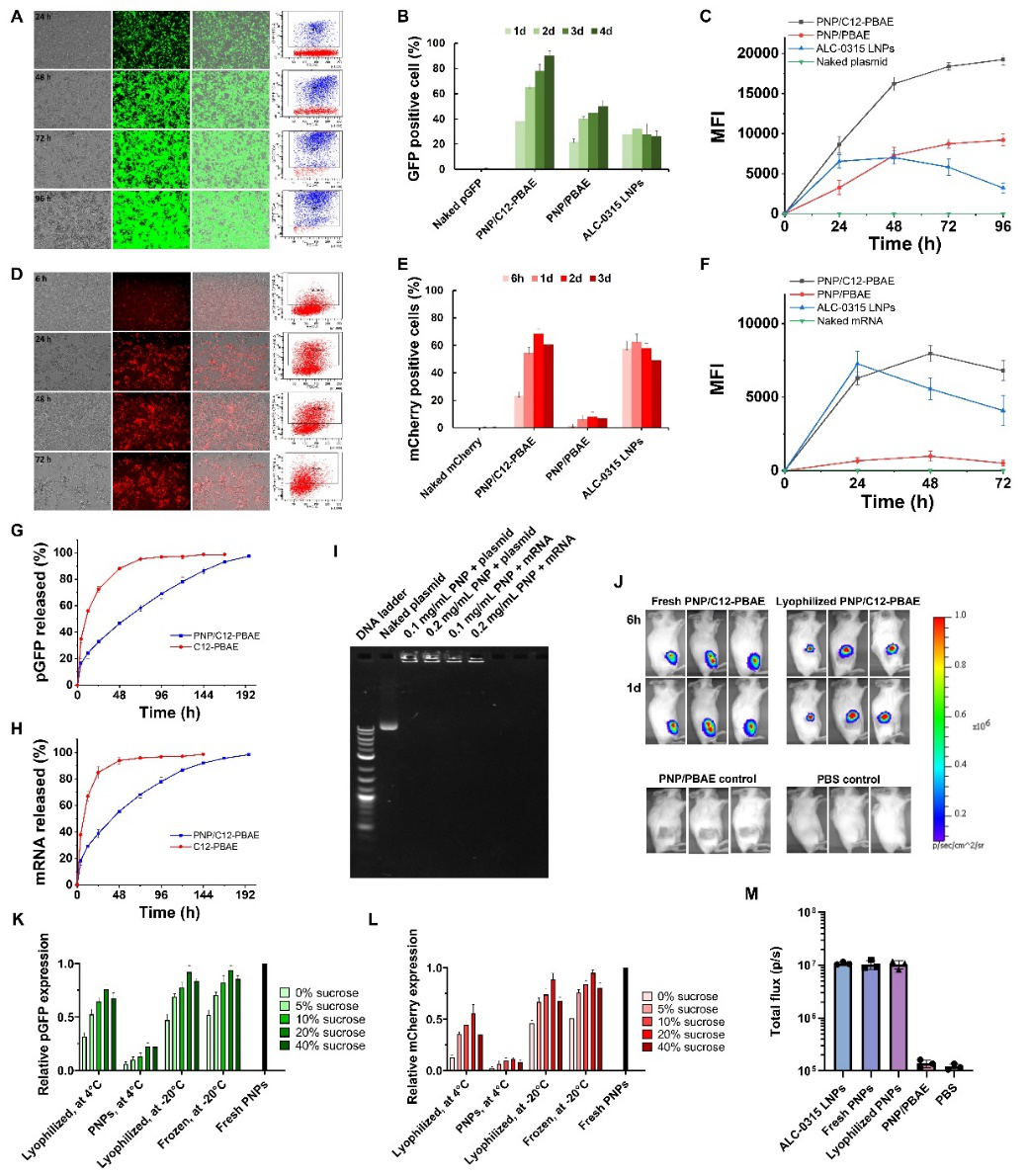
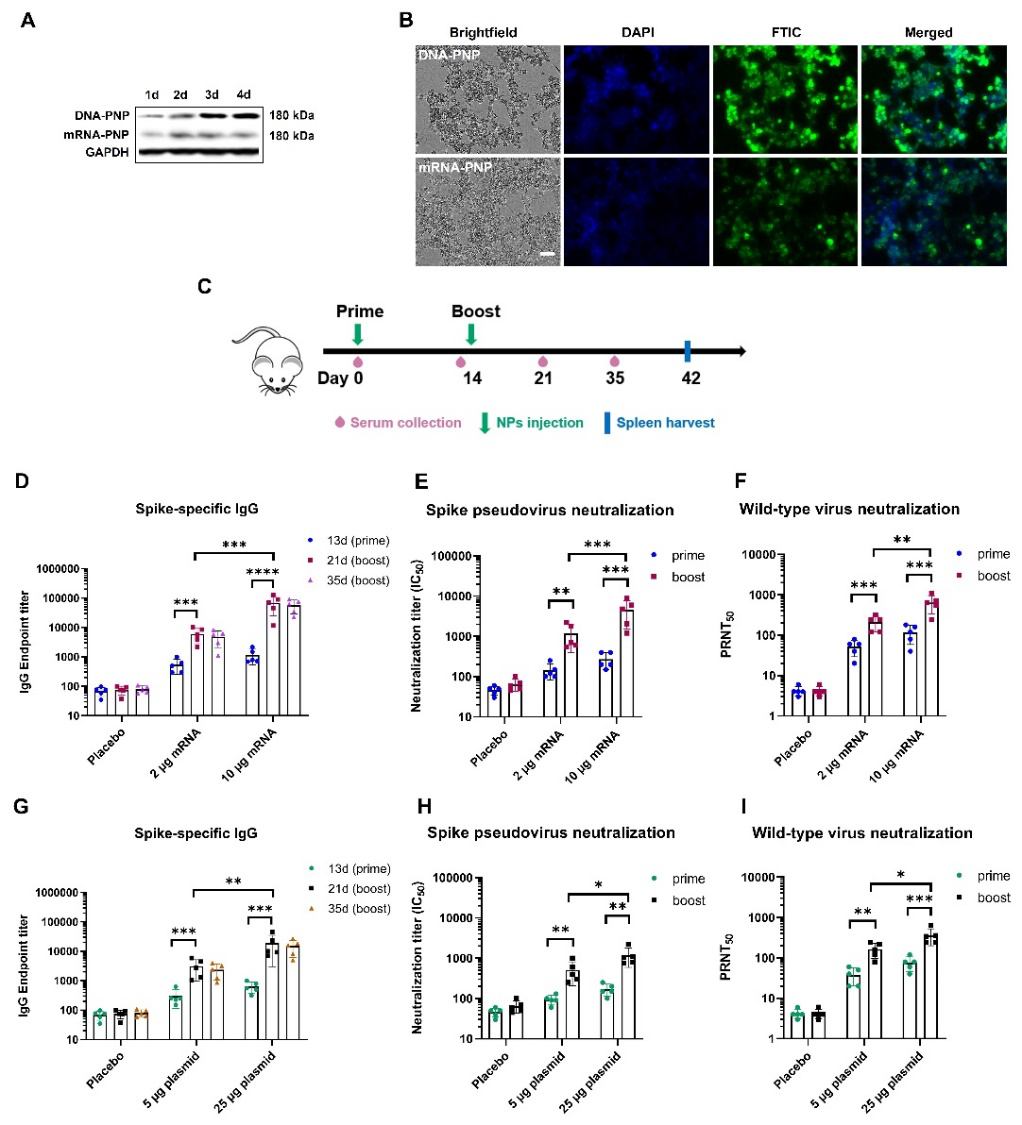
近期,美国新泽西理工学院许晓阳教授团队联合上海交通大学药学院章雪晴教授团队开发出一类新型脂质体修饰的聚(β-氨基酯)命名为L-PBAE,并进一步与PLGA-PEG自组装成“Particle-in-Particle”(PNP)新型PNP纳米结构用于DNA和mRNA的体外与体内的递送(图1)。在众多PNP 的纳米材料库中,研究人员证明了PNP/C12-PBAE作为性能最佳的纳米粒子,能够在体外和体内高效地递送DNA和mRNA,并且呈现出增强的转染效果、缓慢持续的DNA和mRNA的释放和至少 12 个月在-20 °C的条件下冻干保存而不会损失转染效率的出色稳定性(图2)。在包裹刺突蛋白编码的DNA和mRNA后,脂质体修饰的 PNP 新冠疫苗即使在 -20°C 冻干储存 12 个月后,仍能在小鼠模型中成功引发刺突蛋白的特异性抗体和 Th1 型的T 细胞免疫反应(图3)。这种新型脂质-聚合物杂化的 PNP 纳米粒子系统为递送DNA 和 mRNA提供了一种新的策略和方法,并且该递送系统具有长期冻干储存的能力。这项工作以“Lipid-polymer hybrid “Particle-in-Particle” nanostructure gene delivery platform explored for lyophilizable DNA and mRNA COVID-19 vaccines”为题发表在《Advanced Functional Materials》(IF=19.92)(DOI:10.1002/adfm.202204462)。该论文的第一作者为新泽西理工学院化工与材料系博士研究生李忠宇。

原文链接 https://onlinelibrary.wiley.com/doi/10.1002/adfm.202204462
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 西北大学范代娣教授、朱晨辉教授、李阳副教授 AM:基于仿生凝血级联途径的多肽修饰脂质体纳米颗粒可喷涂水凝胶治疗不可压破性创面出血 2025-04-19
- 天津大学史志远教授团队招聘科研助理 - 高分子化学、微凝胶/微囊泡/脂质体、酶包裹递送载体、微流控 2024-12-17
- 桂工甄士杰/李美静博士、广医张天富副教授、华工赵祖金教授、港中深唐本忠院士 AM:近红外二区脂质体多模态光诊疗新成果 2024-11-29
- 安徽理工大学王文新团队 JACS:基于多环聚(β-氨基酯)的基因递送系统 2023-07-31
- 超支化聚(β-氨基酯)用于CRISPR/Cas9基因编辑系统的递送及HPV感染相关宫颈癌的治疗 2020-03-22
- 天工大高辉教授团队 AHM:提升结直肠癌的抗血管生成基因疗法重塑炎症和免疫抑制性肿瘤微环境 2024-12-26
- 暨南大学戴箭课题组 Adv. Funct. Mater.:溶瘤病毒样纳米颗粒用于肿瘤特异性基因递送 2024-04-23
