表皮生物电子需要柔软、功能化的高分子材料,构建稳定、贴肤的界面,以实现无创、精准的生理信号监测,同时保证佩戴舒适度与日常活动不受影响。天然生物高分子如蛋白质、多糖等,因具备可持续性、生物相容性与可降解性,是极具潜力的生物电子界面材料。然而,将其加工成适用于表皮器件的高韧性、可拉伸、超薄膜材料,长期以来仍是领域内的重大挑战。
针对上述问题,苏州大学汪晓巧教授、西北工业大学杨海涛教授创新采用静电纺丝定向排布与吸湿驱动可控结晶协同策略,制备出超高韧性、可拉伸的超薄丝蛋白纤维膜(SPFM)。该复合策略重构了区别于天然蚕丝的多级结构,由单轴取向微纤维与稀疏β-片层纳米晶交联的随机纠缠肽链网络复合而成。这种多级结构不仅克服了天然蚕丝固有的脆性,还使材料在超薄形态下保持极高的力学性能。制备的丝蛋白纤维膜厚度仅约19 μm,断裂应变达220%,断裂强度9.88 MPa,韧性14.97 MJ m-3,断裂能高达98.18 kJ m-2,综合力学性能显著优于现有再生丝蛋白生物材料。同时,该膜具备良好的离子导电性、高透气透湿性与优异生物相容性,可紧密贴合皮肤,在动态运动中依然保持稳定界面。
作为贴肤、透气型传感器,丝蛋白纤维膜能够在各类日常动态条件下高保真地监测人体运动与生物电信号。基于该膜的双通道肌电记录信噪比超过 45 dB,结合机器学习算法,手势识别准确率达到98.91%,充分展现了高性能生物基表皮电子在人机交互领域的应用潜力。
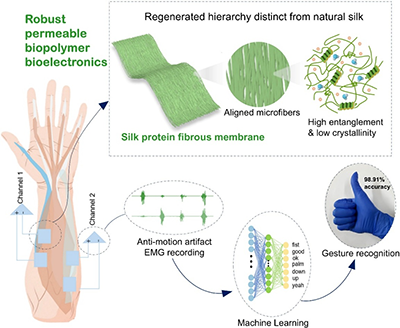
图1. 基于超薄高韧丝素蛋白纤维膜表皮电极的双通道肌电手势识别
2026年4月23日,相关成果以“Ultratough, Stretchable Silk Protein Fibrous Membranes for Robust and Permeable Epidermal Bioelectronic Sensors”为题, 发表于《Advanced Functional Materials》(DOI:10.1002/adfm.75582)。苏州大学硕士研究生潘锡华为论文第一作者,苏州大学汪晓巧教授和西北工业大学杨海涛教授为论文共同通讯作者。研究得到国家自然科学基金、江苏省自然科学基金等项目支持。
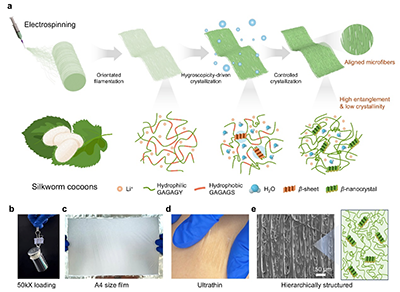
图2. SPFM的制备与宏观/微观结构
研究团队通过静电纺丝结合吸湿驱动结晶法制备丝素蛋白纤维膜。所制备的纤维膜膜厚度约19 μm,能承受自身重量五万倍的载荷而不损坏,并可制成A4尺寸。并且能紧密贴合人体皮肤,在压缩变形下仍保持共形接触。取向排列的微纤维以及由稀疏β-片层纳米晶交联的随机缠结肽网络,这种特殊的层次结构是材料优异力学性能的基础。
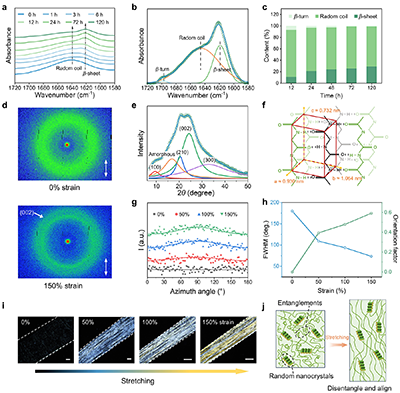
图3. SPFM的多尺度结构表征
傅里叶变换红外光谱显示,随着处理时间延长,丝素蛋白二级结构发生转变,处理72 h后β-片层含量达25.8%,无规卷曲占73.4%。广角X射线散射证实了β-片层纳米晶的形成。WAXS和偏振光显微镜表征共同证实拉伸过程中,分子链沿拉伸方向逐渐取向。示意图总结了内部结构演化:随机缠结肽链在拉伸下发生线圈-取向转变,实现能量耗散。
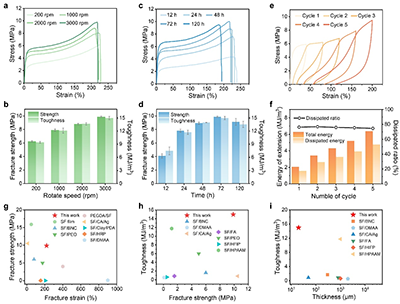
图4. SPFM的机械性能调控
通过优化静电纺丝滚筒收集转速、吸湿驱动结晶时间,获得了取向微纤维、稀疏β-片层纳米晶交联的随机纠缠肽链网络结构的超薄超韧丝素蛋白纤维膜。在高转速(3000 rpm)下收集的具有高度取向微纳纤维,相应的力学性能显著提升。高湿处理12~72 h,β-片层含量增加,强度上升,延展性略有下降,继续延长至120 h则性能退化。与已报道的再生丝蛋白材料相比,SPFM在强度、延展性、韧性及厚度方面均具有显著优势。
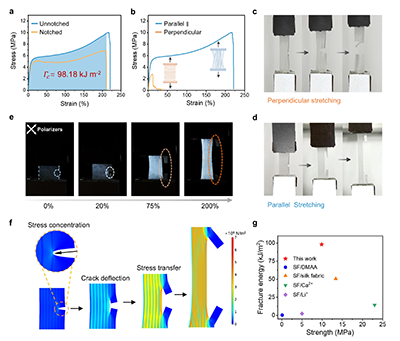
图5. SPFM的抗撕裂性能与裂纹抵抗机制
SPFM展现出优异的抗撕裂性能。在微纤维取向排列与肽链定向结构的协同作用下,材料在缺口处发生剪切变形,促使裂纹沿着拉伸方向发生偏转。偏振光观测与有限元模拟进一步表明,层级结构纤维膜能够通过纳米晶体与纠缠肽链的排列实现高效能量耗散,从而有效延缓裂纹扩展。得益于这一裂纹偏转与能量耗散的特殊机制,SPFM的断裂韧性高达98.18 kJ m-2,在所有报道的再生丝蛋白生物材料中处于最高水平。
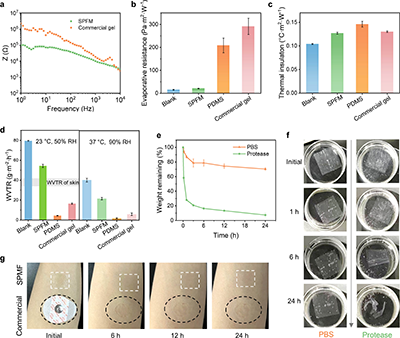
图6. SPFM与皮肤的界面特性
皮肤-电极阻抗测试显示,SPFM在1~104 Hz频率范围内阻抗低于商用凝胶电极。蒸发阻力仅20.5 Pa·m2/W,接近裸皮肤,显著低于凝胶电极和PDMS膜;热绝缘约为0.13 °C·m2/W。水蒸气透过率在23 °C和37 °C下均表现优异。体外降解实验表明,在蛋白酶溶液中能够有效降解。皮肤贴附24~72 h未引起红斑或水肿,证明其良好的生物相容性。
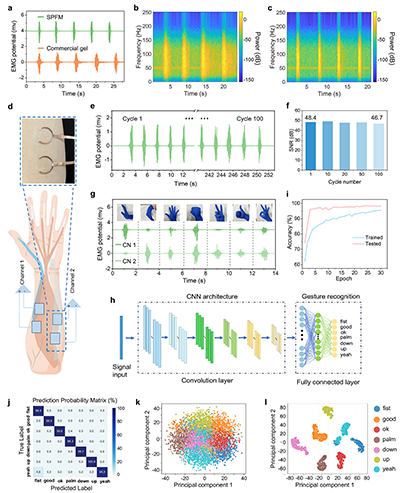
图7. 双通道SPFM电极用于高保真肌电信号记录与手势识别
最后将SPFM电极作为贴肤、透气型传感器用于监测人体生理电信号,包括ECG、EMG等,能够实现长程、高保真地采集电信号,信噪比>45dB。此外,双通道电极设计能区分不同手指动作产生的肌电信号模式,结合CNN算法能够实现对不同手势的识别,准确率高达98.91%,充分展现了高性能生物基表皮电子在人机交互领域的应用潜力。
综合来说,本研究证实,通过多级结构重构,丝蛋白可成为适配表皮电子的理想生物高分子膜材料。该研究在丝蛋白材料微加工和结构调控上实现科学创新,揭示了再生丝素蛋白纤维膜的多级结构与力学性能间的构效关系,实现了强韧、可拉伸、超薄综合特性,促进了高性能、可持续生物基生物电子发展,在柔性电子、生物医学工程、智能穿戴与人机交互领域具有广泛的研究价值与应用前景。
原文链接:https://doi.org/10.1002/adfm.75582
- 四川大学王玉忠团队 AFM:兼具高强度、韧性与回弹性的热塑性弹性体 2026-06-03
- 吉林大学孙俊奇教授、李懿轩副教授团队 AFM: 基于二茂铁构象转变构筑低滞后、高强度与高韧性无液体离子导体 2026-06-02
- 上海工程技术大学宋仕强团队 AM:应变诱导离子通道排列与温度激活离子门控实现超高电导增强-打造宽温域、高韧性全固态离子弹性体 2025-11-30
- 芝加哥大学王思泓教授团队 Nat. Electron.: 大规模可拉伸神经形态电路 - 用于体表边缘计算 2026-05-23
- 苏州大学张晓宏教授课题组招聘柔性电子器件方向博士后 2026-05-06
- 中科院长春应化所刘俊研究员团队 AFM:热塑性聚酯弹性体助力本征可拉伸有机光电探测器 2026-04-28
- 哈工大(深圳)何思斯团队 AM:高性能全聚合物水系准固态纤维电池 - 为透气可穿戴设备提供可靠能源 2026-06-05
