药物的有效负载是实现高效体内递送的关键前提。前期工作中,研究团队虽通过设计跨细胞转运型高分子材料,显著提升了传统纳米药物的体内递送效率,并成功推动了企业转让与临床转化(Nature Nanotechnology, 2019,周泉,申有青*),但在临床转化过程中,作者深刻认识到高分子纳米药物作为复杂制剂,在工业放大生产与批次化制备工艺中仍面临严峻挑战。基于此,过去几年里,研究团队一直在思考能否通过载体结构的理性设计,在提升载药能力的同时简化载药工艺,从而降低后续转化风险并提高临床成功率。基于此,受DMSO(二甲基亚砜)“万能溶剂”启发,并结合团队在含亚砜聚合物(周泉*等,Adv mater 2024, J Control Release 2024, Biomaterials 2026)及凝聚化高分子(周泉* Macromolecules,2024, 2025)的工作积淀,作者构建了一类基于亚砜聚合物的凝聚体内核胶束(Polymeric coacervate core micelles, PCCMs)。相较于传统高分子递药载体,PCCMs 展现出卓越的载药容量、极简的载药工艺以及高效的体内递送性能(图1),为高分子递药载体的设计提供了新的思路。
2026年5月8日,相关工作以Bridging hydrogen-bond-stabilized polymeric coacervate core micelles for high-efficiency drug encapsulation and delivery为题发表于Nature communications, 浙江大医学院王佳峰、应佳佳以及上海交通大学黄建湘博士为该论文的共同第一作者,浙江大学周泉研究员、申有青院士、刘祥瑞教授、周天华教授为论文通讯作者。本研究受到国家自然科学基金委(52173141, 52473151,82102192,52503206)和中央高校基本科研业务费专项基金(2022E50008和2024ZY01056 )等多项基金资助,研究过程中得到了西湖大学张鑫教授和朱龙琛博士的大力支持和帮助。
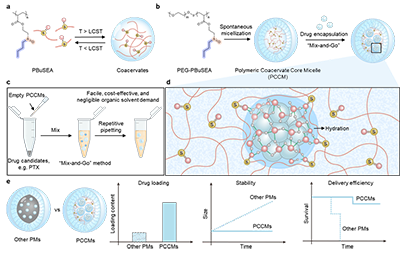
图1. PCCMs胶束的设计及相较传统聚合物胶束的潜在优势。
1、高载药能力及高稳定性
为了验证PCCMs的高载药能力以及其载药性能的通用性,作者随机选择了40 种不同结构的疏水性药物分子,系统评估了PCCMs的载药性能。结果显示:约45%的测试药物载药量(Loading contents)超过40%,80% 的药物LCs超过30%,且所有测试药物的LCs均高于20%。在与商业化载体(如PEG-PDLLA、PEG-PLGA和PEG-PCL)的对比实验中,PCCMs 的载药效率在所有测试药物中均表现出显著优势(图2)。进一步以紫杉醇(PTX)为模型药物进行验证,发现PCCMs相较于现有商业化载体PEG-PDLLA 稳定性能显著提升。即便经历反复冻融或长期储存,PCCMs仍能保持优异的载药稳定性。机制研究表明,这种高稳定性源于载体中亚砜基团、水分子与药物分子之间构建的“桥接氢键网络”,该网络有效避免了药物分子的长程聚集,将药物聚集体稳定在纳米尺度,从而实现了高载药量和高稳定性的平衡。

图2. PCCMs相较传统聚合物载体具有显著提高的载药性能。
2、Mix-and-Go极简化载药过程
在传统载药过程中,研究者们往往需要采用纳米共沉淀、薄膜法、或微流控等方法将药物载入载药体系中。这些过程需要用到大量有机溶剂,并依赖透析、超滤等操作将引入的有机溶剂去除。因此载药周期长、能耗高,放大生产过程中存在较大技术壁垒。鉴于PCCMs的高载药能力以及强载体-药物分子相互作用,作者进一步尝试通过简单的Mix-and-Go方法将药物包载进入PCCMs中(图3),尽管相较传统载药方法,其载药量会有部分下降,但其操作极为简便,仅需物理混合与涡旋震荡即可实现高效包载(图3)。这一策略大幅减少了有机溶剂的使用,显著缩短了制备周期,不仅简化了工艺流程,更从源头上实现了载药过程的绿色化。
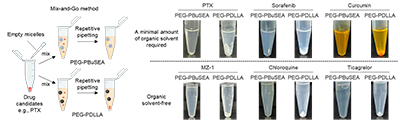
图3.药物分子通过简单的Mix-and-Go方法被载入PCCMs中
3、高体内递送效率
鉴于PCCMs兼具卓越的载药能力与胶束稳定性,作者首先以紫杉醇(PTX)为模型药物,系统评估了其体内递送效能。在恶性程度极高的三阴性乳腺癌动物模型中,PCCMs展现出显著优于商业化紫杉醇聚合物胶束(Genexol-PM)的体内递送效率,不仅大幅延长了实验动物的生存期,且在组织分布分析中证实,PCCMs/PTX在肿瘤部位的药物富集量显著高于Genexol-PM(图4a-d)。
PCCMs的另一优势在于其高载药能力可显著提升药物的最大给药剂量。对于部分安全性良好但需高剂量给药方能发挥疗效的候选药物分子而言,传统载体往往受限于载药量而无法达到有效治疗浓度。而PCCMs高载药量的特点,能显著提高药物的最大给药剂量,为这类高剂量依赖型药物的临床转化创造了新的可能性(图4e-g)。
此外,临床肿瘤治疗常需采用多药联合策略,但传统胶束受限于较低的载药能力,难以实现多种药物的同步高效包载,往往导致各组分药物无法同时达到有效治疗窗。相比之下,PCCMs凭借卓越的载药容量,能够同时实现多种药物的高效负载,不仅确保了联合用药中各组分的有效剂量,更显著提升了协同治疗的整体疗效(图4h-k)。
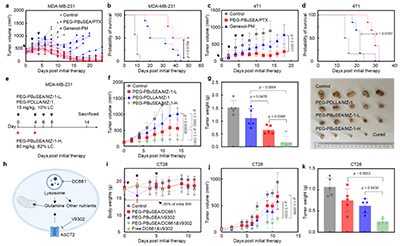
图4. PCCMs高体内递送效率
文章链接如下:https://www.nature.com/articles/s41467-026-72978-5
