炎症性肠病(Inflammatory Bowel Disease,IBD)的口服治疗长期面临靶向性差、生物利用度低、全身毒性显著等关键问题。现有的免疫调节药物如6-巯基嘌呤(6-Mercaptopurine,6-MP)易被酶解、有效成分转化效率低,高剂量给药还会引发肝毒性、骨髓抑制等不良反应,而传统口服递送系统存在胃酸环境中不稳定、药物提前泄漏等缺陷,难以实现炎症部位的精准控释,同时单一的药物递送策略无法破解炎症性肠病中氧化应激、菌群失调与免疫紊乱的恶性循环,治疗效果受限。
针对上述问题,吉林大学杨英威教授、中国医科大学李鹤然教授、吉林大学口腔医院姜欢副教授团队设计合成了一种新型酸稳定的侧链偶氮苯功能化的金属有机框架材料(Azo-MOF),并通过主客体相互作用将 β-环糊精(β-CD)与偶氮苯侧链结合,构建了无后修饰的超分子门控快开型递送纳米系统CAMM(β-CD封端负载6-MP的Azo-MOF )(如图1a所示)。该材料以Zn2+为金属中心,偶氮苯侧链均匀分布于MOF孔道,19.3 ?×19.3 ?的孔道结构实现6-巯基嘌呤高效负载,耐酸型Azo-MOF结合β-CD封端后使递送系统在胃肠道转运过程中药物泄漏率低于5.0%。体外实验证实,CAMM具备缺氧/pH双响应释药特性,在结肠炎部位的缺氧环境中,偶氮还原酶切断偶氮键触发药物快速突释,碱性微环境则诱导MOF骨架降解实现药物持续释放,炎症部位累计释药率超90.0%;同时Azo-MOF凭借共轭π体系与金属配位环境的协同作用,对?OH、?O2-、DPPH?的清除率分别达到96.0%、69.0%、95.0%,可有效清除活性氧;此外,CAMM在炎症结肠黏液中渗透深度提升26.4%,黏膜黏附率维持87.0%以上,且在0-800 μg mL-1浓度范围内溶血率低于5.0%,细胞存活率超80.0%,展现出优异的黏液穿透性、黏膜黏附性和生物相容性。
相关研究成果近期以Construction of a MOF-Based Snap-Top Delivery Nanosystem for Powerful Dual-Responsive Synergistic Colitis Treatment为题发表在Advance Science (DOI: 10.1002/advs.202524174)。该研究第一作者为吉林大学23级博士研究生李鑫,吉林大学杨英威教授、中国医科大学李鹤然教授、吉林大学口腔医院姜欢副教授为共同通讯作者,吉林大学中日联谊医院王鑫副教授、马连君教授参与了该项研究。该工作得到国家自然科学基金、辽宁省青年科学基金、青年教师科研创新能力支持项目、吉林省自然科学基金、中央高校基本科研专项资金的资助。
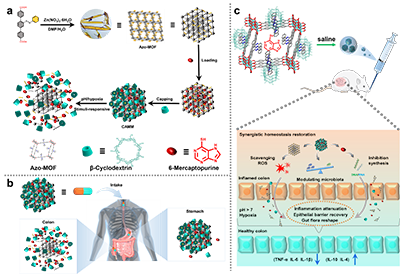
图1. CAMM递送系统的设计、构建及治疗机制:a)Azo-MOF的合成,以及负载6-MP、经β-CD封端的双响应超分子门控递送系统的构建(偶氮苯单元为柄,通过主客体作用结合β-CD阀门);b)递送系统经胃肠道转运后,在病灶处的靶向释药示意图;c)CAMM对葡聚糖硫酸钠诱导的小鼠结肠炎的治疗作用机制。
在葡聚糖硫酸钠诱导的急性结肠炎小鼠模型中,CAMM展现出显著的体内协同治疗效果(如图1c所示)。最优剂量的1-CAMM组实现小鼠体重近完全恢复,疾病活动指数显著降低,结肠长度恢复至5.9 cm,接近正常小鼠水平;能有效下调TNF-α、IL-1β等促炎细胞因子的表达,上调IL-4、IL-10等抗炎细胞因子水平,抑制中性粒细胞浸润并促进巨噬细胞从促炎M1型向抗炎M2型极化;同时可修复肠上皮屏障,恢复紧密连接蛋白ZO-1、claudin的正常表达,减少肠上皮细胞凋亡。此外,16SrRNA基因测序结果显示,CAMM能有效调节肠道菌群结构,富集乳杆菌属、双歧杆菌属等有益菌,抑制肠球菌属等致病菌,降低变形菌门相对丰度,恢复肠道菌群的α和β多样性,实现肠道微生态稳态的重建,其治疗效果显著优于6-MP单药治疗。
该研究首次将超分子门控快开型递送系统应用于炎症性肠病治疗,突破了传统口服递送系统局限,实现药物的靶向递送,同时将MOF载体从被动递送工具转化为兼具抗氧化活性的主动治疗剂,整合了靶向释药、抗氧化治疗与菌群调节三大协同机制,为炎症性肠病的精准治疗提供了全新策略,也为其他胃肠道炎症疾病的口服递送系统设计提供了重要参考。
原文链接:https://doi.org/10.1002/advs.202524174
- 哈工大邵路教授团队 JACS:聚合物编织金属有机框架玻璃膜家族用于超强耐压碳捕集 2026-01-07
- 吉大杨英威教授、秦建春教授团队 JCR:金属有机框架双功能纳米系统用于缓解酸铝胁迫并调节植物生长 2024-11-19
- 英属哥伦比亚大学 Zachary Hudson教授等 JACS:导向网状化学合成介孔ZIFs 2024-11-02
- 浙大黄品同教授/周珠贤教授、南大顾宁院士团队 Adv. Mater.:胞吞转运级联超声空化高效靶向治疗深部细菌生物膜感染 2024-10-30
- 天津工业大学高辉教授课题组 CEJ:具有抗核粒梭杆菌活性的超分子递送系统的构建及其对耐药结直肠癌的靶向治疗 2022-06-20
- 四川大学万乾炳教授和高会乐教授课题组 Small:构建pH响应可聚集银纳米粒用于靶向治疗细菌感染性疾病 2022-05-08
- 暨大刘明贤教授团队 Nano Today: 含有多酚@埃洛石的海藻酸盐微球用于益生菌递送和炎症性肠病治疗 2025-02-19
