近日,海南大学吴锡龙教授团队在Advanced Functional Materials上发表了题为“Photo/Sono/Magneto-Responsive Ternary Heteronanocrystals with S-Scheme Heterojunction for Penetrative and ROS-Amplified Tumor Ablation”的研究论文,研究围绕活性氧(ROS)介导肿瘤消融面临的缺氧抑制和深部递送不足两大挑战,设计构建了一种光/声/磁响应三元异质纳米晶平台(BPF)。该平台创新性融合S型异质结与Fe基纳米酶催化机制,并结合磁场和超声协同驱动,实现了肿瘤深部递送、ROS持续放大和多模态成像引导,为实体瘤精准治疗提供了新的研究方案。研究团队作者单位包括海南大学生物医学工程学院、数字医学工程全国重点实验室,海南大学药学院等相关平台。吴锡龙教授为本文唯一通讯作者,邱硕(硕士研究生)、吴云娣(高级实验师)和刘若灿博士为共同第一作者。该项工作得到了国家自然科学基金、海南省南海育才南海创新人才计划教育领域项目、海南省重点研发项目、海南省自然科学基金创新研究团队项目等支持。
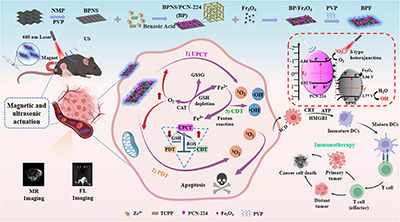
图1 光/声/磁响应三元异质纳米平台BPF的构建及其用于黑色素瘤诊疗示意图
该BPF平台以超薄黑磷纳米片(BPNS)作为压电还原组分,金属有机框架PCN-224作为光敏氧化组分,二者形成S型异质结(S-scheme heterojunction);超顺磁性Fe3O4纳米粒子锚定于异质结表面,赋予体系过氧化物酶(POD)和过氧化氢酶(CAT)样活性。研究团队系统表征了BPF的结构、光电化学性质、压电性能和S型异质结的电荷转移机制,并在体外细胞模型、三维多细胞肿瘤球以及多种小鼠黑色素瘤模型(原位瘤、远端瘤、复发模型和肺转移模型)中全面评估了其治疗效果和免疫激活能力。
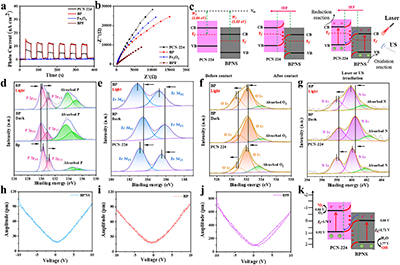
图2 BPF的电性能与电荷转移机制
在光电流响应测试中,BPF经660 nm激光和超声联合激发后,S型异质结的内建电场有效促进光/声激发载流子的定向迁移,抑制电子-空穴复合,显著增强单线态氧和羟基自由基的产生。超声照射10分钟后,BPF的单线态氧生成效率约为BP的1.5倍、PCN-224的3倍。Fe3O4组分在酸性条件下通过Fenton反应催化H2O2生成羟基自由基,同时其CAT样活性分解H2O2产生O2以缓解乏氧,并有效消耗GSH削弱肿瘤的抗氧化防御。
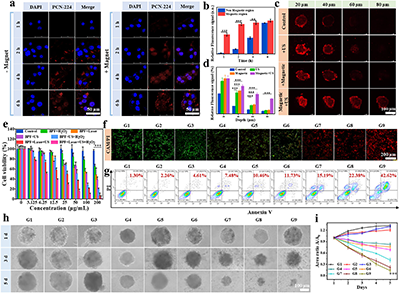
图3 声磁驱动BPF增强肿瘤渗透及杀伤作用的效应
在三维肿瘤球模型中,超声与磁场联合驱动下BPF的穿透深度和荧光强度远超单一驱动或无驱动组,并且磁场引导可显著增强B16F10细胞对BPF的摄取。在过氧化氢存在下,BPF与超声波和激光治疗结合具有显著的肿瘤杀伤效果,且能够抑制肿瘤球的生长。
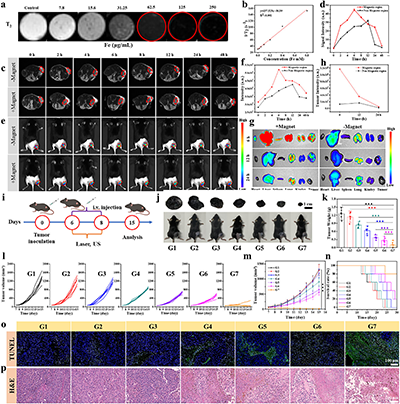
图4 BPF的体内成像与抗肿瘤效果评估
在体内抗肿瘤实验中,BPF联合磁场引导、激光和超声的全模式治疗组表现出最显著的肿瘤抑制效果,小鼠存活率最高,组织学分析显示该组肿瘤细胞大面积凋亡坏死。BPF还表现出MRI T2加权成像(r2 = 157.53 mM-1·s-1)和近红外荧光成像的双模态实时引导能力。进一步的小鼠黑色素瘤模型系列实验显示,全模式治疗组中CRT暴露和HMGB1释放水平最高,成熟树突状细胞比例、CD8+细胞毒性T细胞和CD4+辅助T细胞浸润均显著升高,IFN-γ、TNF-α和IL-6等促炎细胞因子水平上调,抑制性IL-10下调。在肿瘤复发和再挑战模型中,全模式治疗组的复发肿瘤生长被显著抑制,外周血效应记忆T细胞比例最高,表明形成了持久的免疫记忆。在肺转移模型中,该组肺部转移结节数量最少,肺组织结构接近正常。
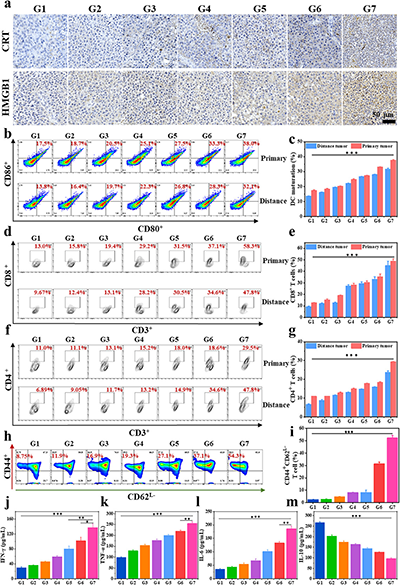
图5 BPF介导的体内免疫激活效果
这项研究的亮点在于将“S型异质结增强电荷分离-Fe3O4纳米酶放大ROS反应-磁/声协同促进深部递送-荧光/MRI双模成像引导”有机整合为一个一体化诊疗平台,不仅实现了超声压电催化(UPCT)、光动力治疗(PDT)和化学动力学治疗(CDT)的协同增效,也把局部肿瘤杀伤与全身抗肿瘤免疫激活连接起来。这项工作不仅提供一个高效ROS治疗方案,也是一条从深部递送、微环境调控到免疫记忆建立的连续治疗新路径,为实体瘤精准消融、复发预防和转移抑制提供了新的研究思路和应用启发。
原文链接:https://doi.org/10.1002/adfm.75094
通讯作者简介:
吴锡龙,海南大学生物医学工程学院教授、研究员,博士生导师,博士后合作导师。入选海南省第四批“南海育才项目南海创新人才”,海南省高层次拔尖人才,海南大学C类高层次引进人才、微纳米智能生物诊疗团队PI。博士毕业于中国科学院长春应用化学研究所,师从陈学思院士,曾在中山大学从事博士后研究工作,主要研究领域包括微纳米诊疗技术、智能个人防护装备、类器官与环境健康等。以通讯作者/第一作者在Advanced Functional Materials、Advanced Science、Biomaterials、Small等期刊上发表论文30余篇,获得国家授权发明专利17项,承担多项国家自然科学基金面上项目、青年项目与地区项目、海南省重点研发项目、海南省南海育才项目和海南省自然科学基金创新研究团队项目等。中国生物医学工程学会类器官和器官芯片分会委员、海南省免疫学会分子免疫与转化医学专业委员会副主任委员、广东省精准医学应用学会类器官和器官芯片分会常务委员、海南自由贸易港知识产权法院技术调查官,同时担任国家卫生健康委科技创新2030-“癌症、心脑血管、呼吸和代谢性疾病防治研究”重大项目评审专家、国家重点研发计划政府间国际科技创新合作重点专项评审专家、国家自然科学基金委面地青项目评审专家等。Research、Progress in Biochemistry and Biophysics(PIBB)、Exploration、BMEMat等学术期刊青年编委。获得全国大学生生物医学工程创新设计竞赛一等奖(五项)指导教师、第十一届“挑战杯”海南省大学生课外学术科技作品竞赛自然科学类特等奖指导教师、"海南省优秀研究生导师"等荣誉。
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 中科大王育才/蒋为团队 Nat. Biomed. Eng.: 利用一氧化氮(NO)突破肿瘤血管基底膜屏障,增强纳米药物瘤内递送 2025-05-03
- 天工大高辉/余云健团队 Nano Today:选择性抗菌脂质递送丁酸梭菌增强具核梭杆菌相关肠道疾病治疗 2025-04-10
- 青农大孔晓颖、康复大学师进生/周祺惠 AFM:激活的免疫系统通过抑制肿瘤相关成纤维细胞左右光疗的体内抗肿瘤效果 2024-02-20
- 河北工大邢成芬课题组《Nano Lett.》:基于近红外光响应共轭聚合物纳米粒子的免疫激活抗真菌策略 2022-12-27
