人体器官芯片是一种可模拟人体器官功能及组织微环境的体外模型。它能够缩短药物研发时间和成本、提升新药研发效率,是生物医学领域引领未来新药发现和精准诊疗范式的变革性前沿技术。为了模拟器官芯片系统中的生理微环境,需要生理相关参数来精确评估药物代谢。氧气含量是维持细胞或组织功能并调节其行为的关键参数。细胞和组织功能极易受微环境氧含量的影响。目前的器官芯片平台除了常规缺氧培养箱中的生理氧合或环境氧浓度外,还补充了标准培养基,其氧含量约为21%,高于几乎所有生理所需的氧含量。并且,每个组织中的生理氧气水平各不相同,范围从 0.5% 到 13%。而这些传统方法都无法同时为不同微组织提供生理所需且具有差异性氧含量的微环境。
基于此,哈佛医学院Y. Shrike Zhang教授团队开发了一个闭环模块化多器官芯片系统。该系统不仅可以实时监测流动培养基的氧含量,而且能够独立且同时将单一微组织器官芯片中的氧含量严格控制在 4-20% 的范围内。此外,基于该系统进行药物研究表明,氧含量会分别影响并联的肝脏芯片、肾脏芯片和血管芯片的药物代谢。该研究预计可以显著拓宽多器官芯片在疾病建模和药物筛选中的应用。该工作以“A Closed-Loop Modular Multi-Organ-on-Chips Platform for Self-Sustaining and Tightly Controlled Oxygenation”为题,发表在 Proceedings of the National Academy of Sciences (PNAS)上。该论文的第一作者是Nan Jiang(姜楠,现四川大学教授)、Guoliang Ying (应国量,现四川大学副研究员)、Yixia Yin(殷义霞)、Jie Guo(郭洁),哈佛医学院Y. Shrike Zhang教授是通讯作者。
研究背景及意义
体外维持人体组织和器官的代谢活动和功能行为对于药物研究至关重要。传统的2D或3D细胞培养能够保存细胞体外活性。然而与动态细胞培养不同,静态细胞培养通常无法持续供应新鲜培养基,并且难以准确再现体内微环境的生理条件。器官芯片技术实现了体外模拟人体生理或疾病的 3D 器官结构和功能。它能够结合微流控技术实现多个3D 微尺度器官相互作用及药物筛选的研究。因此,器官芯片系统已被广泛采用作为一类强大的药物开发和治疗筛选体外模型。
氧含量对器官或组织生理和代谢至关重要,因为它是维持细胞基本功能所必备条件之一。众所周知,典型的体外细胞培养是在 21% 的氧气含量条件下进行的,而细胞在体内经历的氧气水平几乎远低于 21% 或 160 mmHg。事实上,持续暴露于高氧含量的微环境会影响细胞或组织的代谢。缺氧条件对微组织代谢、生理途径和组织重塑也有重大影响,可能会抑制或阻止体外组织细胞的增殖和生长,并且不足以维持呼吸速率,细胞可能会从糖酵解中获取更多能量。因此,在体外实现与体内微环境相关的氧含量控制非常重要。
人体内生理氧含量因器官而异,例如动脉血中 10-13%,脑中 0.5-7%,软骨中 1%,肝脏中 10-13%,肾脏中 4-6% 等。因此,在多器官芯片系统中为不同器官创造不同氧含量的微环境应当考虑这一关键问题。此外,由于脂质过氧化反应和活性氧攻击酶和核酸,氧气调控对于组织/器官的药物代谢至关重要。所以,在体外微组织药物毒性中也应考虑氧气控制。为了实现器官芯片中不同氧含量的控制,传统方法是将器官芯片在低氧培养箱中进行培养。尽管这种方法能够使器官芯片稳定维持在任意氧含量的环境中,但是由于使用的标准培养基中的氧含量无法实现自动控制,所以该方法受限于芯片中需要进行多个组织和器官的培养。
在微流控芯片中直接降低氧气含量是近年来器官芯片研究的一个热点方向。然而,同时将降低和升高氧气含量的装置结合起来,以自我维持的方式精确控制器官芯片微环境中的氧含量的报道较少。另外,目前大多数降氧和升氧装置用于半开放或开放式的细胞培养,而没有通过循环流动模拟体内微环境。并且,常用的器官芯片平台基于聚二甲基硅氧烷材料,这也增加了外部氧气扩散的难度。因此,有必要在封闭的微循环系统中开发一个控制氧气的(多)器官芯片平台,以重现组织和器官微环境和相关药物研究。
研究思路和设计
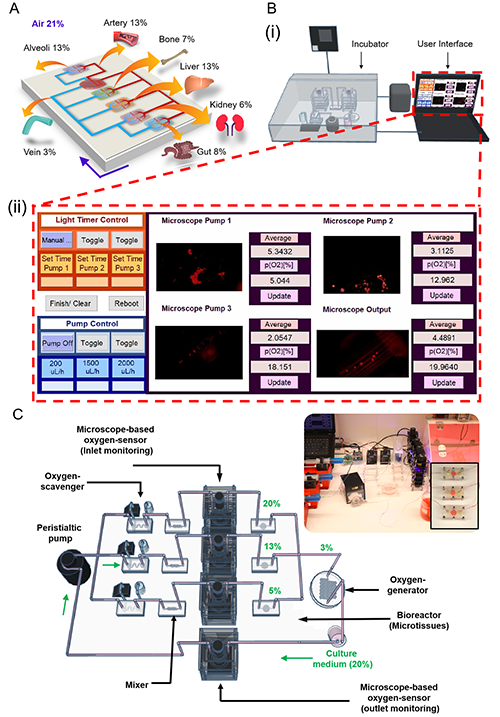
图1.自动化闭环多器官芯片平台的构建及其用于氧控制和实时监测的研究。
研究结果和分析
该工作分别研究了每个模块化微流控芯片的设计和性能,进一步测试和分析了自动控制系统。通过连续监测实时系统中不同部位的氧含量,并动态调整以适应每个模块化微流控芯片的需求。该工作分别对并联的肝脏、肾脏和血管微组织在不同氧气水平下进行的药物反应进行独立评估。
模块化氧实时监测芯片的构建和性能研究
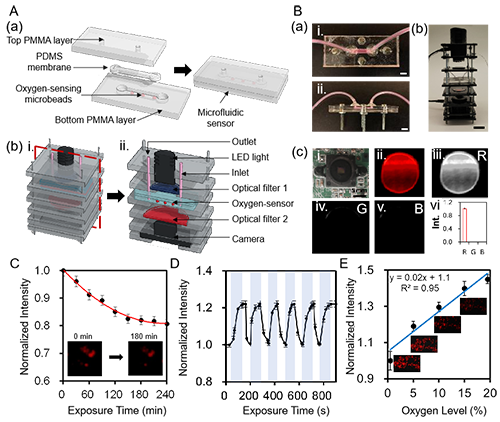
图2. 微型显微光学氧传感器的构建及氧实时监测性能的研究。
模块化降氧芯片和混合芯片的研究
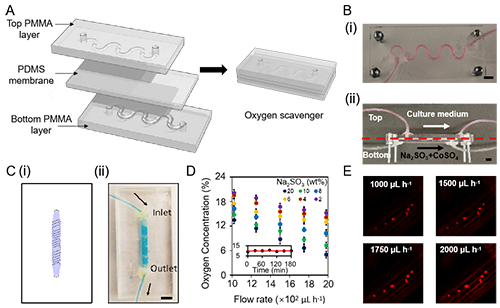
图3. 降氧芯片和混合芯片模块的构建和性能研究。
动态升氧芯片的研究

图4. 升氧芯片和混合芯片的构建和性能研究。
微组织器官芯片的构建
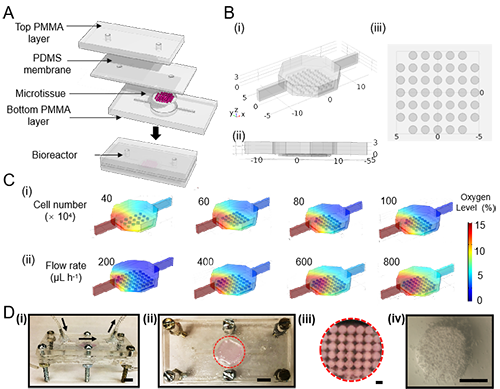
图 5. 概念验证单个微组织芯片平台的设计。
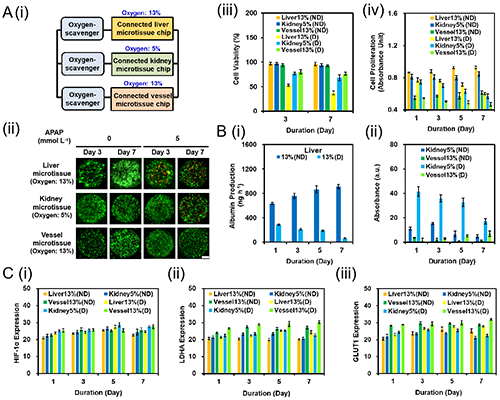
图6. 在他们的闭环多器官芯片平台中评估氧气对药物毒性的影响。
综上所述,本研究开发了一种自动化闭环多器官芯片系统。该系统采用热塑性微流控芯片的模块化设计,以确保密闭循环的微环境,从而独立控制和监测溶解氧含量。所有氧气控制和监测均以实时和自动控制的方式进行,允许在多器官芯片中对药物引起的组织或器官反应进行自我维持研究。研究结果表明,该系统能够在循环流动的培养基中独立提供更符合体内生理环境的氧含量,从而可以研究生理微环境中药物筛选研究。
文章信息:
Jiang N, Ying G, Yin Y, Guo J, Lozada J, Valdivia Padilla A, Gómez A, Gomes de Melo BA, Lugo Mestre F, Gansevoort M, Palumbo M, Calá N, Garciamendez-Mijares CE, Kim G-A, Takayama S, Gerhard-Herman MD,Zhang YS*. A Closed-Loop Modular Multi-Organ-on-Chips Platform for Self-Sustaining and Tightly Controlled Oxygenation. Proceedings of the National Academy of Sciences USA, 2024, in press.
https://www.pnas.org/doi/10.1073/pnas.2413684121
- 四川大学王玉忠团队 AFM:兼具高强度、韧性与回弹性的热塑性弹性体 2026-06-03
- 浙江大学凌君教授课题组 Macromolecules:无金属催化剂催化两仪聚合构筑聚氨基酸热塑性弹性体 2026-05-03
- 大连理工大学韩丽、舍布鲁克大学赵越 JMCA(HOT Paper):无交联策略制备热塑性液晶弹性体驱动器 2026-04-30
- 中南大学蒋炳炎、吴旺青教授 CEJ:突破微流控芯片模内键合技术 2024-12-19
- 东华大学史向阳教授团队 Nano Today:微流控合成肿瘤微环境调控型超小氧化铁纳米团簇用于动态MR成像导引的肿瘤联合治疗 2022-09-17
- 北航常凌乾教授等《Biosens. Bioelectron.》:手指驱动式微流控芯片用于结核病的快速多重诊断 2021-09-27
- 武汉理工戴红莲教授团队Chem. Mater.:具有可调凝胶pH值和碱性pH响应性的硼氮内配位硼酸酯水凝胶的模块化设计及凝胶机理 2023-03-09
