
化石能源的快速消耗造成了温室效应、大气污染、水污染等严重的环境问题。生物质资源作为唯一的可持续碳源,可以通过绿色化工工艺,减少对不可再生资源的依赖。生物质单糖广泛存在于生物体内,主要用于食品、化工等行业。同时,以单糖为原料可以通过催化转化制备多种高值化学品。在这些高价值化学品中,乳酸是一种多用途精细化学品,可广泛应用于食品、制药、皮革、纺织、环保和农业等领域。此外,乳酸可以作为可生物降解聚合物(聚乳酸,PLA)的前驱体,在医疗保健和消费品市场上有7亿美元的市场。目前,乳酸主要通过高温高压化学合成或繁琐的生物发酵。在温和的条件下,通过单糖的光化学转化来获得高产量的乳酸仍然是一个关键的挑战,因此需要合理设计合适的光催化剂。
纳米纤维素(CNF)是一种以纤维素为原料高强机械力作用下被解离成单个的纳米纤丝。纳米纤维素具有较高的长径比,同时CNF表面存在丰富的亲水官能团(羟基、羧基等),有望成为制备一维光催化材料的理想模板剂。石墨氮化碳(g-C3N4)是一类由含氮前驱体热聚合制备的聚合物半导体类光催化剂,具有-1.4 V的导带(CB)和1.3 V的价带(VB),适用于大多数光催化生物精炼。然而,原始g-C3N4的可见光吸收范围有限,光激发载流子重组速度快,比表面积小,活性不理想。g-C3N4的形貌控制是提高光催化性能的关键因素,一维纳米结构g-C3N4材料具有沿长轴的矢量电子和声子输运通道以及高表面体积比等优点。以CNF为软模板,有望得到纳米结构g-C3N4材料。同时,CNF分子链上的羟基、羧基在热解过程中能与氮化碳前驱体发生缩合反应,在氮化碳分子结构中引入缺陷和掺杂,进而调控氮化碳的电子结构。通过CNF辅助制备氮化碳,可同时调控氮化碳的形貌和电子结构,优化反应中间体的吸附强度,从而获得更高的光催化催化活性。

CNF衍生氮化碳基光催化剂(HCN)的制备流程如图1所示,主要包括双氰胺与CNF官能团(羟基和羧基基团)之间的氢键作用以及后续的热聚合和H2O2分子剪切过程。在上述光催化剂制备中,CNF同时起到了软模版和掺杂剂的作用。氮空位和氧元素掺杂成功的引入到氮化碳分子骨架中,同时通过改变CNF的用量可以调控氮空位的浓度。在H2O2的分子剪切作用下,催化剂(HCN)转化为一维纳米棒,同时纳米棒内部填充纳米片状框架结构。这种一维的纳米棒状结构极大的提升了HCN的比表面积(由0.411 cm3 g-1提高到116.84 m2 g-1),这增大了催化剂与反应底物的接触面积,同时充分暴露了催化剂的活性位点。
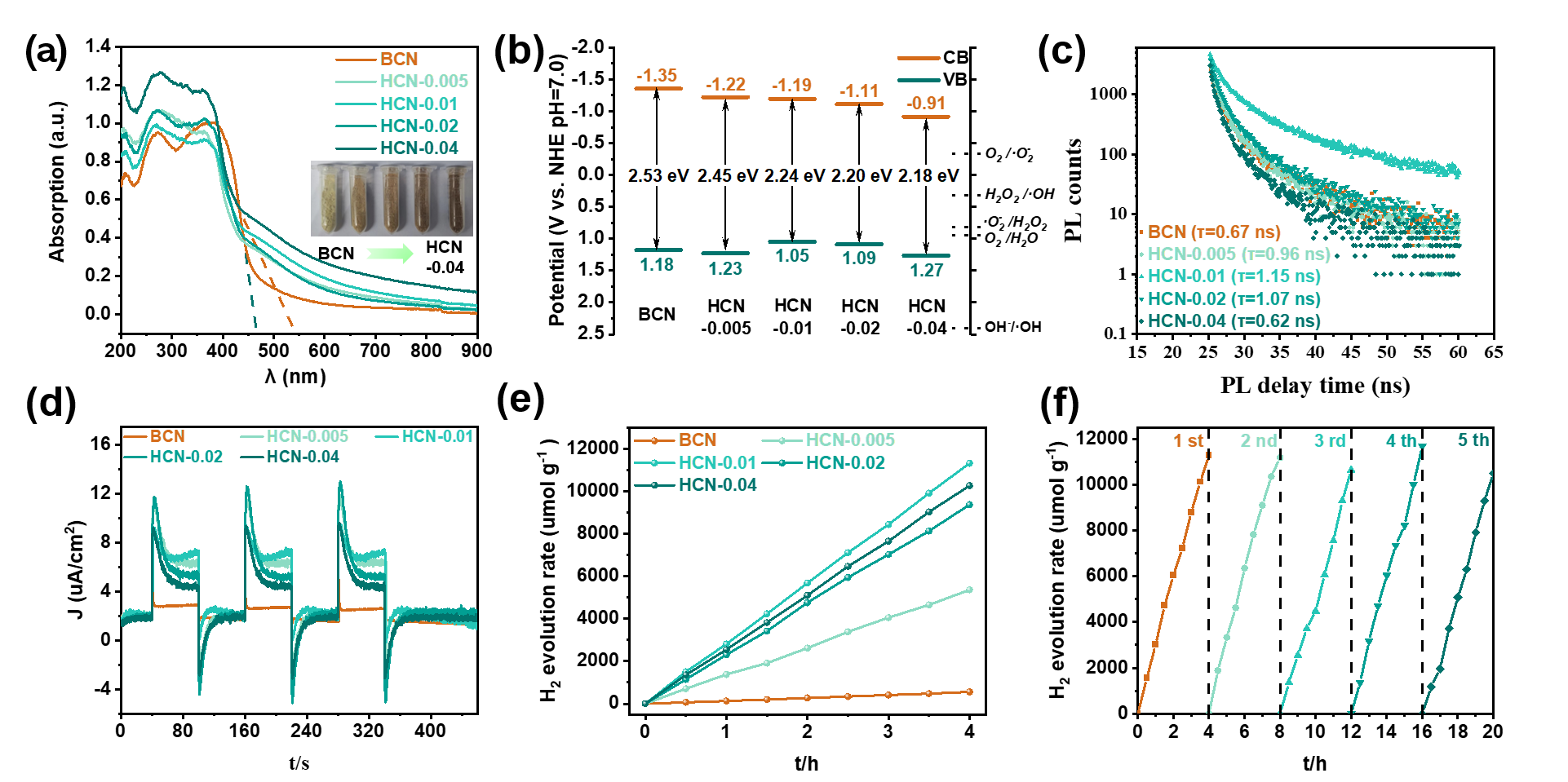
图3 HCN的光/电性能和光催化产氢性能
在g-C3N4分子骨架中引入氮空位和氧掺杂明显改变了样品的光学性质和可见光捕光能力。如图3a所示,HCN催化剂比BCN具有更强的可见光吸收能力,由于氮空位和氧掺杂剂的引入,HCN催化剂表现出显著的吸收红移。根据Kubelka-Munk函数的计算结果,BCN和HCN的带隙从2.53 eV逐渐窄到2.18 eV。瞬态荧光的结果也表明HCN(1.15 nS)的荧光寿命比BCN(0.67 nS)长(图3c),这表明光致电子/空穴的复合减少。通过电化学阻抗响应(EIS)和瞬态光电流响应研究了BCN和HCN的光电电化学性能。由于HCN的导电性较高,其Nyquist图中的半圆直径比BCN小得多,从而降低了光电子传递电阻。与BCN相比,在HCN-0.01中观察到快速且可重复的光电流响应(图3d),表明具有较强的电子转移能力和光生载流子分离能力。
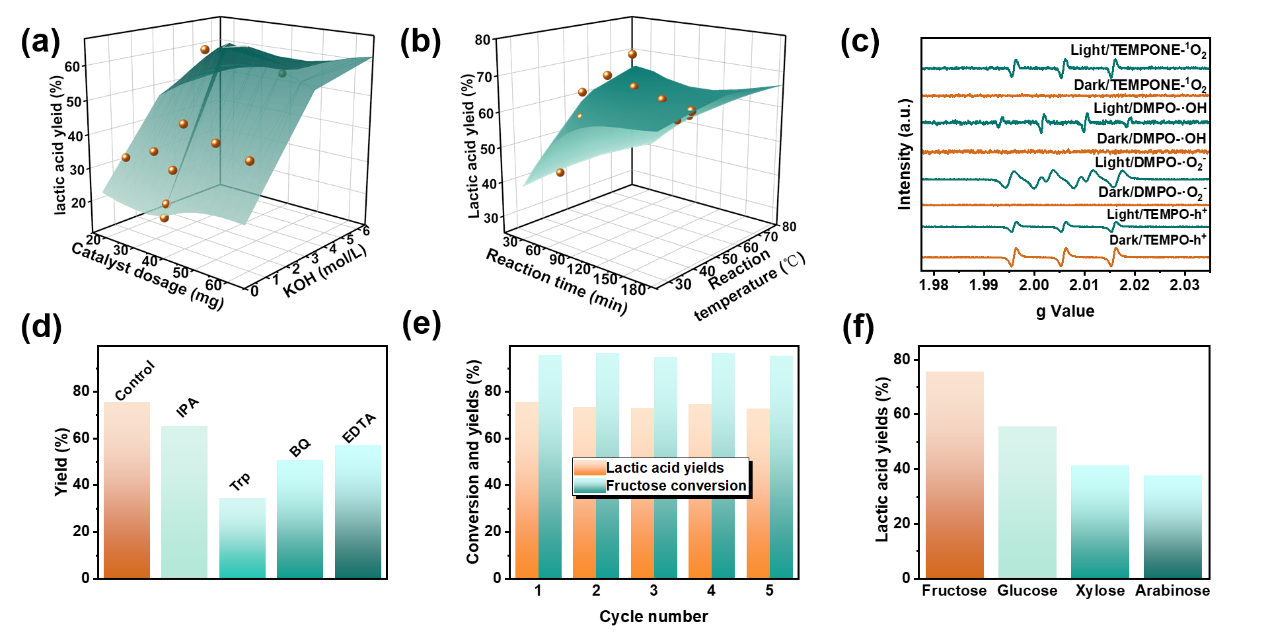
图4 HCN的光催化氧化生物质单糖生成乳酸性能

图5 基于HCN的DFT计算
通过第一性原理密度泛函理论(DFT)计算,进一步证明了氮空位和氧掺杂与能带结构之间的关系。如图5a-c所示,HCN-2的带隙比BCN和BCN-O的带隙小,并且有一个下移价带底。HCN-2的这种变化是氧掺杂和氮空位的结果。图5d给出了不同底物在HCN-2表面的吸附能,其中(果糖,Eads = -0.721 eV; O2,-1.868 eV和OH-, -1.178 eV),这表明HCN的结构易于吸附底物进行后续的光催化转化。基于上述研究,图5e提出了一个合理的反应机理。在中性(pH = 7)条件下,HCN在可见光的激发下产生电子和空穴。然后氧分子被附近的电子激活,通过单电子氧还原过程产生大量·O2-阴离子自由基(O2/·O2-= -0.33 V vs. NHE)。这一过程是可行的,因为HCN的CB电位(-1.35 ~ -0.91 V vs. NHE,图3b)比单电子氧化还原电位更负。由于HCN的VB边电位(+1.27 ~ +1.05 V vs. NHE)小于H2O/·OH-的氧化还原电位(+2.40 V vs. NHE),因此在HCN上h+很难直接氧化OH-或H2O生成·OH自由基。但HCN的CB电位足够正,足以使水氧化转化O2(+0.94 V vs. NHE)。·O2-阴离子自由基也可获得另一个e-生成中间产物H2O2(·O2-/H2O2= 0.94 V vs. NHE)。H2O2随后通过单电子过程还原为·OH自由基 (H2O2/·OH= 0.32 V vs. NHE)。此外,·O2-阴离子自由基也可与h+结合生成1O2。碱性条件下,pH增大CB位置更负,更有有利于·O2-的生成。通过比较HCN和BCN的能带结构排列,他们得出结论,氧掺杂和氮空位是直接和间接产生活性物质的必要条件。在h+、·O2-、·OH和1O2的作用下,果糖快速氧化成乳酸、乙酸和甲酸,选择性主要是由·O2-决定的。
该工作以“Nanocellulose-Assisted Molecularly Engineering of Nitrogen Deficient Graphitic Carbon Nitride for Selective Biomass Photo-oxidation”为题发表在《Advanced Functional Materials》上。文章第一作者是华南理工大学博士生邹刃和香港中文大学(深圳)陈仲欣博士,通讯作者为浙江大学陆俊教授和华南理工大学彭新文教授。
文章链接:https://doi.org/10.1002/adfm.202301311
- 天津大学苏荣欣教授团队 AFM:液相调控赋能高性能纳米纤维素凝胶设计 2026-01-14
- 华工方志强/川大王静禹/广工邱学青《ACS Nano》:折纸龙结构启发的高韧性、高延展性纳米纤维素薄膜 2025-08-31
- 华东师范大学张强课题组《Sci. Adv.》:基于纳米纤维素制备高强度、高柔韧性的全降解生物质泡沫材料 2025-08-08
- 天津大学李立强-陈小松课题组《Nat. Commun.》:大自然的精巧设计 - 有机半导体内的痕量氧掺杂 2024-01-27
- 北化杨卫民/李好义团队《Compos. Part A》:电纺纱线绿色高效短流程制备技术取得新进展 2025-05-15
- 陕西科技大学“生物质化学与材料”院士创新团队赵伟教授课题组:聚氨酯/木质素智能复合材料的绿色高效制备 2021-07-05
- 中国矿大何新建/徐欢团队 ACS Nano:火场应急防护用多尺度取向耐高温聚乳酸活性纳纤膜 2025-12-24
