抗生素的不规范使用导致耐药菌株的涌现。因此,研发非抗生素抗菌疗法迫在眉睫。生物活性气体,如氧气(O2)、一氧化氮(NO)及一氧化碳(CO)等已被开发用于抗菌治疗。NO与CO能够在一定浓度下直接杀菌,而O2则可通过形成单线态氧(1O2)实现杀菌。然而,气体治疗在时空上的不可控性严重制约了其杀菌效果,同时对正常细胞造成损伤。
“按需”杀菌策略成为解决上述问题的有效途径。现有的“按需”抗菌策略主要基于细菌感染微环境的氧化还原状态、pH、温度、酶等进行设计。然而,这些细菌感染微环境的特殊状态不能很好的关联细菌感染的程度,不能用于精确调控气体释放及后续抗菌效果。细菌分泌的细菌穿孔毒素(Pore-forming toxins, PFTs)在细菌感染的进程中扮演重要角色,是细菌入侵宿主的主要“武器”之一,且PFTs浓度与细菌感染进程呈较好的正相关。因此,利用细菌分泌的PFTs调控气体释放从而调控光治疗效果成为新的智能抗菌策略。

基于此,温州医科大学附属第二医院陈一杰研究员、谢聪颖教授联合温州医科大学药学院赵应征教授、陈梦纯博士合作构建了一种细菌PFTs毒素响应型仿生纳米气泡(RBC(IR780)-PFC)。该纳米气泡由红细胞膜包裹近红外光敏剂IR780和气体载体全氟化碳(PFC),并在使用前充入足量氧气(RBC(IR780)-PFC(O2))。结果显示,该纳米气泡能够吸附多种致病菌(包括耐甲氧西林金黄色葡萄球菌MRSA、李斯特菌LM、乙型溶血性链球菌GAS)分泌的PFTs。吸附PFTs能够在纳米气泡表面打孔,促进内部O2和IR780释放,并在近红外NIR光照下产生活性氧族(ROS),发挥光动力杀菌效果。这是一种独特的“按需”杀菌策略,即在同一剂量纳米气泡作用下,感染越严重、毒素累积越多、释放O2和IR780也越高,在NIR光照作用下产生的ROS也越多,抗菌效果也越好。有意思的是,研究团队构建的载体也可溶解NO形成RBC(IR780)-PFC(NO),同样能利用PFTs调节NO的直接杀菌效果。本研究将细菌毒素中和与调控光动力治疗有机结合起来,将我们通常认为细菌感染过程中的“有害事件”消除的同时将其转化成抗菌效果的“有益事件”,具有良好的临床抗菌治疗前景。
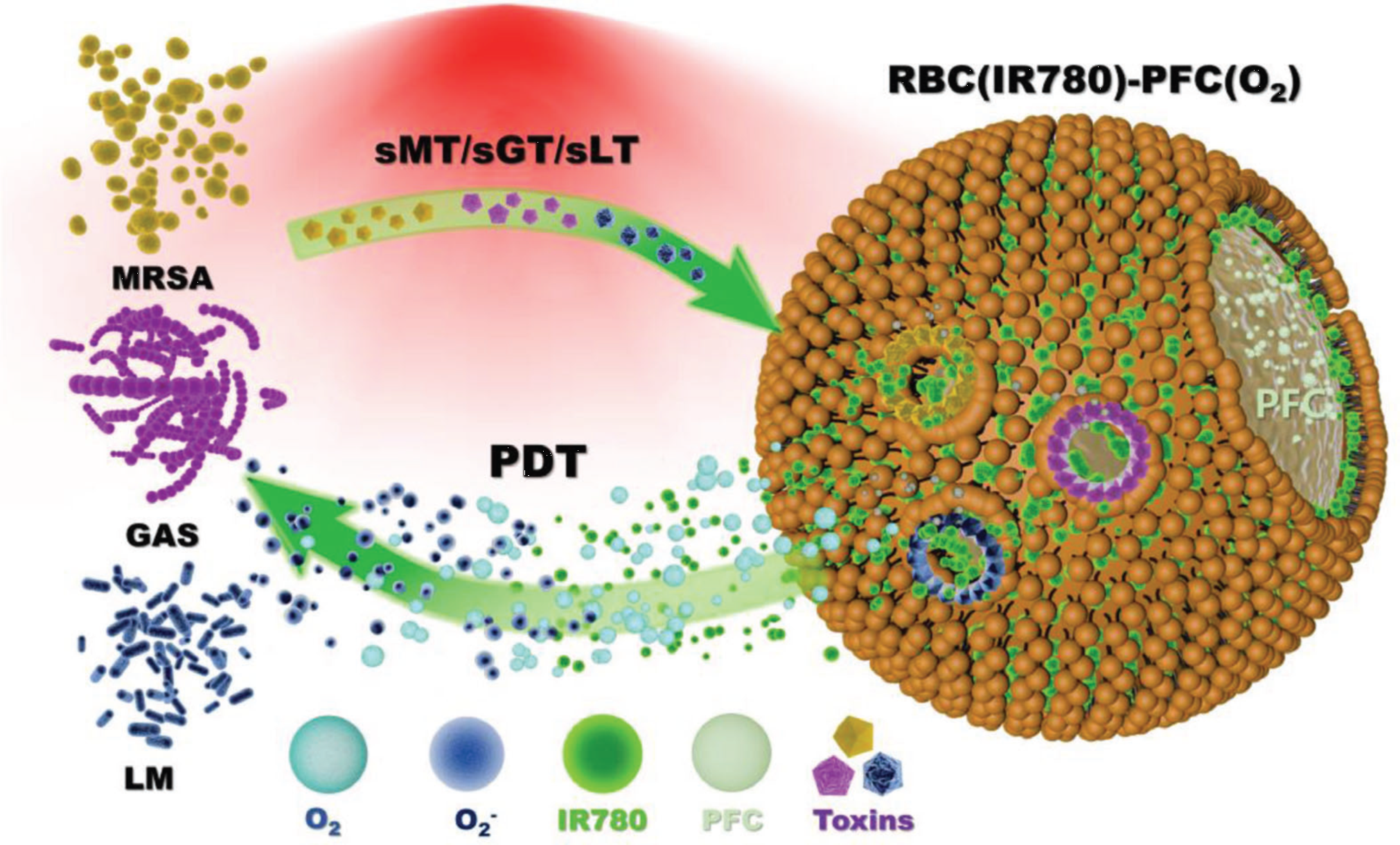
图1. 仿生纳米泡用于按需光动力治疗细菌感染

图2. RBC(IR780)-PFC的制备与表征

图3. 细菌毒素作用下RBC(IR780)-PFC(O2) 增强抗菌光动力治疗

图4. PFTs 促进NO从RBC(IR780)-PFC(NO)中释放并增强杀菌效果
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adhm.202200698
