三阴性乳腺癌(Triple negative breast cancer, TNBC)是雌激素受体、孕激素受体和人表皮生长因子受体检测均为阴性的乳腺癌。由于这些生物学特性,TNBC 对靶向这些受体的治疗性抗体无响应,临床治疗选择有限。化疗是TNBC 最常用的治疗手段。尽管化疗策略可以有效的去除肿瘤内已分化的肿瘤细胞,但是无法有效杀伤具有多重耐药机制的肿瘤干细胞(CSCs),反而导致残余肿瘤组织内肿瘤干细胞富集,成为肿瘤复发和转移的起点。
2021年4月1日,Advanced Materials在线发表了上海交通大学公共卫生学院宋海云研究员、化学化工学院樊春海院士和上海师范大学化学与材料科学学院陈楠研究员等人合作完成的题为 Epigenetic Remodeling Hydrogel Patches for Multidrug Resistant Triple Negative Breast Cancer的论文。该研究利用原位形成的肿瘤微环境响应型表观遗传重塑水凝胶贴发展了针对耐药性三阴性乳腺癌的联合疗法,通过诱导肿瘤干细胞分化和免疫激活,克服该肿瘤模型对多种化疗药物的耐药性,抑制肿瘤生长、术后复发和转移。

研究人员在三阴性乳腺癌小鼠模型中,通过高剂量、持续性地注射化疗药物5-氟尿嘧啶(5-FU),构建了耐药性三阴性乳腺癌模型。与正常肿瘤模型相比,这种类型的肿瘤中所含肿瘤干细胞的比例显著升高,由1-2%上升至15-20%。富含肿瘤干细胞的耐药性三阴性乳腺癌模型不仅对5-FU治疗失去响应,对其他多种化疗药物(例如表柔比星、紫杉醇和吉西他滨)也产生强烈的交叉耐药性。
研究团队在细胞和活体水平验证了该表观遗传学疗法一方面能够诱导乳腺癌干细胞分化,恢复肿瘤的化疗敏感性;另一方面激活肿瘤天然免疫,并进一步诱导T细胞免疫反应(图1)。因此,将表观遗传学调控和化疗药物联用,能有效抑制肿瘤生长、术后复发和转移。

图1表观遗传学疗法诱导肿瘤干细胞分化和免疫激活。
研究人员还发现这种肿瘤微环境响应型水凝胶贴介导的集表观遗传调控、天然免疫激活和化疗于一体的联合疗法不仅恢复了耐药性三阴性乳腺癌对5-FU的治疗响应性,还显著增强了该类型肿瘤对表柔比星、紫杉醇和吉西他滨等化疗药物的敏感性,说明这种治疗策略具有光谱的适用前景(图2)。
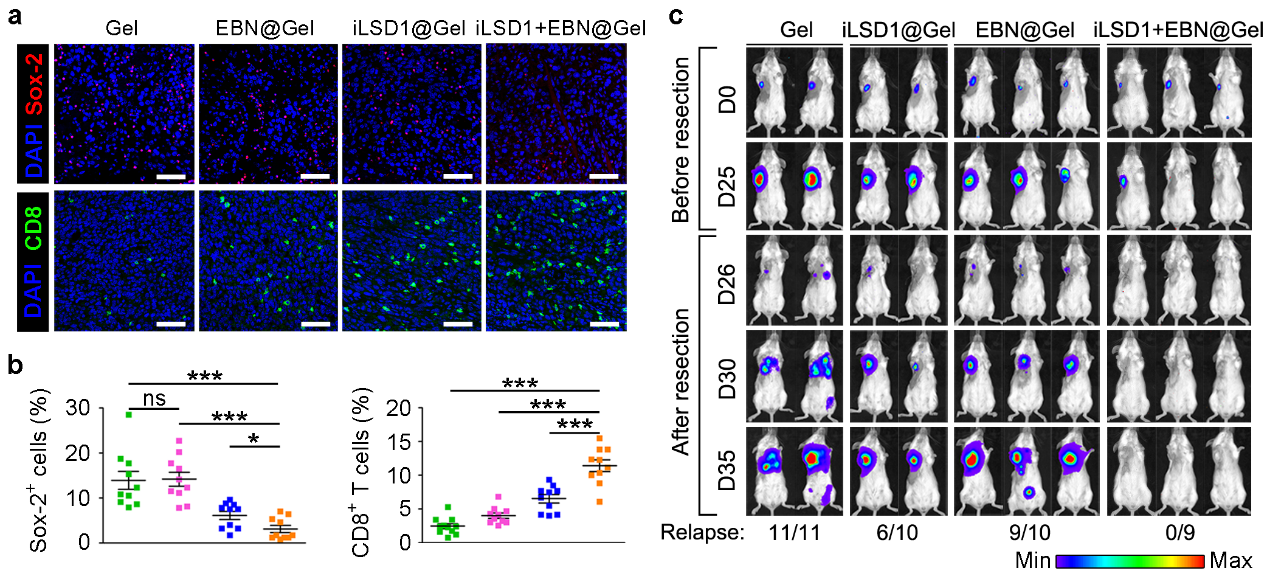
图2 肿瘤微环境响应型水凝胶贴克服三阴性乳腺癌的交叉耐药性。
助理研究员季晓媛和博士研究生郭道霞为该论文的并列第一作者,宋海云研究员、樊春海院士和陈楠研究员为该论文的共同通讯作者。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202100949
- 新医大一附院盛伟斌教授/华科大马良教授 AFM:构建了仿生多功能水凝胶贴片-在脊髓损伤治疗方面取得新进展 2026-03-02
- 四川大学王云兵/张婕妤团队 Adv. Mater.:可注射导电水凝胶贴片通过时空调控实现心肌修复 2025-10-27
- 湖北大学张玉红、陈朝霞/武汉工程大学江学良 AHM:具有三明治结构热致变色、抗菌、导电水凝胶贴片用于可视化感染性慢性伤口 2025-09-29
- 中山大学吴进等 AFM:基于坚韧可降解皮革水凝胶的自供电、超灵敏柔性H2S气体传感器 2026-06-05
- 中国石油大学(华东)张丽媛/青岛科技大学程浩然 Nat. Commun.:在耐盐水凝胶领域获重要进展 2026-06-04
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
