免疫疗法在癌症的治疗中展现出了极大的潜力,但是即使在抗原负荷较高的肿瘤中,抗原提呈的低效率也极大地限制了免疫治疗的响应率,导致了一系列的肿瘤免疫逃逸和缺陷。其中一个主要原因就在于大多数癌症的发生会下调一些抗原提呈相关蛋白的表达,从而抑制抗原提呈的进行。
针对抗原提呈过程的不足,武汉大学化学与分子科学学院张先正教授课题组报道了一种可以捕获癌细胞内蛋白质,促进抗原呈递的三肽Asp-Phe-Tyr(DFY)。该三肽由可被氧化的酪氨酸,易于自组装的苯丙氨酸和亲水性的天冬氨酸构成。DFY能被恶性黑色素瘤细胞内的酪氨酸酶特异性催化聚合,而聚合中间产物的醌式结构可以和癌细胞内蛋白上的巯基发生迈克尔加成的交联反应。这一系列的多肽聚合和蛋白质交联反应,最终生成了携带抗原蛋白的微米纤维pDFY。这种不溶性微米纤维不仅能够捕获癌细胞内蛋白质,还可以通过尺寸依赖的机制将蛋白质递送至抗原呈递细胞 (APC),进而双管齐下激活免疫系统杀死癌细胞(图1)。
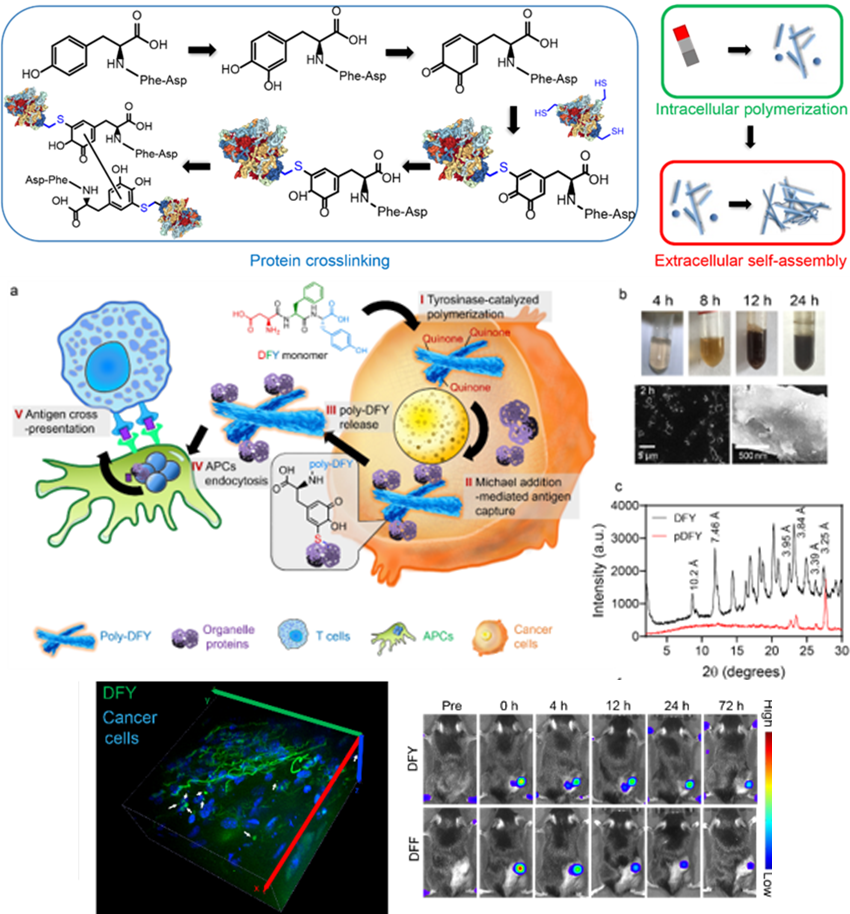
图1:基于DFY三肽的酶催化聚合反应及抗原呈递策略
该工作首先通过研究证明,在酪氨酸酶高度表达的恶性黑色素瘤细胞和小鼠模型中,DFY可以通过聚合反应来交联肿瘤蛋白,实现肿瘤部位的特异性聚集和保留。而DFY在发生聚合反应后,大分子的聚合产物pDFY被证实更倾向于被APC内吞,且内吞效果远比小分子的DFY要好。这说明APC可以通过尺寸依赖机制来摄取pDFY,从而成功刺激了APC的成熟并活化后续的免疫。而将DFY用于恶黑小鼠的治疗时,DFY与免疫检查点抑制剂aPD1的联合使用能够导致免疫细胞的进一步活化,显著地抑制了肿瘤生长(图2)。由于药物注射不可避免地会带来侵入性,该工作最后将DFY载入透皮凝胶用于可切除恶黑小鼠的治疗。体外、体内结果都证明该三肽透皮凝胶(DFY@gel)具有良好的生物相容性,并且透皮传递到肿瘤部位的DFY也能够成功激活免疫来延缓复发瘤的生长(图3)。

图2:pDFY的免疫激活能力以及DFY对不可切除恶黑小鼠的免疫治疗
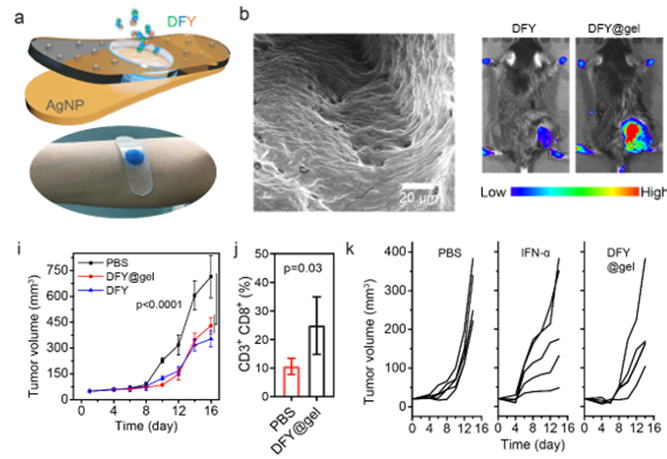
图3:DFY透皮凝胶对可切除恶黑小鼠的免疫治疗
该体系不仅在抗原呈递缺陷的恶黑小鼠体内抑制了肿瘤的生长,在透皮治疗中,DFY三肽也表现出免疫系统的高效活化和很好的生物相容性。这项工作为多功能合成生物学材料的设计提供了一种新的策略。
相关研究成果以“A Strategy Based on Enzyme-Catalyzed Polymerization Reaction of Asp-Phe-Tyr Tripeptide for Cancer Immunotherapy”为题,近期发表在JACS (DOI:10.1021/jacs.1c00945)上。论文第一作者和共同第一作者分别为武汉大学博士生张秋玲和郑迪威,通讯作者为武汉大学张先正教授。论文得到了国家自然科学基金和国家重点研究发展计划等项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.1c00945
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 西安交大吴道澄团队 ACS Nano:分子堆砌@无限配位聚合物复合纳米粒实现肿瘤连续高强度光热-热动力交替循环治疗和化疗 2025-08-01
- 巴黎高科化学学院李敏慧教授与合作者 JACS: 创新型“类酶”纳米材料 → 饿死癌细胞 2025-07-20
- 武汉大学张先正教授团队《Nano Lett.》:微藻基“活”凝胶瘤内光合作用增强肿瘤饥饿/免疫疗法 2024-03-16
- 仰大勇教授课题组 Angew:智能DNA水凝胶用于黑色素瘤免疫与光动力协同治疗 2024-02-23
- 川大高会乐/曹俊 Adv. Sci.综述:PD-L1在癌症治疗中的空间异质性表达行为 - 挑战与机遇并存 2023-11-12
