目前,良性前列腺增生、恶性肿瘤和动静脉畸形等疾病严重危害人类的生命健康。传统的药物治疗和外科手术治疗所带来的副作用和创伤限制了它们在临床上的广泛使用。经导管动脉栓塞术(TAE)具有创伤小、简便、安全、疗效高和并发症少等多种优势,受到人们的广泛关注。传统的栓塞材料在临床使用过程中存在功能单一、药物释放快、缺乏X光显影性及栓塞剂返流等问题。因此,开发新型多功能栓塞材料成为TAE领域研究的热点。
近日,华中科技大学生命学院杨光教授团队在生物材料高水平期刊Bioactive Materials上发表了题为“Immobilized thrombin on X-ray radiopaque polyvinyl alcohol/chitosan embolic microspheres for precise localization and topical blood coagulation”的研究论文,该期刊的最新即时影响因子为13.07。
临床使用的栓塞剂绝大部分缺乏X光显影性,介入医师通常需要通过将栓塞材料与碘造影剂(如碘海醇、优维显等)物理混合然后注入到靶动脉。然而,这种方法存在几个方面的缺陷:首先,造影剂容易与栓塞剂分离,导致成像模糊或误诊;第二,造影剂的快速扩散导致TAE术后复查困难;第三,碘造影剂具有一定的肾毒性而且可能会引起一些患有甲状腺疾病的患者发生不良反应。栓塞过程中存在的另一个挑战是栓塞材料的返流现象,即栓塞材料进入血管后因为推注速度过快或注入过程中血流速度减慢等原因沿着与注入方向相反的方向流入其它动脉或导管。这种现象可能会导致严重的问题,包括非靶向性栓塞、导管夹闭,甚至治疗失败。
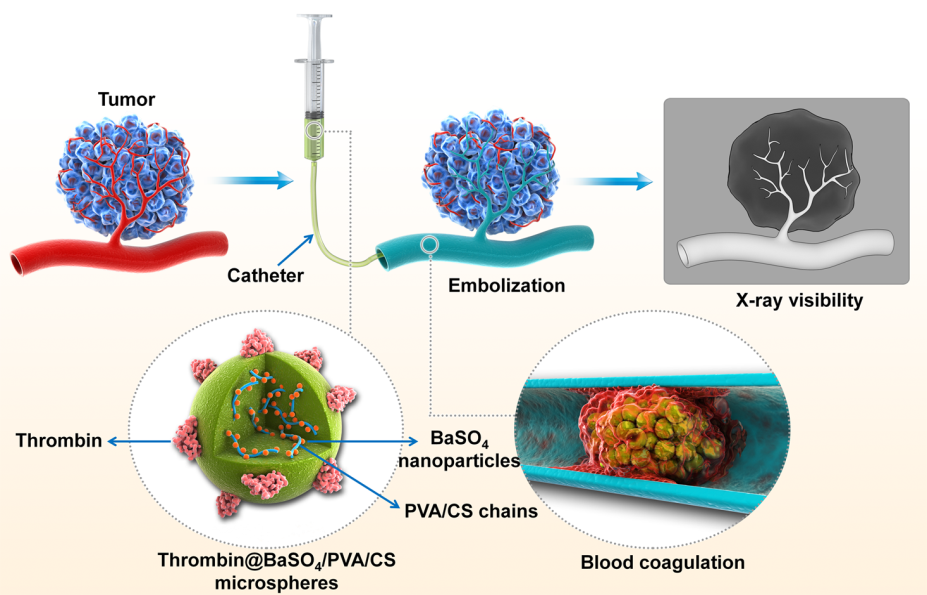
图1 兼具X光显影性和局部促凝血活性的凝血酶@BaSO4/PVA/CS微球用于动脉栓塞的示意图。
基于以上问题,研究团队开发一种同时负载凝血酶和BaSO4纳米颗粒的多功能栓塞微球,这种栓塞材料兼具X光显影性和局部促凝血的功能,能够实现栓塞过程中精准定位和避免栓塞剂的返流(图1)。该研究通过共沉淀法合成了BaSO4纳米颗粒作为X光显影剂,将其负载到聚乙烯醇/壳聚糖(PVA/CS)聚合物基质后制备成BaSO4/PVA/CS微球,然后将凝血酶共价负载到微球表面以实现微球的生物功能化。体外凝血动力学实验、全血凝集实验、血细胞粘附及血纤维蛋白诱导生成实验证实了凝血酶@BaSO4/PVA/CS微球具有较好的促凝血活性(图2)。此外,BaSO4/PVA/CS微球在X光下具有良好的显影性,随着BaSO4纳米颗粒负载量的增加,X光显影性能逐渐增强。兔耳中央动脉栓塞的实验结果表明了BaSO4/PVA/CS微球在体内具有长时间显影稳定性。此外,BaSO4/PVA/CS 和凝血酶@BaSO4/PVA/CS微球栓塞均能引起兔耳组织出现缺血坏死,且随着栓塞时间延长组织坏死情况更加严重(图3)。

图2 凝血酶@BaSO4/PVA/CS微球促凝血活性分析。A. 全血凝集动力学曲线。B. 全血在微球表面凝集测试。C. 血纤维蛋白诱导生成测试。
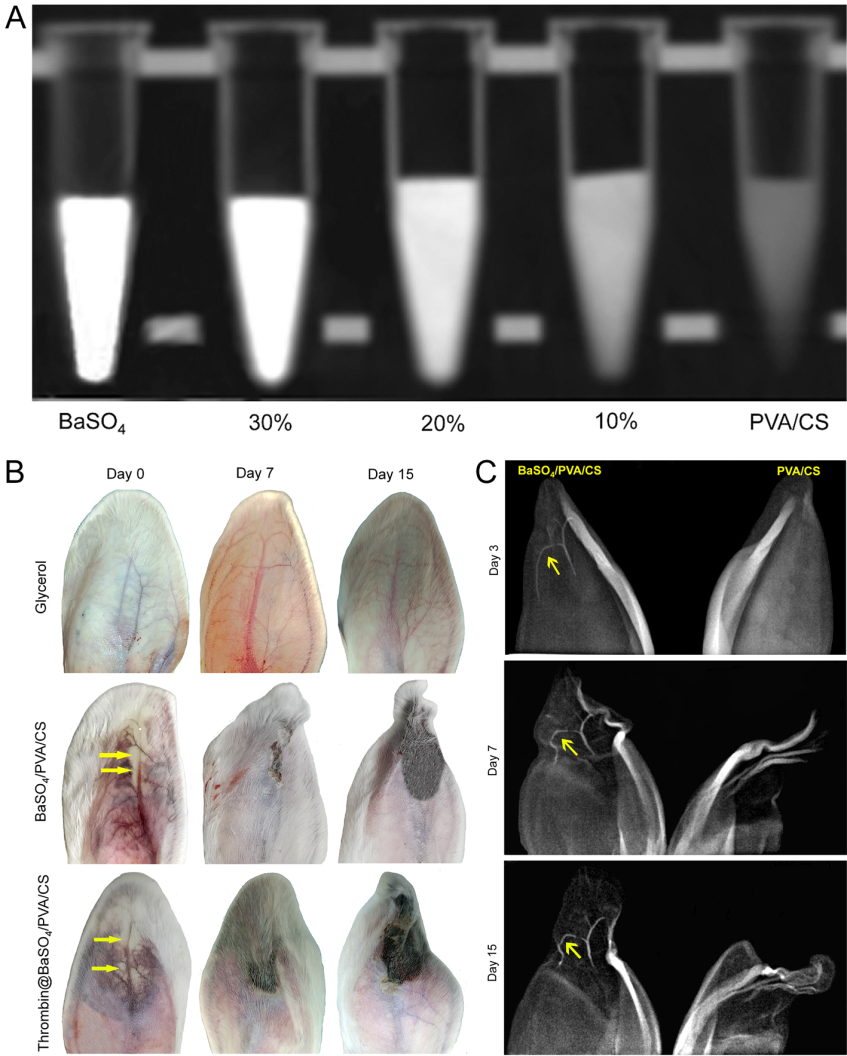
图3 A. 体外X光显影测试。B. 兔耳栓塞不同阶段形态变化分析。C. 微球体内X光显影分析。
华中科技大学生命科学与技术学院的杨光教授、华中科技大学同济医学院附属同济医院的肖骏教授以及中山大学生物医学工程学院的肖林博士为本论文的共同通讯作者,华中科技大学生命学院15级博士李晓宏为该论文第一作者。广东省人民医院骨科纪雄发博士后、华中科技大学同济医学院附属同济医院的博士李拔森等参与了该研究工作。研究工作得到了国家自然科学基金和国家重点研发计划等项目的资助。
论文链接:https://www.sciencedirect.com/science/article/pii/S2452199X20303388
在另一项研究工作中,该团队制备了一种具有离子交换性能的多孔PVA微球作为化疗栓塞的栓塞剂。首先通过反相乳化法结合热诱导相分离(TIPS)技术制备了多孔PVA(PPVA)微球,该微球球形规整,表面为“蜂窝状”多孔结构,通过淬火温度的改变可以有效调节微球的孔径(图4)。将对苯乙烯磺酸钠(SSS)单体在PPVA微球上接枝聚合,得到的PPVA-g-PSSS微球上具有带负电荷的磺酸根基团,因而可以通过离子交换机制将带正电荷的DOX有效地负载到接枝的 PPVA-g-PSSS微球中, 这种载药微球在体外具有长时间药物缓释性能(图5)。

图4 A. 反相乳化法结合TIPS技术制备PPVA微球的示意图。B. 在不同淬火温度下制备的PPVA微球的FESEM图:(a1, a2)-196 oC, (b1, b2)-80 oC, (c1, c2)-23 oC, (d1, d2)-15 oC。

图5 A. 接枝聚合法制备PPVA-g-PSSS微球及通过离子交换交换机制负载DOX的示意图。B. 每10 μm为间隔拍摄的DOX@PPVA-g-PSSS微球的CLSM图(标尺为60 μm)。C. PPVA、PPVA-g-PSSS和DOX@PPVA-g-PSSS微球的表面和截面FESEM图。D. 体外药物释放性能分析。
通过体外抗肿瘤活性测试表明,这种载药微球对HepG2细胞具有明显的抑制作用。兔耳动脉栓塞的结果表明在栓塞3、7、15天后,DOX在兔耳血管周围组织的荧光强度没有降低,载药微球在组织中能维持较长时间的药物浓度(图6),这种新型药物缓释体系有望提高肝癌栓塞的治疗效果。
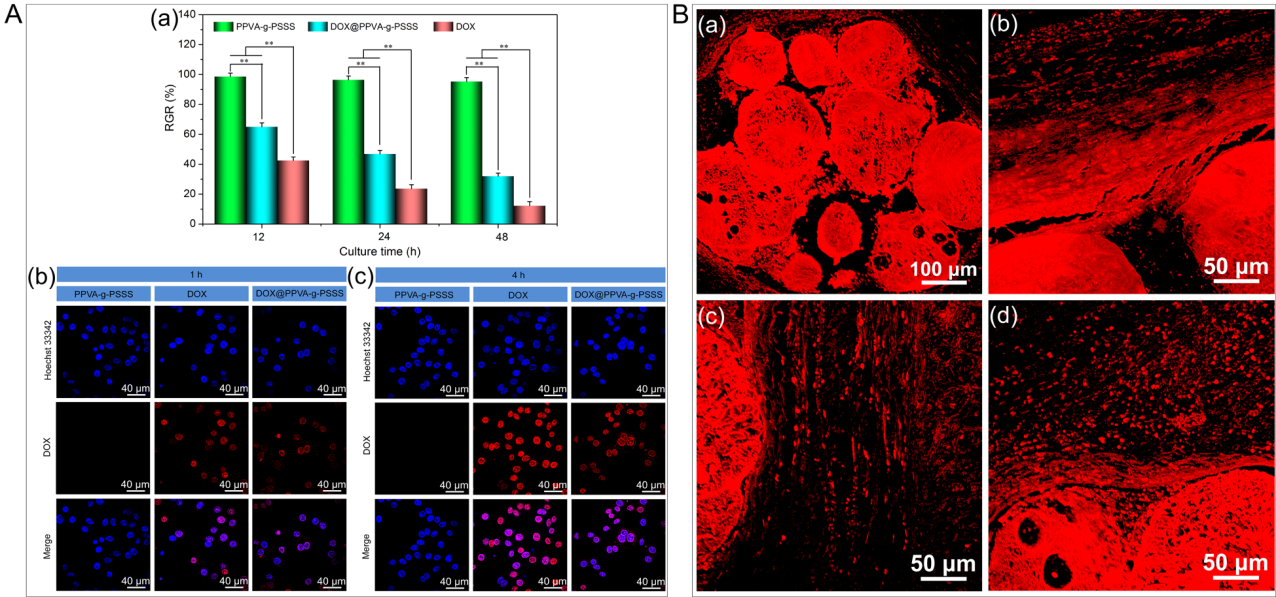
图6 A. 体外抗肿瘤活性分析:(a) 微球及药物对HepG2细胞的毒性分析(CCK-8)。(b)和(c)分别为微球和药物与HepG2细胞共孵育1 h和4 h的CLSM图像。B. 兔耳组织中DOX荧光分布分析:(a)DOX@PPVA-g-PSSS微球栓塞兔耳中央动脉3天后微球在兔耳动脉分布的CLSM图像(横切面),(b)-(d)DOX@PPVA-g-PSSS微球分别栓塞兔耳中央动脉3、7、15天后DOX在血管周围组织分布的荧光图像。
该研究工作以“Preparation and evaluation of ion-exchange porous polyvinyl alcohol
microspheres as a potential drug delivery embolization system”为题发表在Materials Science & Engineering C上。
论文链接:https://www.sciencedirect.com/science/article/pii/S0928493121000278
此外,该团队针对目前尚无载药栓塞剂用于良性前列腺增生的治疗和研究的现状,开发了多种药物递送系统,将前列腺动脉栓塞术和局部药物治疗结合起来,对增强BPH的治疗效果具有非常重要的意义,同时为开发新一代载药栓塞材料用于良性前列腺增生的应用和研究提供了重要的实验支撑。
研究成果分别发表在Materials Science & Engineering C 、Biomaterials Science 和Engineered Science上。
论文链接:
https://www.sciencedirect.com/science/article/pii/S0928493119337002
https://pubs.rsc.org/en/content/articlelanding/2020/bm/c9bm01775e#!divAbstract
http://www.espublisher.com/journals/articledetails/384
