最近,国际权威期刊Nano Letters(影响因子12.08)在线报道了中国药科大学孙敏捷教授和钱程根副研究员在抗肿瘤研究取得的最新进展——Biomimetic hybrid nanozymes with self-supplied H+ and accelerated O2 generation for enhanced starvation and photodynamic therapy against hypoxic tumors。中国药科大学博士生杨学为论文第一作者,孙敏捷教授和钱程根副研究员为本文共同通讯作者。
自2007年Fe3O4纳米颗粒被报道具有过氧化物酶活性以来,纳米酶作为一种模拟天然酶活性的人工酶,和天然酶一起在癌症的诊断和治疗中得到了广泛的关注。然而,如何保证酶在活体复杂的肿瘤微环境下还具有较强的酶活性仍是一个挑战。例如:葡萄糖氧化酶(glucose oxidase, GOx)是一种天然的需氧酶,可以将葡萄糖氧化成葡萄糖酸和过氧化氢来干扰葡萄糖代谢,从而实现肿瘤饥饿治疗。然而在肿瘤缺氧区域GOx酶活性随着氧气水平的降低而减弱。二氧化锰(manganese dioxide,MnO2)是一种具有过氧化氢酶活性的纳米酶,它与肿瘤内源性过氧化氢反应生成氧气,以减轻肿瘤乏氧。在酸性条件下,MnO2的催化效率可以大大提高。
针对上述问题,中国药科大学孙敏捷教授课题组采用纳米酶和天然酶相互促进的策略设计了一种高酶活性的新型仿生杂化纳米酶(rMGB)用于乏氧肿瘤治疗。在这项研究中,通过整合纳米酶MnO2和天然酶GOx的特性,在肿瘤乏氧环境下,rMGB仿生纳米酶系统中的MnO2可以与内源性H2O2反应生成O2,从而提高GOx的酶活性用于加速肿瘤饥饿治疗的葡萄糖消耗;同时GOx通过氧化葡萄糖生成葡萄糖酸,提供大量的氢离子可以最大限度地提高MnO2的催化效率,进一步加速局部O2的生成,在肿瘤光动力治疗中减轻肿瘤乏氧,加速具有肿瘤杀伤性的活性氧物质的生成。因此,rMGB利用纳米酶和天然酶的相互促进,实现自供H+和加速O2生成,减轻肿瘤乏氧,提高抗肿瘤效率(图1和2)。
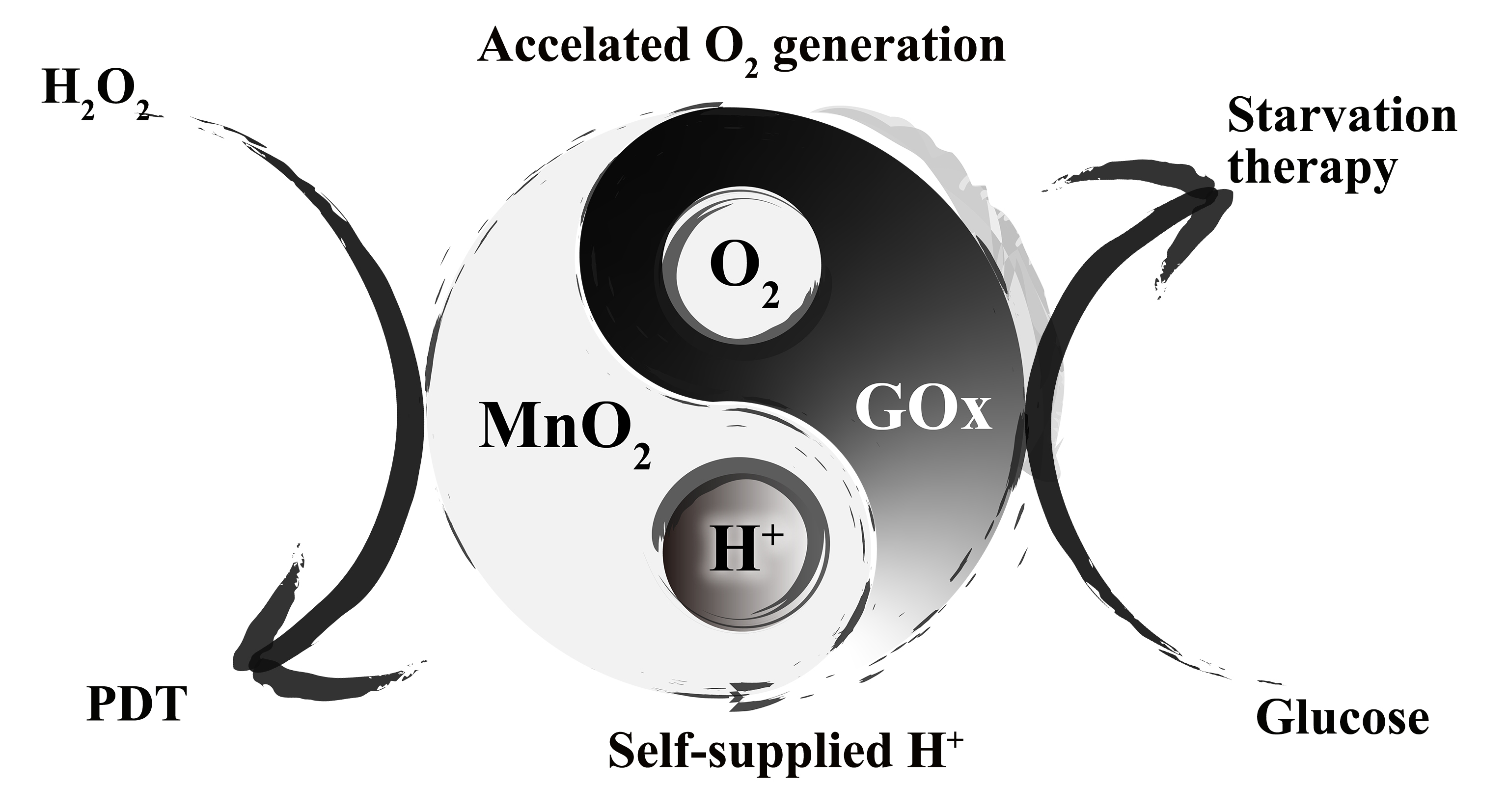
图1. 仿生杂化纳米酶rMGB中纳米酶MnO2和天然酶GOx相互促进示意图
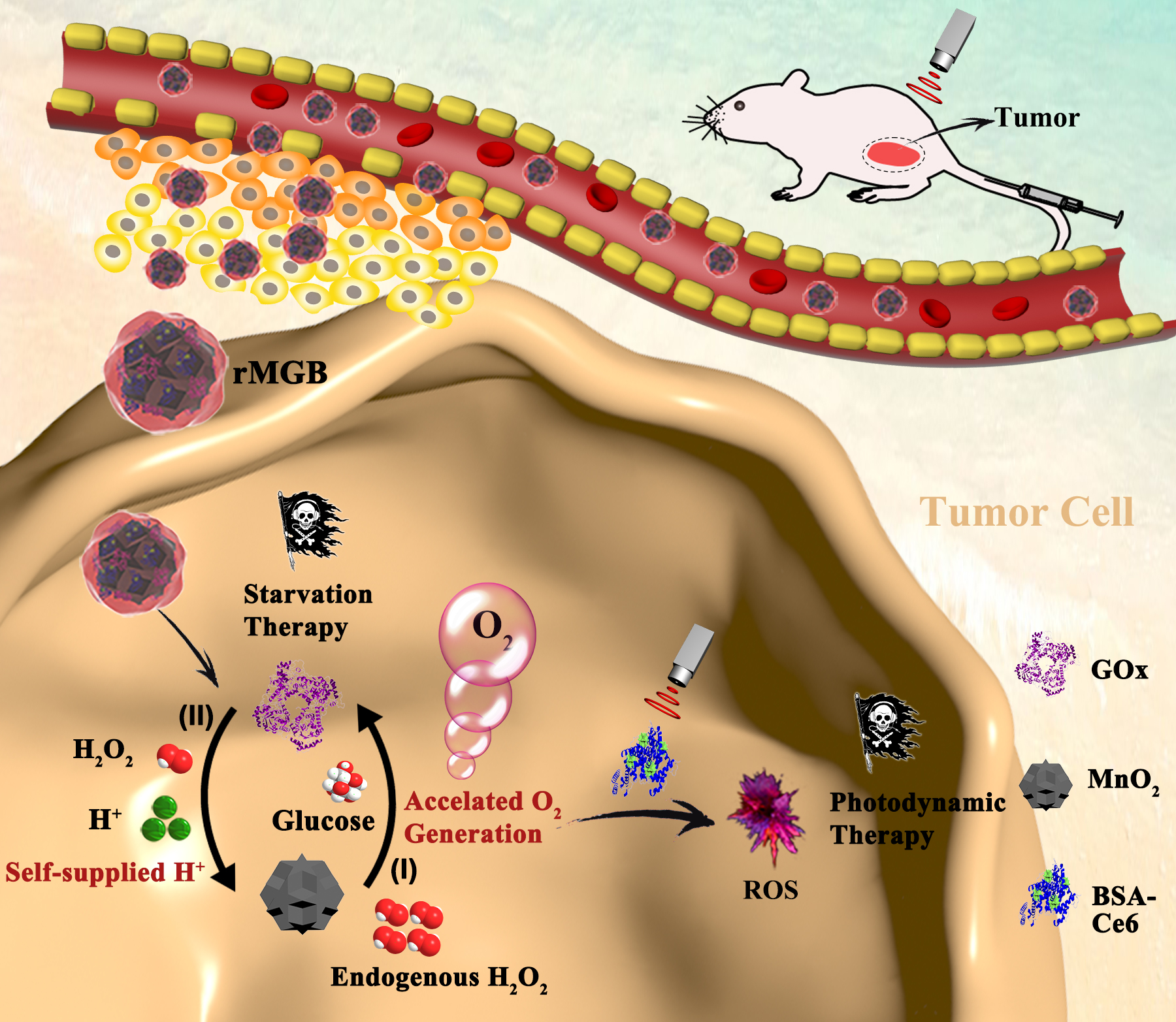
图2. 新型仿生杂化纳米酶通过自供H+和加速O2生成实现乏氧肿瘤光动力治疗和饥饿治疗
研究结果表明,设计的仿生杂化纳米酶rMGB在常氧和乏氧条件下均能产生连续的O2。尤其对乏氧肿瘤具有较强的饥饿治疗和PDT协同治疗作用,在体内外均有较强的抗肿瘤作用。此外,由于rMGB外包覆的红细胞膜的长循环能力和优异的生物安全性,rMGB是一种安全的药物传递系统,小鼠安全性实验初步证明不会引起系统性的影响。这种仿生杂化纳米酶有望成为低氧肿瘤治疗的潜在供氧剂。同时,该杂化纳米酶为开发用于癌症治疗的催化纳米药物提供了创新的设计指导。
该研究得到了国家重大研发计划“纳米专项”、国家自然科学基金面上和青年项目、江苏省杰出青年基金等资助。特别感谢中国药科大学天然药物活性组分与药效国家重点实验室提供的研究平台支持。
- 石河子大学贾鑫/孙美州团队 Matter:光热响应微针纳米酶构建植物-材料生物界面 - 实现精准养分递送与氧化应激调控 2026-03-16
- 天工大高辉/余云健团队 ACS Nano:创新纳米酶精准消除肿瘤胞内菌 助力结直肠癌免疫治疗突破 2026-02-20
- 杭师大黄又举教授团队 AFM:超强H2O2亲和力的体外医疗诊断试剂盒 2025-09-08
- 武汉大学张先正教授团队《Nano Lett.》:微藻基“活”凝胶瘤内光合作用增强肿瘤饥饿/免疫疗法 2024-03-16
- 澳门大学代云路课题组 AFM:利用金属-多酚纳米递送平台结合可调控的低强度超声实现肿瘤放疗增敏及放疗-声动力联合疗法 2022-07-22
- 浙江大学周民团队《Sci. Adv.》:活性微藻调节肿瘤乏氧,提高肿瘤联合治疗效果 2020-05-29
