
干细胞疗法在退行性病变和组织损伤修复中具有较好的应用前景。在各种类型的干细胞中,间充质干细胞(MSC)因其强大的自我更新能力、免疫调节能力和旁分泌功能而被视为再生医学的理想种子细胞。然而,传统贴壁培养扩增后的MSC在临床应用及动物实验中存活率较低,其治疗效果达不到理论高度。这可能是由于体外扩增的2D细胞层与体内3D组织体的微环境相差较大,导致干细胞衰老、分化和旁分泌能力降低,进而使移植的MSC的体内保护作用减弱。由于结构和性能与细胞外基质(ECM)类似,生物材料目前已被广泛应用于干细胞疗法以促进移植细胞的滞留率和存活。尽管模拟ECM的功能性生物材料在开发中取得了相当大的进展,但大多数合成材料仍然缺乏天然ECM所表现出的动态特性。例如,细胞介导的动态ECM重塑(如纤连蛋白的展开),其在组织结构形成、内环境稳态等基本生理活动中发挥着重要的协调作用。利用简便的方法设计合成生物响应性材料诱导3D干细胞球体仍然是一个巨大的挑战。
受此启发,南方医科大学陈敏生教授和蔡延滨副教授团队研发了一种具有生物响应性的酶促自组装多肽(Nap-pD-E7),该多肽由自组装单元、酶触发底物和MSC锚定基序共价结合而成。这种酶促自组装磷酸肽能够靶向锚定于MSC细胞表面,随后它在细胞间隙被碱性磷酸酶去磷酸化,以此提供一个动态转变的微环境来自组装形成纳米纤维结构。这种原位自组装纳米纤维能够增强细胞-ECM和细胞-细胞粘附力并诱导MSC形成3D细胞球体(图1)。进一步的研究表明,细胞间的组装体和ECM分子的相互作用增强了纤维粘附,并且MSC细胞球体的形成激活了细胞HIF-1α信号通路,继而增强MSC的旁分泌功能,促进血管新生。最后,通过构建仿生组织修复体系,评估了该仿生系统在小鼠心肌梗死模型中的治疗效果。目前,这一研究成果已发表于期刊Chemical Engineering Journal上,题目为“Enzymatic self-assembly nanofibers anchoring mesenchymal stem cells induce cell spheroids and amplify paracrine function for myocardial infarction therapy”,硕士研究生范祥霖、战捷博士为第一作者,陈敏生教授、蔡延滨副教授为通讯作者。该研究得到了国家自然科学基金、广东省基础和应用基础研究基金和中国博士后科学基金创新支持计划的支持。

图1: Nap-pD-E7诱导MSC球体的形成及其在小鼠心肌梗死治疗中的应用。
【本文要点】
(1)设计与合成具有生物响应性的酶促自组装多肽Nap-pD-E7
利用固相合成法合成Nap-pD-E7,通过流变,透射电镜和圆二色谱等方法对材料的组装性能进行表征。

图2:Nap-pD-E7的设计合成及表征。
(2)MSC细胞球体的形成及相关机制研究
Nap-pD-E7可以通过与内源性ECM分子相互作用诱导MSC形成细胞球体,并且磷酸化-去磷酸化这一动态转化过程和E7靶向序列对细胞球体的形成至关重要。

图3:MSC细胞球体的形成及Nap-pD-E7材料与ECM分子的共定位。
(3)MSC细胞球体的形成对细胞旁分泌功能的影响
通过qPCR、WB和免疫荧光等实验研究细胞球体的旁分泌功能。与对照组相比,细胞球体形成后MSC的旁分泌功能有所增强,特别是促血管生长相关因子,这一细胞功能的改变与HIF-1α信号通路的激活有关。
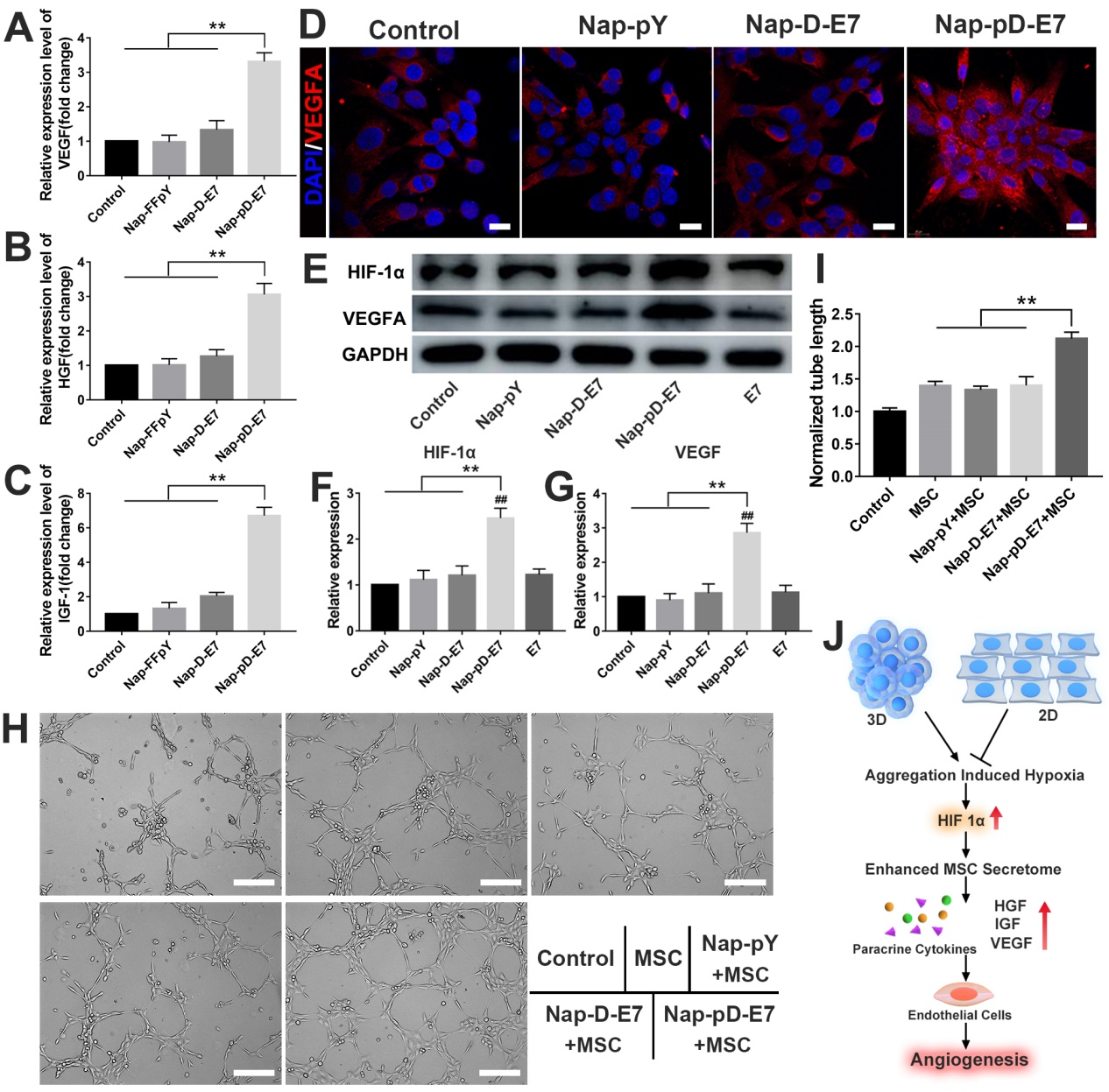
图4:MSC细胞球体旁分泌功能的增强及相关机制探讨。
(4)仿生组织修复体系对心梗小鼠心脏功能的影响
由于MSC细胞球体旁分泌功能的增强有助于缺血损伤组织的修复,因此构建了Nap-pD-E7水凝胶包裹MSC细胞球体的仿生移植体系。在相关动物实验中,该仿生系统的移植明显减轻了心肌梗死后心脏功能的恶化。
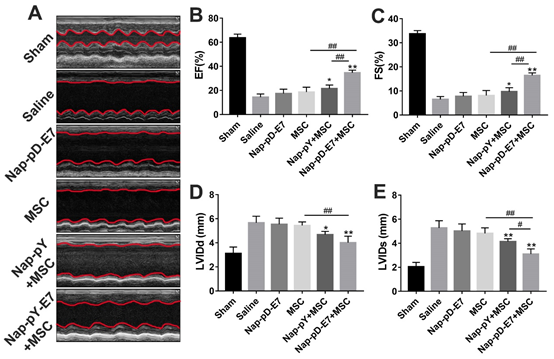
图5:仿生移植体系的构建及其在小鼠心肌梗死治疗中的应用。
(5)仿生组织修复体系对心梗小鼠心脏重构和血管新生的影响。
通过心脏组织切片染色研究该仿生体系对心梗小鼠心室重构和梗死周边区域血管新生的影响。结果表明,Nap-pD-E7水凝胶包裹MSC细胞球的移植能减轻心梗后左心室胶原沉积和不良肥大,同时促进梗死周边区小血管的新生,以保留更多的心肌细胞。

图6:心肌梗死后心室重构的变化。
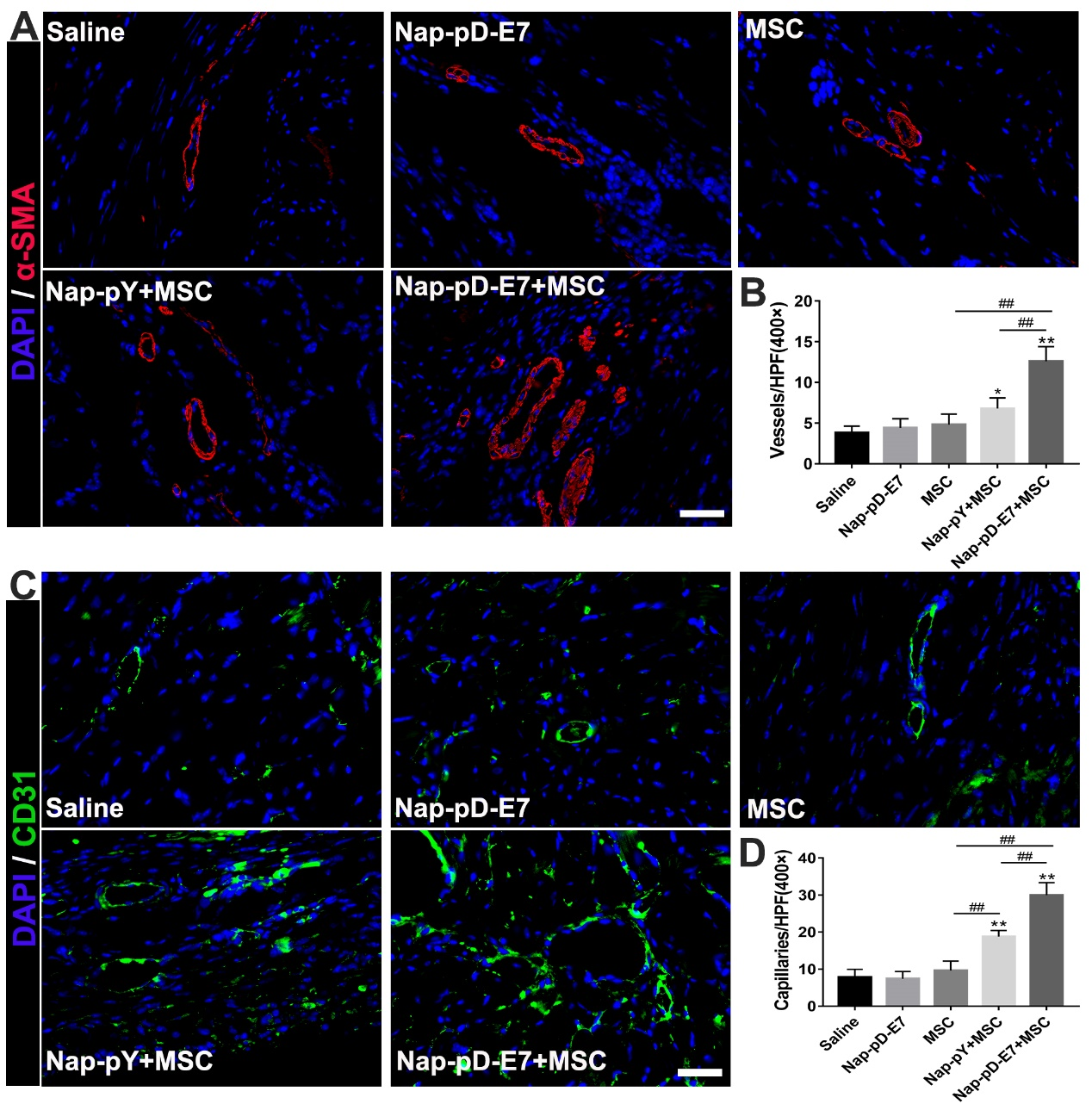
图7:心肌梗死周边区域小血管新生情况。
文章链接:https://doi.org/10.1016/j.cej.2022.135224
通讯作者简介
陈敏生教授:二级教授,博导,国务院特殊津贴专家,主要从事心血管疾病临床与发病机制研究、心血管组织工程、药物释放等研究。长期致力于可注射功能化水凝胶体系制备及其对微环境调控,功能化水凝胶在细胞三维培养、药物传输与缓释、干细胞移植、心肌修复等领域的研究,以通讯作者在Adv. Sci., Biomaterials, Theranostics, ACS Appl. Mater. Interfaces, ATVB等学术期刊上发表一系列研究成果。先后主持承担国家“863计划”子项目2项、国家自然科学基金(含重点项目1项)6项、广东省科技计划项目5项、广东省自然科学基金项目3项、广州市科技计划项目(含市教育局创新团队项目)7项,横向课题和院级课题各1项。国家发明专利6项,主编专著3部:《疾病诊断治疗常规》(广东高教出版社出版,120万字)、《心血管病学前沿--基础与临床》(广东科技出版社,118万字)及《生命救助手册》。获教育部科技进步二等奖、广东省科技进步二等奖、广州市科技进步二等奖各2项,广东省教育厅科技进步三等奖、广州市科技进步三等奖各1项。担任国家科学技术奖评审专家,国家自然科学基金委员会同行评议专家,全国高等医学教材建设指导委员会理事,广东省医学会心血管病分会副主任委员,广东省医学会健康管理学分会主任委员、《南方医科大学学报》主编。
蔡延滨副教授:硕士生导师,广东省药理学会心血管专委会常委,广东省病生学会心血管青年委员会委员,主要从事小分子多肽水凝胶体系及其生物医学应用的研究,具体包括:基于自组装多肽的新型抗癌纳米药物;多肽自组装的纳米荧光探针的构建及其在生物检测中的应用;多肽自组装材料及生物相容性水凝胶材料在心血管疾病中的应用,以第一或通讯作者在J. Am. Chem. Soc., Angew. Chem. Int. Ed., Biomaterials, Theranostics, ACS Appl. Mater. Interfaces, Anal. Chem., Chem. Commun., Nanoscale等学术期刊上发表SCI论文20余篇。主持国家自然科学基金2项,广东省自然科学基金2项。
- 四川大学丁明明教授/付维力教授《Nat. Commun.》:生物响应和生物活性多色荧光高分子 2024-11-24
- 四川大学林云锋教授课题组《Adv. Mater.》: “太阳神鸟”启发的基于四面体框架核酸的生物响应性miRNA递送系统 2022-08-01
- 新加坡国立大学熊泽博士和John S. Ho教授团队《Sci. Adv.》:基于DNA水凝胶的无线、柔性伤口感染监测器件 2021-11-23
- 同济大学杜建忠/范震团队《Adv. Funct. Mater.》:酶促自组装多肽纳米颗粒治疗细菌性感染伤口 2023-03-13
- 东华大学朱美芳/成艳华团队 Adv. Mater.:轻质热防护材料助力空间离轨与柔性舱展开系统 2026-06-02
- 中国矿业大学 Nat. Commun.:深地深空复杂条件微环境管理多级异质界面纳纤 2026-05-15
- 苏州大学汪晓巧教授、张克勤教授团队 ACS Nano:兼具辐射制冷与空气过滤双功能的螺旋纳米纤维膜 2026-04-30
