利用人工设计的功能分子调控细胞间的识别并进一步调控细胞的行为和功能是近年来生命科学领域的研究热点。作为一种生物材料,DNA分子具有序列可编程性并且可与其他功能分子耦合实现多级次组装,在细胞表面工程化及细胞相互作用调控等方面具有良好的应用前景。然而,由于细胞对纳米材料的内吞作用以及细胞膜结构高度动态的特性,利用DNA纳米结构对活细胞膜表面进行可控组装进而精准调控细胞间相互作用仍然存在一定的困难。
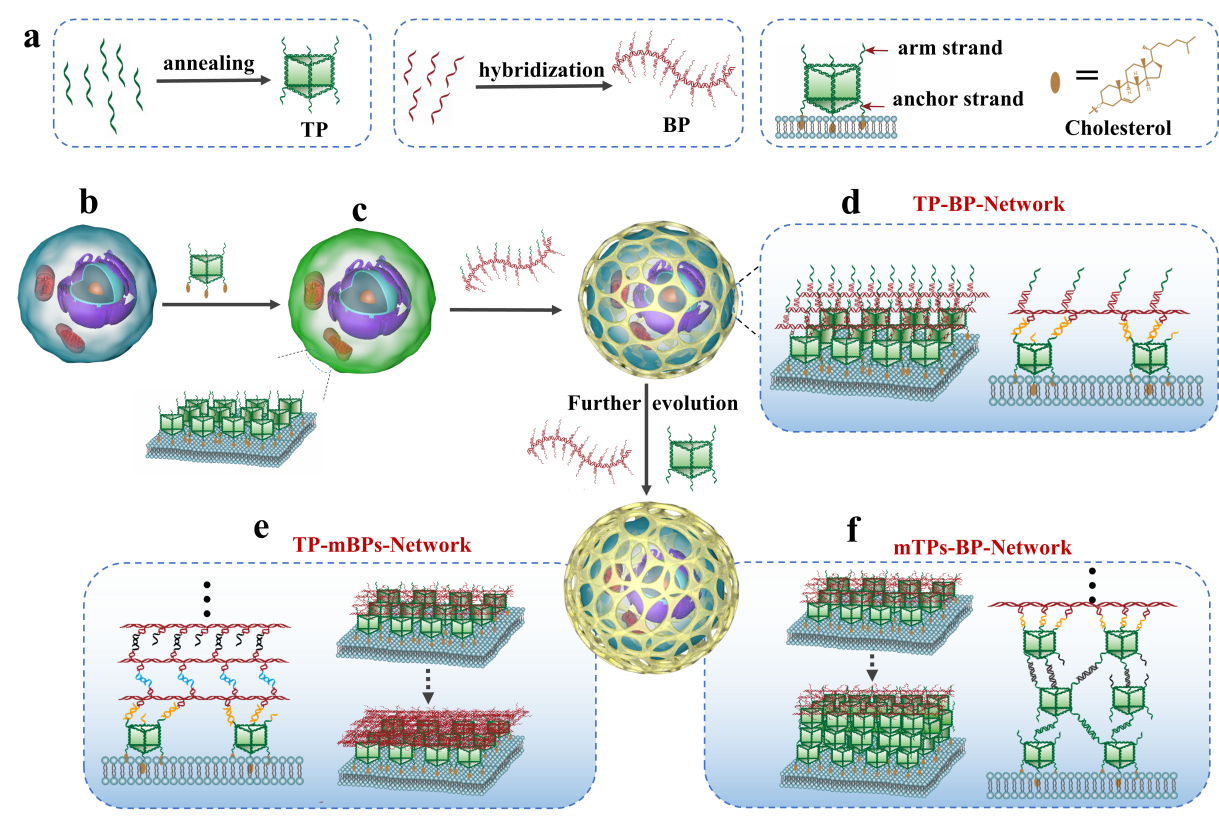
图1 活细胞膜表面构筑可调控的多层DNA网络结构示意图
近期,湖南大学谭蔚泓院士团队刘巧玲课题组采用经典的DNA纳米三棱柱(TP)和DNA纳米分支聚合物(BP)作为结构单元,利用DNA分子自组装技术在细胞膜表面设计了一种全新的灵活可调控的DNA网络结构用于操控细胞间的相互作用(图1)。源于互补DNA链的碱基之间形成的可预测和稳定的配对结构,这些DNA网络结构之间的相互作用增加了DNA纳米结构在细胞膜表面的稳定性并且克服了细胞内化的问题。通过对DNA网络结构中的识别单元进行合理设计,研究人员对细胞间的特异性识别、刺激响应性识别以及动态可逆相互作用进行了人为设计和操控,并且实现细胞间物质传输的调控(图2)。

图2 利用DNA结构网络操控多种形式的细胞间相互作用
综上所述,这种DNA网络结构赋予了可调控的细胞识别能力,为人为操控细胞间相互作用提供了一种简单、普适的策略,有助于拓展基于DNA分子的人工识别体系在细胞表面工程、合成生物学和生物医学领域中的应用。该工作以“Manipulation of Multiple Cell-Cell Interactions by Tunable DNA Scaffold Networks”为题发表在《Angew. Chem. Int. Ed.》上。文章第一作者是湖南大学大学博士研究生郭振振。
此工作是该课题组将DNA纳米技术用于生物膜界面功能化设计与调控的最新进展之一。近年来,课题组围绕基于细胞膜囊泡的人工细胞的构筑和应用开展研究工作,建立了基于细胞膜囊泡的新型细胞仿生模型(Research, 2019, 6523970),结合DNA纳米技术对细胞膜囊泡进行功化设计与改造(J. Am.Chem. Soc., 2017, 139, 12410-12413)获得易于操控的人工细胞,实现了人工细胞对外界环境变化的动态响应与反馈(J. Am. Chem. Soc., 2019, 141, 6458-6461),以及人工细胞与外界环境、人工细胞之间的物质交换与信息交流(Nature Commun., 2020, 11, 978;J. Am. Chem. Soc. 2021, 143, 232-24),为构筑智能化人工生命体系提供新方法。
原文链接:https://doi.org/10.1002/anie.202111151
- 南开大学王粉粉、河北工业大学瞿雄伟/陈胜利 JACS:异步聚合-结晶动力学驱动的分级自组装 - 从V-型缺口球晶到多级防伪材料 2026-03-10
- 郑州大学庞新厂/张文杰/何彦洁教授团队 ACS Nano:多级金纳米团簇组装体的精准胶体聚合 2026-03-06
- 香港中文大学(深圳)唐本忠团队 Nat. Commun.:均聚多肽自组装体系圆偏振室温磷光 2026-02-24
- 天津大学仰大勇课题组《Nat. Commun.》:利用DNA功能材料在活细胞中构建人工过氧化物酶体 2022-12-22
- 北京大学张成/许进团队JACS封面:可重构DNA分子电路 2019-10-10
- MIT科学家首次发现一种生物机制能控制DNA分子扭结 2018-05-09
