联合用药可以有效克服单一化疗药物治疗的缺点,减少癌细胞耐药性的产生,降低毒副作用,并可以通过不同药物的协同效应增强治疗效果。蛋白药物具有功能活性高、特异性强、副作用小以及遗传风险低等优点,将其与化疗药物联合使用在基础研究以及临床评估中已经取得了重要进展。然而,常用的与化疗药物联合应用的蛋白药物主要是细胞因子及单克隆抗体等在细胞外发挥功能的蛋白。细胞内发挥抗癌功能的蛋白具有与细胞因子及单克隆抗体不同的抗癌机制,因此,将其与化疗药物联合使用可以为新型联合疗法的开发提供更多选择。然而,如何在同一个纳米结构中高效共担载理化性质差异极大的疏水化疗药物和亲水蛋白药物,实现两种药物的体内稳定递送,细胞内的可控释放,以及蛋白药物的内涵体/溶酶体逃逸是这两种药物共递送载体开发所面临的巨大挑战。
针对以上问题,中国科学院长春应用化学研究所陈学思院士和肖春生副研究员团队设计、合成了一种含有邻苯二酚(CA)侧基和三级胺(TA)侧基的mPEG-b-PGCA-b-PGTA三嵌段共聚物,并将其用于高效共担载核糖核酸酶A(RNase A)和阿霉素,实现了高效的协同抗肿瘤效果(图1)。其中,阿霉素(DOX)被包裹在pH响应性的PGTA链段,而苯硼酸修饰的RNase A(RNBC)则通过通过苯硼酸键共价结合作用担载在含邻苯二酚基团的PGCA链段,从而形成稳定的载药纳米粒子。当载药纳米粒子进入细胞后,内涵体/溶酶体的酸性微环境促使PGTA链段的三级胺侧基质子化引起PGTA链段亲水性增加。同时,邻苯二酚与苯硼酸的结合作用也在酸性条件下解离,从而实现DOX及RNBC的共同释放。PGTA链段的三级胺侧基还具有质子海绵效应,能够实现RNBC的内涵体/溶酶体逃逸,而逃逸后的RNBC会在DOX介导的癌细胞内高水平ROS的作用下实现苯硼酸基团的去修饰,恢复为天然的RNase A,从而实现高效的协同抗肿瘤作用(图1)。
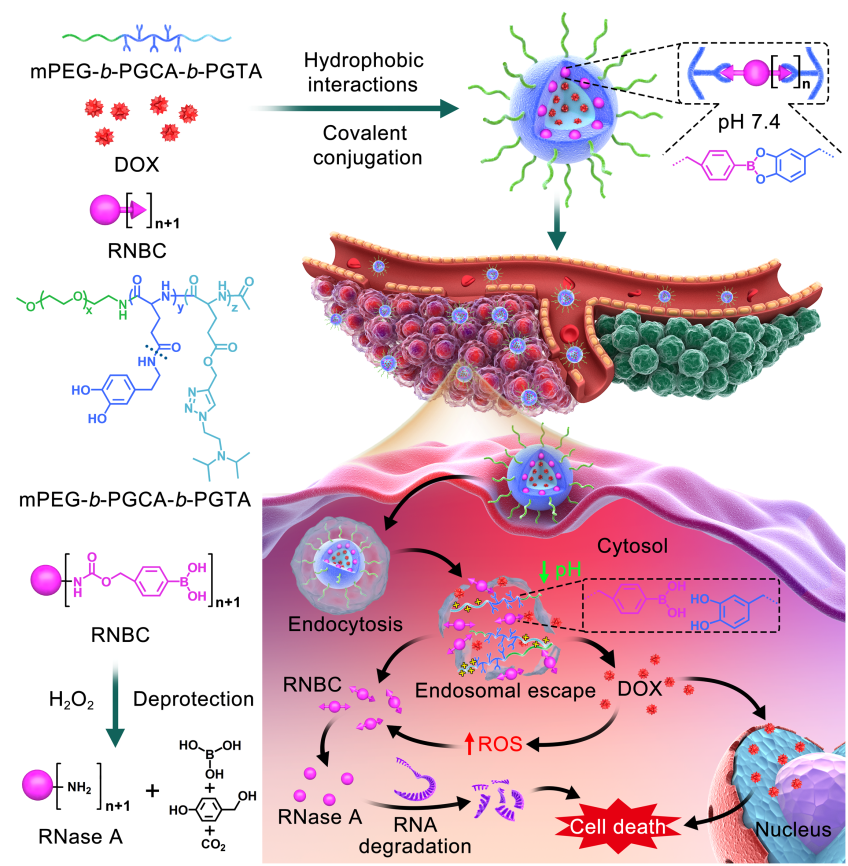
图1. 基于mPEG-b-PGCA-b-PGTA的多级协作纳米平台用于蛋白药物及小分子化疗药物细胞内共递送的示意图
实验结果表明,mPEG-b-PGCA-b-PGTA可有效共担载DOX及RNBC,获得药物共担载纳米粒子NP-DOX-RNBC(图2A)。体外药物释放实验结果表明,NP-DOX-RNBC具有可控的酸响应药物释放行为,且由于邻苯二酚与硼酸的共价结合能力强于葡萄糖,生理浓度(10 mM)的葡萄糖不会影响其药物释放行为(图2B和2C)。这表明NP-DOX-RNBC具有较好的生理稳定性,可用于DOX及RNase A的体内稳定共传输。共聚焦成像结果表明,NP-DOX-RNBC可将DOX及RNBC共递送入癌细胞内,其中DOX被递送入细胞核中,而RNBC被递送入细胞质中(图3)。细胞内ROS水平检测结果表明,NP-DOX-RNBC释放的DOX显著提高了细胞内的ROS水平,可促进细胞内RNBC的苯硼酸去修饰,获得天然的RNase A(图4A)。细胞活性及细胞凋亡检测结果表明,NP-DOX-RNBC具有体外协同的抗肿瘤细胞增殖及癌细胞凋亡诱导效果(图4B和4C)。动物实验结果表明,NP-DOX-RNBC具有体内协同增强的抗肿瘤效果,且其治疗组具有最长的生存时间(图5)。鉴于动态共价键的通用性,该多级协作纳米平台有望进一步应用于其他小分子化疗药物及细胞内活性蛋白药物组合的细胞内共递送。
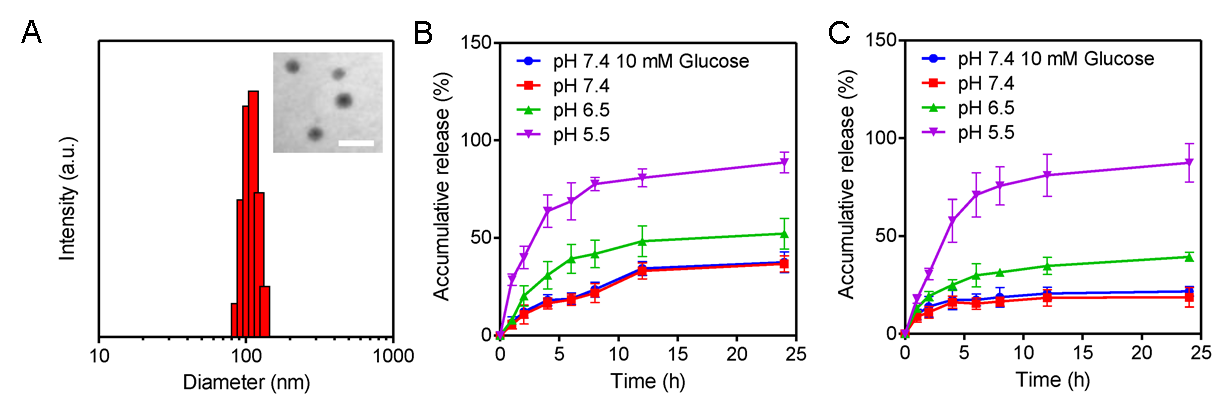
图2. (A)NP-DOX-RNBC的粒径及形态;(B)DOX的体外释放结果;(C)RNBC的体外释放结果。
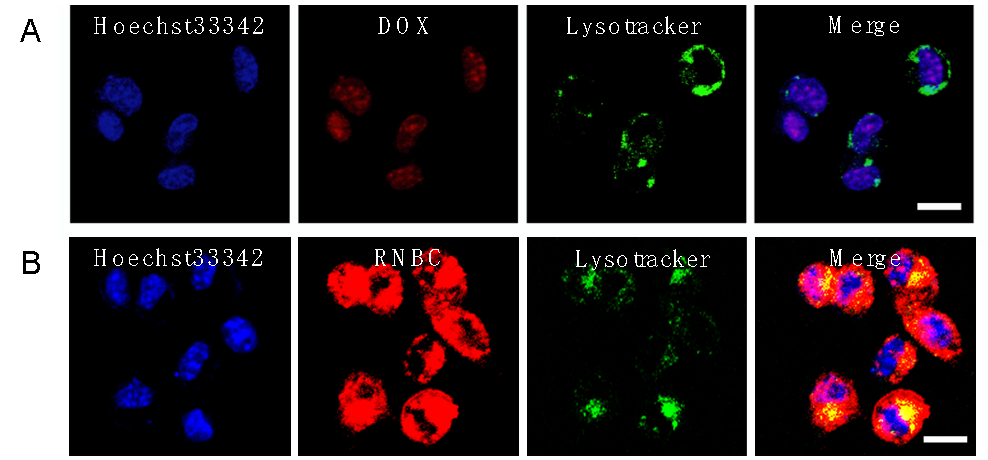
图3. (A)NP-DOX-RNBC介导的细胞内DOX递送结果;(B)NP-DOX-RNBC介导的细胞内RNBC递送结果。
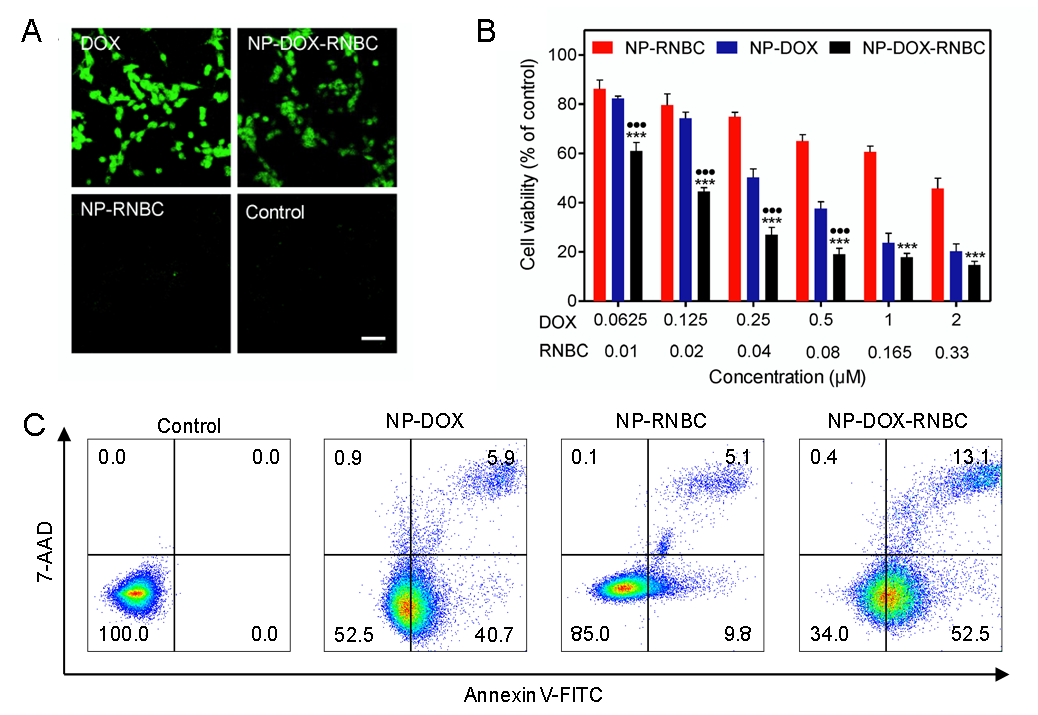
图4. (A)不同药物处理后的细胞内ROS水平检测结果;(B)不同纳米药物处理后的细胞活性检测结果;(C)不同纳米药物处理后的细胞凋亡检测结果。
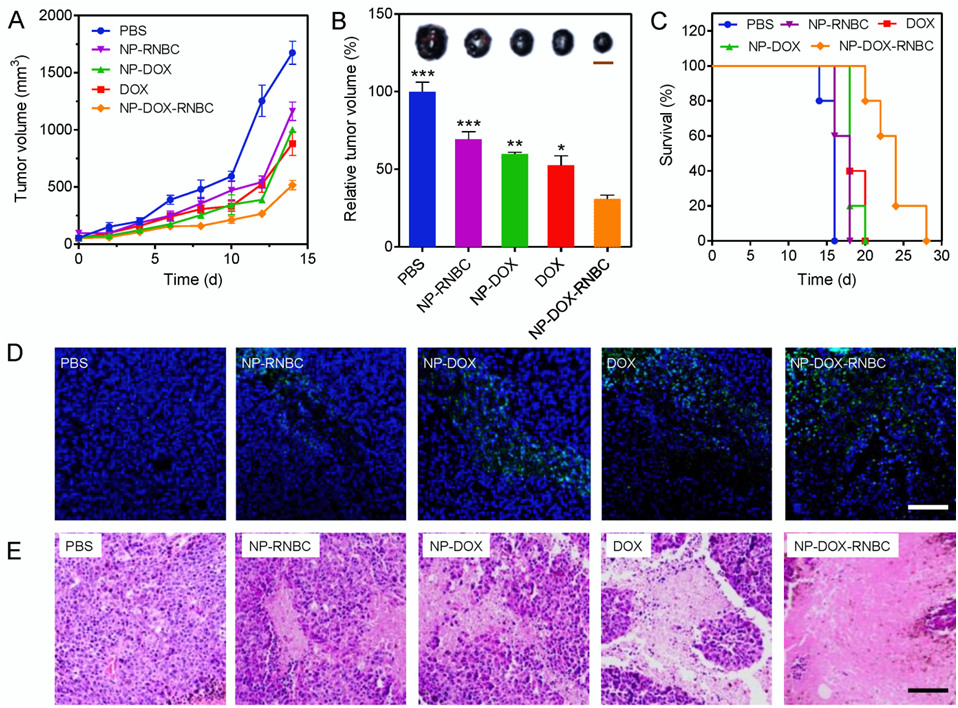
图5. (A)不同药物治疗组的肿瘤生长曲线;(B)不同药物治疗组的相对肿瘤体积;(C)不同药物治疗组的小鼠生存期;(D)不同药物治疗组肿瘤组织的TUNEL检测结果;(E)不同药物治疗组肿瘤组织的H&E染色结果。
以上研究成果发表在Advanced Materials(10.1002/adma.202000013)上,论文的第一作者为中国科学院长春应用化学研究所助理研究员张鹏,通讯作者为中国科学院长春应用化学研究所陈学思院士及肖春生副研究员。该研究工作得到国家自然科学基金、吉林省科技发展计划项目以及中国科学院青年创新促进会项目的资助。
原文链接:https://doi.org/10.1002/adma.202000013
- 天津大学宋东坡教授/复旦大学李卫华教授 Angew:非对称瓶刷嵌段共聚物相图 - 发现稳定六方穿孔层状结构(HPL) 2026-04-22
- 复旦大学彭娟团队 Macromolecules: 分子工程实现共轭嵌段共聚物结晶取向的高效调控 2026-04-07
- 华科大王勇研究员团队 JACS:有机硼介导的有氧串联聚合新策略-构建嵌段共聚物一锅法合成通用平台 2026-03-04
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 西安交大吴道澄团队 ACS Nano:分子堆砌@无限配位聚合物复合纳米粒实现肿瘤连续高强度光热-热动力交替循环治疗和化疗 2025-08-01
- 巴黎高科化学学院李敏慧教授与合作者 JACS: 创新型“类酶”纳米材料 → 饿死癌细胞 2025-07-20
- 中科大王育才/朱书/蒋为团队 Science:系统揭示高分子载体材料发生系统性清除的底层机制 2026-03-20
