骨质疏松性骨折愈合困难是临床面临的挑战之一。这不仅源于骨质疏松导致的骨结构脆弱和缺损,还与骨折局部失衡的骨重塑微环境密切相关,主要体现在持续的慢性炎症与氧化应激、破骨细胞活性异常亢进、成骨细胞分化与功能受损,以及新生血管形成障碍。这些因素相互交织,形成不良循环,严重阻碍骨组织的自我修复能力。
近日,山东大学崔基炜教授和齐鲁医院王连雷教授合作团队开发了用于骨修复的金属-有机网络创可贴。该研究通过构建金属-有机网络材料,实现了抗炎、促血管生成及调节骨吸收/形成平衡的多重活性成分的协同递送,旨在从多维度重塑利于再生的局部微环境,为提升骨质疏松性骨折的修复效果提供了富有前景的新策略(图1)。
2025年12月4日,相关研究成果以“Engineering of Metal–Organic Networks as Band-Aid for the Repair of Osteoporotic Bone Fractures”为题发表在《ACS Nano》上。山东大学化学与化工学院崔基炜教授和齐鲁医院王连雷教授为该论文的共同通讯作者,山东大学化学与化工学院博士生魏绍银和齐鲁医院博士后尤云昊为该论文的共同第一作者。
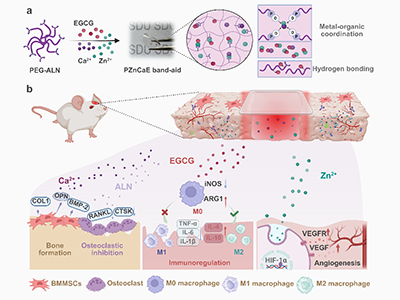
图1. PZnCaE创可贴治疗骨质疏松性骨折的示意图。(a)PZnCaE创可贴的制备流程图。(b)PZnCaE创可贴通过增强骨再生、抑制破骨细胞活性、调节免疫并促进血管生成的作用机制。
研究团队将抗骨质疏松经典药物阿仑膦酸钠(ALN)接枝到聚乙二醇(PEG)上,形成可降解的网络骨架,可持续释放ALN以精准抑制过度的破骨活性。随后利用锌离子(Zn2+)和钙离子(Ca2+)与ALN及天然多酚的配位作用,将多种功能组分整合到骨创可贴中,不仅增强了材料的力学性能,还能有效促进成骨分化和血管生成。多酚组分可消除氧化应激、缓解炎症,并将对修复有害的M1型巨噬细胞极化为有益的M2型,从而实现主动免疫调节。总体而言,这款创可贴不再是被动的填充物,而是一个能同时下达“抑制破骨、促进成骨、刺激血管、平息炎症”四大指令的主动调控平台。
该研究利用金属离子(Zn2+/Ca2+)与ALN、EGCG之间天然的配位作用,通过简单的混合、离心即可形成稳定的金属-有机网络。这种简易高效的制备方法避免了复杂的化学合成,具有良好的转化潜力。创可贴在降解过程中,能按需、持续地释放ALN、Zn2+、Ca2+和EGCG等多种活性成分,模拟了天然骨修复过程中不同阶段的生物学需求,实现了治疗因子的“精准投送”。研究超越了单纯的“成骨-破骨”平衡调控,深入到了骨免疫学前沿。通过EGCG调控巨噬细胞表型,将促炎的“破坏性”环境转化为抗炎的“修复性”环境,从更深层次解决了骨质疏松性愈合的核心障碍。
该研究通过系统的材料制备与表征、体外细胞实验及体内动物模型验证,全面评估了所研发的骨创可贴(PZnCaE)的效果(图2-7)。研究首先利用扫描电镜、X射线光电子能谱等表征手段证实了材料具有稳定的多孔结构和预期的化学相互作用。力学测试、溶胀与降解实验以及体外释放曲线表明,该材料具有良好的机械性能、可控的降解速率和ALN、Zn2+、Ca2+的持续释放能力(图2)。体外生物学实验进一步揭示骨创可贴具有良好的生物相容性,其提取物能显著促进骨髓间充质干细胞的成骨分化(ALP活性、钙结节形成及相关基因/蛋白表达上调),抑制破骨细胞分化(TRAP染色阳性减少及相关标志物下调),促进人脐静脉内皮细胞的迁移与成管(血管生成相关基因/蛋白表达增强),并能诱导巨噬细胞向抗炎的M2表型极化(CD206表达升高,炎症因子分泌减少)(图3-5)。在骨质疏松大鼠颅骨缺损模型中,植入PZnCaE创可贴8周后,Micro-CT三维重建及定量分析显示,其骨矿物质密度(BMD)、骨体积分数(BV/TV)等指标显著优于对照组及其他单组分材料组;组织学染色(H&E、Masson)观察到更完整的新骨与胶原形成;免疫荧光染色进一步证实缺损区域有更强的成骨(COL1、BMP2)、促血管生成(CD31)信号和更显著的M2型巨噬细胞(ARG1)聚集(图6-7)。该研究不仅提供了一种具临床转化潜力的骨修复材料,更展示了一种“材料设计-微环境调控-组织再生”协同策略。通过简单配位组装实现多重活性成分的时序释放,为代谢性骨病的修复材料开发提供了新思路。
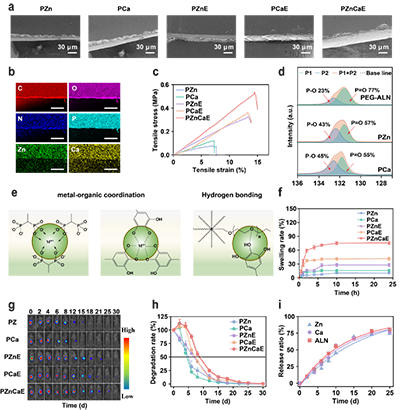
图2. PZnCaE创可贴的制备与理化表征。(a)不同类型创可贴的SEM图像。(b)PZnCaE创可贴的元素分布图。(c)PZn、PCa、PZnE、PCaE和PZnCaE创可贴的拉伸应力-应变曲线。(d)8-arm-PEG-ALN、PCa 和 PZn 创可贴的XPS谱图分析。(e)形成创可贴的相互作用示意图。(f)溶胀性能曲线。(g)体内降解荧光代表性图像。(h)体内定量降解曲线。(i)ALN、Zn2+和Ca2+的体外累积释放曲线。
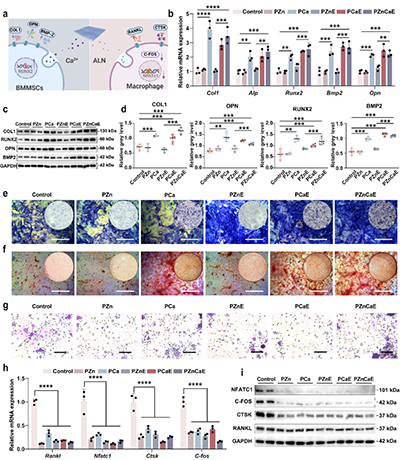
图3. PZnCaE创可贴调控BMMSCs的体外骨稳态行为。(a)PZnCaE创可贴释放Ca2+和ALN以促进成骨细胞分化和抑制破骨细胞活性的示意图。(b)成骨相关基因mRNA表达水平。(c,d)成骨相关蛋白表达水平及定量结果。(e)ALP染色结果。(f)茜素红S染色结果。(g)TRAP染色图像。(h)破骨相关基因mRNA的表达水平。(i)破骨相关蛋白的WB数据。
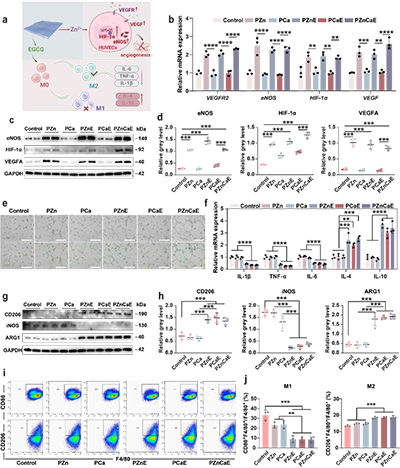
图4. PZnCaE创可贴对血管生成调控与巨噬细胞极化的体外调节研究。(a)PZnCaE创可贴调控血管生成和免疫反应的示意图。(b)血管相关基因mRNA表达水平。(c,d)血管相关蛋白表达水平及定量分析结果。(e)不同处理条件下HUVECs的血管生成能力。(f)炎症相关基因mRNA的表达水平。(g,h)不同处理后细胞中CD206、iNOS和ARG1的蛋白表达水平及定量结果。(i,j)巨噬细胞极化表型及定量结果。
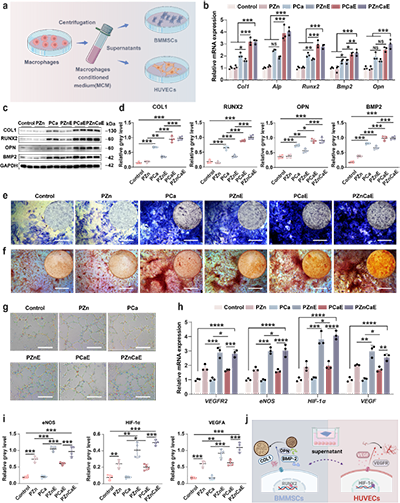
图5. 通过巨噬细胞极化调控成骨和血管生成的体外研究。(a)利用巨噬细胞极化调控成骨和血管生成的实验流程。(b)不同处理组成骨相关基因的表达水平。(c,d)成骨相关蛋白的表达水平及定量分析结果。(e,f)ALP和茜素红S染色。(g)体外成管能力。(h)不同处理组血管相关基因mRNA的表达水平。(i)不同处理组血管相关蛋白表达水平的定量结果。(j)利用巨噬细胞极化调控成骨和血管生成机制示意图。
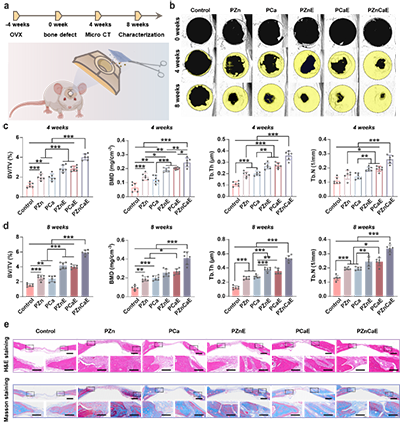
图6. PZnCaE创可贴调控骨质疏松骨愈合的体内评估。(a)使用PZnCaE创可贴治疗骨愈合的示意图。(b)移植后0、4和8周的三维Micro-CT图像。(c,d)第4和第8周Micro-CT定量分析。(e)第8周缺损区域H&E和Masson染色。
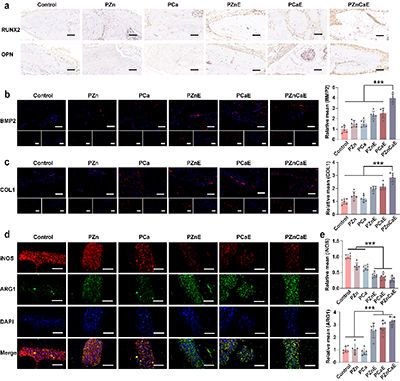
图7. 体内成骨作用、免疫反应及血管生成评估。(a)缺损区域 RUNX2 和 OPN 的免疫组化染色图像。(b,c)缺损区域 BMP2及(c,d)COL1的免疫荧光染色图像和定量分析。(f,g)缺损区域iNOS和ARG1的免疫荧光染色图像和定量分析。
综上所述,本研究成功开发了一种基于金属-有机配位网络的多功能骨修复支架。它不仅仅是一个结构替代物,更是一个能够动态响应并主动重塑局部病理微环境的“智能系统”。通过协同调控“破骨-成骨-血管-免疫”这四大关键环节,该创可贴有效逆转了骨质疏松性骨缺损的不利条件,实现了高质量的骨再生。这项工作为治疗骨质疏松性骨折及其他难愈性骨缺损提供了全新的材料设计思路。上述研究工作得到国家自然科学基金与国家重点研发计划等项目的资助和支持。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c15619
- 华东理工刘润辉教授课题组 AFM:基于仿生有机-无机互穿网络的增强型微球用于骨修复 2025-11-04
- 浙江大学赵玥绮团队 AFM: 仿生梯度结构水凝胶助力骨软骨修复 2025-10-15
- 纳米能源所王中林、蒲雄/北大口腔医院周永胜、李峥 Adv. Mater.:机械-离子电水凝胶通过内源性生物电刺激促进软骨再生 2025-09-23
- 东华大学沈明武研究员/史向阳教授团队:不对称含磷树状大分子递送菠萝蛋白酶用于骨关节炎的抗炎和软骨保护治疗 2025-06-13
- 浙大周民教授团队 Bioact. Mater.:微藻药物递送系统"降尿酸-抗炎-消化系统保护"三位一体协同用于痛风性关节炎的治疗 2025-06-04
- 西南医大口腔医院陶刚/黎春晖/蔡蕊团队:具有ROS触发药物释放特性的可注射水凝胶实现抗菌剂和抗炎纳米颗粒协同递送用于牙周炎治疗 2025-04-15
- 中科院深圳先进院赵晓丽/潘浩波/边少荃团队 CEJ:负载铈掺杂生物活性玻璃的可注射水凝胶利用活性氧消除功能治疗糖尿病慢性创面 2024-01-31
