植入相关感染(IAIs)是导致植入物植入失败的主要因素,特别是在糖尿病人群中更为常见。常见的治疗手段包括植入物的更换及术后的系统性抗生素治疗,这些方法不仅伴随风险,而且由于抗生素的广泛使用,导致了多药耐药性病原体的增加,使得治疗变得更加复杂。为应对这一挑战,四川大学华西口腔医院梁坤能副教授与邓怡研究员团队开发了一种创新的MXene/Ag3PO4@GOx(M/A@GOx bio-HJzyme)涂层技术,该技术通过水热处理和逐层沉积工艺,将涂层应用于惰性磺化聚醚醚酮(SP-M/A@G)植入物表面。该涂层不仅增强了成骨细胞在植入物表面的粘附与增殖,而且在808纳米近红外(NIR)光照射下,能够引发局部高温和活性氧(ROS)的产生,激活类芬顿反应和类漆酶的反应,耗竭糖尿病感染微环境中的谷胱甘肽(GSH),实现治疗效果的级联放大。
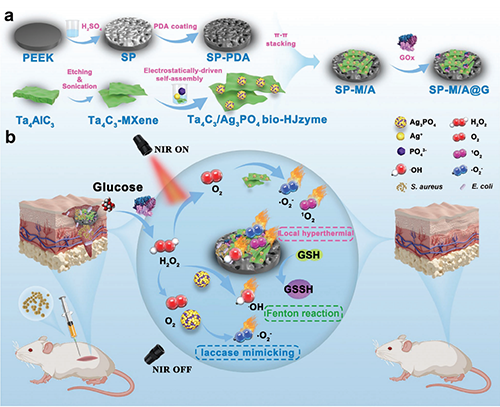
图1: a) SP-M/A@G 的制作示意图,b) 其用于治疗植入物相关感染的级联放大治疗机制。
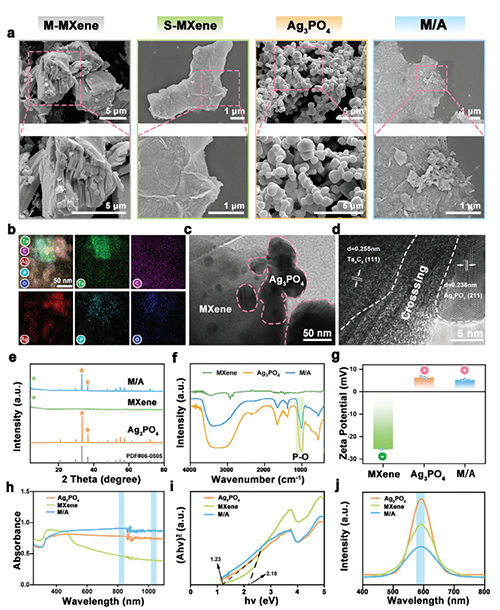
图2.:M/A异质结的表征。a) M-MXene、S-MXene、Ag3PO4和M/A异质结的SEM图像。b) M/A异质结的元素图。c) M/A异质结的TEM图像。d) M/A异质结的HR-TEM图像。e) MXene、Ag3PO4和M/A异质结的XRD图谱。f) MXene、Ag3PO4和M/A异质结的FTIR光谱。g) MXene、Ag3PO4和M/A异质结的Zeta电位。每组n = 3。h) 紫外-可见-近红外吸收光谱和相应的 i) MXene、Ag3PO4 和 M/A 异质结的Tauc图。j) MXene、Ag3PO4和M/A异质结的PL发射光谱。

图3: SP-M/A@G的表征。a) SP、SP-M/A和SP-M/A@G的SEM图像。b) SP-M/A@G的元素图。c) PEEK、SP、SP-M/A和SP-M/A@G的WCA变化,以及显示每个样品上液滴的相应图像。每个样本 n = 3。d) SP-MX和SP-M/A@G的XPS测量光谱,以及相应的高分辨率 e) Ta 4f、f) C 1s、g) O 1s XPS光谱。 h) SP-M/A@G的Ag 3d光谱。
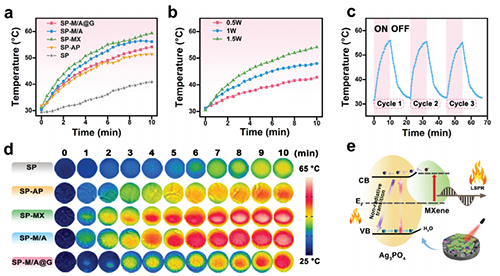
图4:光热特性。 a) 各种植入物在PBS中经受808 nm NIR (1.5 W cm?2) 的光热性能。b) 含 SP-M/A@G的PBS经过NIR(0.5、1.0、1.5 W cm?2)处理后的温度变化。 c) PBS中的 SP-M/A@G的光热循环经受三次开/关照射。d) 不同样品的实时近红外热图像。e) SP-M/A@G光热机理示意图。
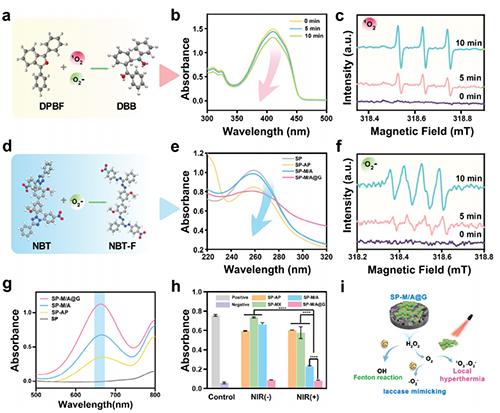
图5:光动力学和化学动力学特性。 a) 原理和 b) 表明DPBF耗尽的紫外可见吸收光谱。c) ESR光谱证明1O2的存在。 d) 原理和 e) 吸收光谱说明NBT还原。f) ESR谱显示·O2?的产生。g)反映TMB氧化的紫外可见吸收光谱。h) 不同处理后GSH溶液的OD值。每个样本 n = 3。i) SP-M/A@G 级联催化机制的示意图。
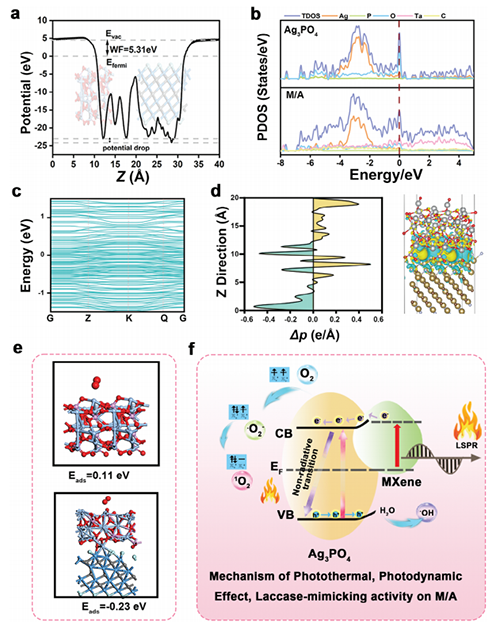
图6:M/A异质结的DFT理论计算:a) M/A界面沿z轴的静电电位变化。b) Ag3PO4和M/A界面的预计态密度(DOS)。c) M/A界面相应的带隙结构。d) 沿M/A系统z轴的平面平均差分电荷密度(Δρ),黄色区域表示电子积累,蓝色区域表示电子耗尽。e) Ag3PO4和 M/A上吸附O2后的结构表征。 f) 光动力和漆酶模拟活性的潜在机制的示意图。

图7:体外抗菌性能评估:该图显示的图像显示经过各种处理的 a) 金黄色葡萄球菌和 c) 大肠杆菌菌落,以及在近红外辐射10分钟后观察到的各自的 b、d) 抗菌效率。e) 显示不同处理后金黄色葡萄球菌的活/死活力图像,f) 相应的存活/死亡比率。g) 使用结晶紫染料可视化的生物膜的典型图像与 h) 相应的定量分析一起呈现。每组 n = 3;p值通过单向方差分析评估;**** 代表 p < 0.0001。

图8:体外抗菌特性分析:用不同样品处理的 a) 金黄色葡萄球菌和 b) 大肠杆菌的SEM形态,粉色箭头突出显示膜收缩。c) 细菌的TEM形态。不同处理后金黄色葡萄球菌和大肠杆菌中的 d) DNA和 e) 蛋白质泄漏。每组 n = 3;p值通过单向方差分析评估;**** 代表 p < 0.0001。

图9:体外生物相容性和成骨。通过 a) SEM和 c) CLSM评估SP、SP-M/A和SP-M/A@G支架上的MC3T3-E1细胞形态,伪足用红色星号标记。b) 24小时孵育后的活/死染色。通过 d) PT、e) APPT、f) FIB 和 g) TT 测定评估血液相容性。每个样本n = 3。h,i) ALP活性的定量和染色结果。每个样本n = 3(图 S19 中植入物的局部放大倍数,支持信息)。j, k) ARS的量化和染色结果(图 S19 中植入物的局部放大,支持信息)。每个样本n = 3。p值通过单向方差分析评估;* 代表 p < 0.05,*** 代表 p < 0.001,**** 代表 p < 0.0001。

图10:各种材料体内抗菌性能和伤口愈合功效的评价。a) 描绘模型制作和各种治疗管理的时间线的示意图。b) 植入物周围组织的近红外热图像和 c) 近红外光下植入物的温度变化。d)SP和SP-M/A@G处理后第1天和第7天的残留菌落,以及第7天的液体培养物,以及f,g)相应的细菌存活率。每组 n = 3。e) 感染伤口的照片。h)吉姆萨染色。红色箭头表示被感染的细菌。p值通过单向方差分析评估;*** 代表 p < 0.001,**** 代表 p < 0.0001。

图11:不同治疗组收集的伤口皮肤组织的组织学染色:a) H&E染色结果和 c) 不同治疗组皮下组织的Mason染色结果(绿色箭头和星号分别表示炎症小体和胶原沉积)。b) 中性粒细胞数和d) 来自大鼠血常规检查的白细胞数。e) 不同治疗组的TNF-α和IL-6的免疫组织化学染色结果。每个样本n = 3。p值通过单向方差分析评估;* 代表 p < 0.05,** 代表 p < 0.01,*** 代表 p < 0.001。
体外实验结果表明,这种多功能bio-HJzyme工程化的植入物展现出了显著的循环抗菌特性。体内评估进一步证实了其能够有效清除植入物及其周围组织上的感染病原体,并促进糖尿病感染皮肤的再生。本研究不仅提供了一种构建具有级联放大治疗能力的多功能植入物的革命性方法,也为治疗顽固性糖尿病相关植入感染(IAIs)提供了新策略。
该工作以题为“Multi-Functional Bio-HJzyme Engineered Polyetheretherketone Implant with Cascade-Amplification Therapeutic Capabilities Toward Intractable Implant-Associated Infections”发表于《Small》。文章第一作者为四川大学华西口腔医院2022级硕士研究生龚靖和四川大学化学工程学院特聘研究员赖双权,通讯作者为四川大学华西口腔医院的梁坤能副教授和四川大学化学工程学院邓怡研究员。本工作得到了国家自然科学基金、四川省科技厅项目的资金支持。
原文链接:https://doi.org/10.1002/smll.202409437











