构建体外模拟活组织和器官的模型具有巨大的潜力。这些模型可能会为创造用于组织再生的植入式生物材料带来突破并为有效的药物和毒性筛查提供平台。挑战在于开发能够模拟生理或病理条件复杂性的技术,包括活细胞、细胞外基质和专门的生物材料。自上而下的生物制造技术可以将细胞和生物材料操纵成预先确定的、空间排列的结构,从而制造出厘米大小的模型。这些模型能够捕捉组织和器官的基本结构细微差别和功能。在自上而下的方法中,无论是基于挤出的,还是基于光照的 3D 生物打印都很普遍。基于挤出的方法将充满细胞的“生物墨水”沉积在分层图案中以形成 3D 结构。这些方法适用于广泛的生物材料,但它们面临着低分辨率(≈200微米)和结构简单等局限性。尤其是在创建具有管腔的复杂自由曲面结构时,这种方法面临着挑战。
2024年4月8日,来自深圳大学微流控与软物质课题组在《Advanced Functional Materials》杂志发表题为“Multi-Material Digital Light Processing (DLP) Bioprinting of Heterogeneous Hydrogel Constructs with Perfusable Networks”的研究论文,提出了利用生物墨水PEGDA-AAm和多材料DLP生物打印来开发多组分、多模量、充满细胞的水凝胶构建体。这些结构具有异质的机械性能、复杂的结构和精确设计的表面微观结构。
1.使用多材料DLP打印并将AAm和PEGDA分别作为水凝胶的软硬结构组分混合来制备水凝胶前体。

图1 用作体外模型的水凝胶构建体的示意图
2.PEGDA-AAm生物墨水的性能表征
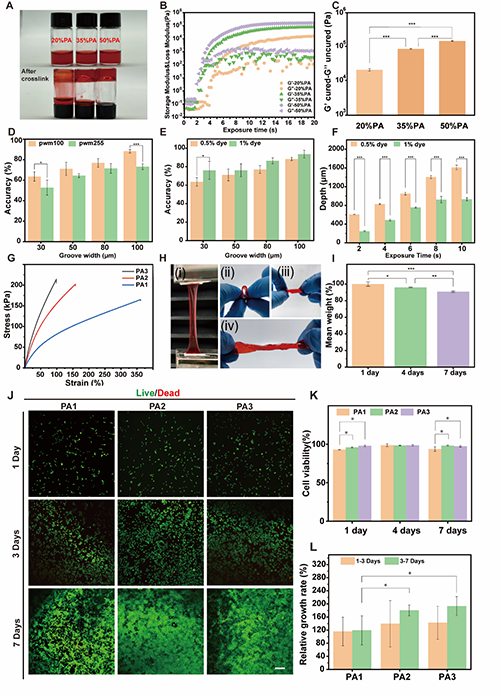
生物墨水的凝胶化时间(Tgel)显著影响其可打印性。对25、35和50wt%浓度的PA生物墨水进行照射交联10秒。结果显示,低浓度的PA生物墨水仅部分凝胶化,当瓶子倒置时未固化的墨水沿瓶壁流下。相反,50wt%浓度的PA生物墨水显示完全凝胶和固化,几乎没有墨水流动。这表明50wt%的PA生物墨水更适合创建复杂的结构(图2A)。
为了定量确定PEGDA-AAm(PA)生物墨水的凝胶化时间(Tgel),对其光流变性能进行了表征。当储存模量(G'')与损耗模量(G'''')相匹配时,确定了Tgel。将PA生物墨水的单体浓度提高会导致Tgel降至2.75秒(图2B),这比通常需要几十秒的GelMA的凝胶化时间要快得多。
在DLP 3D生物打印中,优化打印分辨率涉及调节未固化墨水的粘度和固化后水凝胶的刚度。这对确保固化结构与残留液体墨水之间的清晰分离至关重要。这些属性的相互作用通过固化后水凝胶的G''和未固化墨水的G''''来定量捕捉。打印分辨率的有效性由这些模量的差异(ΔG)决定。比较不同单体浓度的PA生物墨水的ΔG,发现50%单体浓度的PA生物墨水的ΔG要高一个数量级(图2C)。鉴于其较短的Tgel和较高的ΔG,50%单体浓度的PA生物墨水更有希望增强可打印性,成为了后续实验的首选。
为了优化曝光参数,研究者们探索了曝光参数对XY平面和Z方向的打印分辨率的影响。研究者发现,使用较高的光能来打印100 μm宽的凹槽会导致过固化。相比之下,较低的光能使得相同宽度的凹槽的打印精度提高到了约90%(图2D)。在较高的光能水平下,精度降低的原因是因为在没有光吸收剂的情况下,生物墨水中的光散射增加,导致凹槽变窄。对于30 μm宽的凹槽,在较高和较低的光能下的打印精度分别为53%和60%。在创建细微的平面结构时,可通过调整光强度和曝光时间从而精确控制所得到的打印宽度。
向生物墨水中添加光吸收剂可以有效提高打印精度。光吸收剂均匀混合到墨水中后可降低不同区域的光能。它们吸收大部分散射光,显著减少了不必要的固化,从而提高了打印精度。然而,虽然较高浓度的光吸收剂可以增加精度,但也可能导致固化层变薄,影响打印效率。研究者发现,将1%的光吸收剂添加到PA生物墨水中可以实现最佳平衡,既确保了高打印精度,又保持了效率(图2E,F)。
在PA生物墨水中,研究者成功地将得到的PEGDA-AAm水凝胶的弹性模量调整在数十到数百kPa的范围内。仅通过控制单体浓度和PEGDA:AAm(PA)比例来实现这一点。具有2%、5%和10%比例的特定PA墨水被分别命名为PA1、PA2和PA3。这些水凝胶的弹性模量在45至210 kPa之间,应变范围从90%到350%不等(如图2G,H所示)。PA水凝胶在水环境中表现出了良好的结构完整性和尺寸稳定性,使其成为体外模型建设中的理想支架材料。例如,PA1水凝胶在浸泡在水中7天后的重量几乎保持不变,这意味着PA1水凝胶没有水解(图2I)。这种稳定性是由于PA水凝胶与双网络的强化学交联,确保了水凝胶的结构在较长时间内保持完整,即使在PBS溶液中也是如此。鉴于这些性质,PA水凝胶可以用于构建各种组织的模型。
3.使用PA生物墨水构建单组分体外组织模型
为展示DLP生物打印在制备具有可灌注网络的细胞载体水凝胶结构方面的潜力,研究者创建了微流控芯片,其中包含直通和气管状通道。为验证结构内部成功打印了空腔通道,将显示蓝色荧光的NIH-3T3细胞注入到这些通道中(图3A)。研究者展示了两种不同水凝胶构建物的成功制备,其中包含嵌入的空心结构(图3B,E)。混合到生物墨水中的Hela-GFP细胞在整个水凝胶中均匀分布,而注入的NIH-3T3细胞充满了空心通道,它们的蓝色荧光清晰地勾勒出这些嵌入式微通道。绿色荧光的Hela-GFP细胞与蓝色荧光的NIH-3T3细胞之间的清晰区别(图3C,D,F,G),每个细胞都限定在特定区域。这些结果表明,在DLP打印中使用的PA生物墨水非常有效,可以制造具有精确灌注通道的模型,确保水凝胶构建物中特定细胞的均匀分布。

图3 充满细胞的PA水凝胶构建体具有可灌注网络和工程表面形貌。
4.使用PA生物墨水构建单组分体外组织模型
在组织工程中,复制肝小叶、皮肤和软骨等组织和器官固有的多样化机械模量是一个挑战。研究者利用多材料DLP技术和多功能PA生物墨水将具有不同机械特性的组件可靠地组装成单一的体外模型。例如,PA1和PA2水凝胶通过在它们的界面处固化未固化的PA生物墨水来实现它们之间的粘接(图4A)。结果表明,将两种尺寸相同但配方不同的水凝胶组合在一起,得到了具有适度且平衡的机械特性的水凝胶(图4B)。此后,在同一平面上打印PA1和PA3生物墨水的预设计图案,并允许它们相互连接(图4C)。总的来说,这种异质结构的整体机械性能取决于不同机械特性的不同组分如何配置和连接在一起。良好设计的结构布局可以确保应力均匀分布或指向更坚硬的区域,增强结构完整性和机械稳健性。
为了展示多材料DLP在制造与生物相关的异质组织模型方面的能力,研究者开发了一个简化的肝小叶模型(图4D),其中蓝色PA3和红色PA1生物墨水分别代表肝窦和肝板。由于NIH-3T3和Hela-GFP细胞在生物材料中的广泛应用,研究者选择了这两种细胞作为代表性例子。这些细胞类型被合并到了PA1和PA3生物墨水中,形成了一个平面的异质生物结构。这种成功创建的多组分模型展示了该方法在研究水凝胶材料中的细胞相互作用方面的潜力。这些材料在细胞类型和机械特性上都有差异,满足了不同组织模量的需求。
为了将对异质性的探索扩展到XY平面之外,并展示沿Z轴构建异质结构的可行性,研究者还设计了一个涉及具有TPMS拓扑结构的管状结构的实验。这个结构被分成了三个不同的部分,每个部分都使用具有不同模量的PA1、PA2和PA3生物墨水制作(图4G)。对这个集成样品进行的应力加载测试证实了不同组分在具有TPMS特征的中空管中的有效融合,展示了沿Z轴方向的异质模量。这种成功的集成展示了该方法在以3D方式创建复杂的多模量结构方面的潜力。
作为概念验证,研究者利用多组分、多模量水凝胶结构并配有表面微结构来研究细胞行为。众所周知,肿瘤细胞的粘附、增殖、迁移和侵袭行为与材料基质的特性密切相关。为了研究肿瘤细胞的优先迁移和生长,将Hela-GFP细胞引入到多组分TPMS结构中。PA1水凝胶上的Hela-GFP细胞在扩展方面比PA2和PA3部分上的细胞更加广泛,显示出与侵袭性侵袭行为相关的开放式、纺锤形态。相反,PA2、PA3水凝胶上的Hela-GFP细胞倾向于在凹陷区域内聚集,主要呈现圆形,几乎没有扩散迹象(图4J)。因此,模量约为40 kPa的水凝胶结构有利于宫颈癌肿瘤细胞的迁移和侵袭,而模量较高的水凝胶鼓励细胞聚集。本研究开发的模量差异化的异质结构提供了一种多功能方法,用于研究基质模量对各种细胞行为的影响。此外,这些结构还有望用于共培养系统,以研究异质细胞群体之间的相互作用,这对于增强工程组织的性能至关重要。

图4 充满细胞的多材料异质水凝胶构建体。
本文的第一作者是深圳大学硕士生杨铭,共同通讯作者是深圳大学孟思副研究员和孔湉湉教授。本研究受到了国家自然科学基金、广东省自然科学基金等项目的支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202316456
- 中科院动物所顾奇团队 Adv. Mater.:研发 CAMP 冷冻保存生物墨水 - 实现黏附细胞 “即取即用” 3D 生物打印 2026-04-03
- 广东医大赵名艳、暨大刘明贤 Compos. Sci. Technol.:3D打印构建海藻酸钠/埃洛石复合陶瓷支架用于骨再生 2024-03-11
- 哈佛医学院Y. Shrike Zhang教授课题组 Adv. Mater.: 脱细胞基质生物墨水的快速体积生物打印 2024-01-25
- UCSD蔡盛强教授团队《Sci. Adv.》:超灵敏且强韧的力致发光活性软材料 2023-10-23
- 香港城市大学吕坚教授 Adv. Mater.:多材料3D和4D生物打印异质结构用于组织工程 2023-09-26
- 东华大学何创龙教授团队《Adv. Funct. Mater.》:3D生物打印支架重塑神经调节微环境促进骨再生 2023-06-02
- 多伦多大学Eugenia Kumacheva团队 AFM:AI赋能多组分复合水凝胶逆向设计-精准定制仿生粘弹性网络 2026-05-14
