宁波大学陈重一课题组 Biomacromolecules:手性调控聚氨基酸的簇发光
2024-03-04 来源:高分子科技
与传统的有机发光材料相比,簇发光高分子表现出较好的生物相容性和生物降解性。但是簇发光高分子的低发射效率限制了其在生物成像等领域中的应用。聚氨基酸因其具有良好的生物相容性和生物可降解性,被广泛应用于生物医学领域。在前期研究中,他们发现手性不仅能影响聚氨基酸材料的构筑,并且可以调控其力学性能和生物响应行为(J. Am. Chem. Soc. 2019, 141, 8680; Chem. Mater. 2020, 32, 1153; Macromolecules 2022, 55, 3801; Biomacromolecules 2023, 24, 3283)。
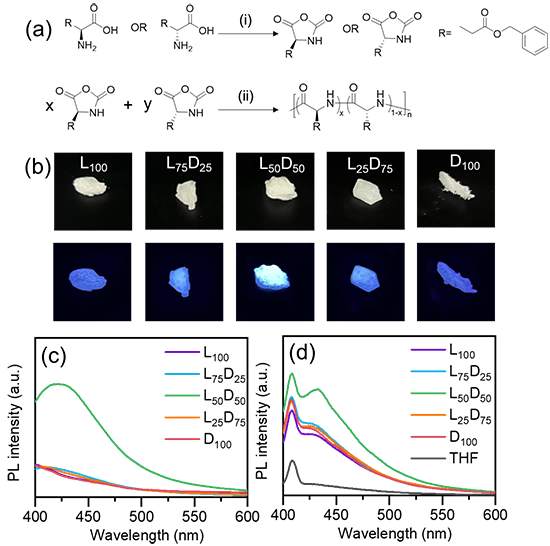
图1 不同手性聚氨基酸的合成与荧光强度。
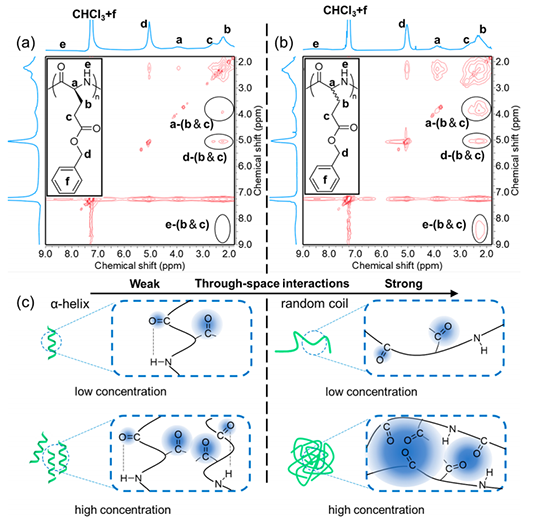
图2 不同手性聚氨基酸的簇发光机理
他们合成了一系列不同手性的聚氨基酸,发现了聚氨基酸的手性在簇发光中起到的关键作用。聚氨基酸的簇发光来自于n-π*空间相互作用,而相反手性单体的引入,导致聚氨基酸的α螺旋结构逐渐转变为无规线团结构。无规线团结构的灵活性使得聚氨基酸链上的羰基可以形成更多的n-π*空间相互作用,从而产生更强的荧光。通过加入尿素和三氟乙酸破坏聚氨基酸的螺旋结构和聚集,进一步证明了α螺旋-无规线团的转变与荧光强度的关系。本研究为发光多肽/聚氨基酸材料的开发提供了新的设计思路。
原文链接:https://pubs.acs.org/doi/abs/10.1021/acs.biomac.3c01328
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 郑州大学化学学院张伟教授团队招聘教师、博士后 - 高分子合成、手性高分子、超分子组装和功能高分子材料、DFT和分子动力学计算合成/组装 2026-03-17
- 苏大/郑大张伟、淮师缪腾飞、郑大贺子翔 Angew:给体-受体(D-A)效应指导聚合物聚集态超分子手性传递路径 2026-02-09
- 浙江大学凌君教授课题组 Macromolecules:无金属催化剂催化两仪聚合构筑聚氨基酸热塑性弹性体 2026-05-03
- 宁波大学陈重一课题组 Macromolecules:基于可编程α-螺旋的多重形状记忆聚氨基酸材料 2026-03-10
- 长春应化所陈学思、丁建勋团队 JACS:一种肿瘤选择性自组装聚氨基酸网络通过微囊泡分裂扩增诱导级联旁观者细胞毒性 2026-01-12
- 中山大学顾林课题组 CEJ:基于簇发光标记,实现环氧防腐涂层中氮化硼纳米片分散的原位三维可视化与定量分析 2025-08-22
