肿瘤耐药是临床化疗效果受限的重要原因之一。化疗药物到达癌细胞需经过复杂的运输步骤,不仅要克服体循环中的生物屏障,还需克服肿瘤微环境(TME)内在的多重阻碍。在此期间,药物容易被机体清除,并产生脱靶效应,作用于正常组织催生副作用。同时,TME通过代谢重编程、免疫检查点相互作用、免疫抑制型细胞群富集等多种机制,使得许多化疗药物催生的免疫反应失活,阻碍免疫细胞识别和杀伤,使得疗效不尽如人意。即使药物最终抵达癌细胞内部,癌细胞还会通过一些耐药保护机制阻滞药物发挥效果,如耐药癌细胞表面会表达药物外排泵P-糖蛋白(P-gp)将化疗药物外排。因此,开发克服肿瘤耐药性和 TME 免疫抑制的新型给药策略十分重要。
纳米载体可用于延长传统治疗剂的血液循环时间,提高药物生物利用度,促进其肿瘤蓄积,从而增强抗肿瘤疗效。在众多纳米载体材料中,纳米凝胶由于其灵活的网络设计、良好的生物相容性、优异的载药量、药物释放可控等性能,在肿瘤药物递送中被广泛应用。树状大分子作为一类3D结构的大分子材料,由于其独特的结构、理化特性,也被视为一类极具潜力的载体材料。树状大分子外围能共价修饰药物或标记活性分子,其内部也能用于负载药物及功能性纳米颗粒,因而被广泛应用于肿瘤纳米药物及诊疗试剂的构建。合成基于树状大分子的纳米凝胶,有望获得兼具水凝胶和树状大分子两者优势的纳米递送平台。

团队选用CT26小鼠结直肠癌细胞进行体外实验评价。结果表明,5-FU在CT26细胞中存在一定的耐受现象,但载药凝胶FDNG克服了这一问题(图2a)。进一步实验显示,DNG在被癌细胞内吞后能够在胞内滞留较长时间(图2b-d),且能下调细胞表面的药物外排泵P-gp的表达(图2e-f),有助于克服癌细胞中P-gp介导的耐药性。通过细胞周期实验发现,相较于自由的5-FU,癌细胞在经过FDNG或共递送凝胶体系(FDNG/cGAMP)处理后,G1-S细胞周期阻滞效果更佳(图3a-b)。

图2.(a)CT26 细胞经不同浓度5-FU和FDNG 处理 24 小时后的细胞活力;(b)流式细胞术检测不同培养时间后CT26细胞中FDNG-Cy5.5的滞留情况和(c)平均荧光强度;(d)FDNG-Cy5.5与细胞在不同培养时间段后细胞的共聚焦显微镜照片(比例尺= 20 μm);(e)不同浓度5-FU和FDNG处理24小时后CT26细胞中P-gp表达的Western印迹分析和(f)定量结果。

图3.(a)CT26 细胞经不同材料处理24小时后的细胞周期流式检测和(b)各周期定量结果;(c)体外检测树突细胞/巨噬细胞免疫激活效果的Transwell系统示意图;(d)上室CT26细胞分泌IFN-β的ELISA检测结果;不同材料处理后下室(e)CD80+CD86+树突细胞和(f)M1/M2巨噬细胞的流式检测定量结果;(g-j)不同材料处理后下室树突细胞表面递呈MHC-I/II的流式细胞检测结果。
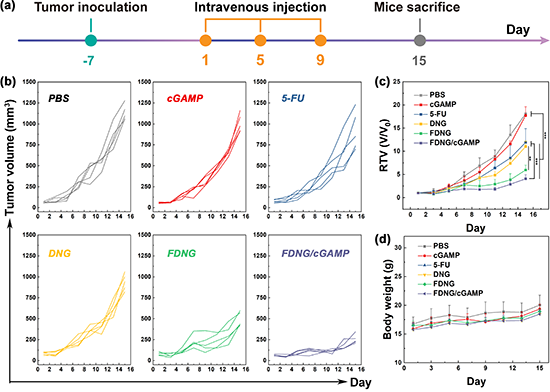
图4.(a)体内抗肿瘤评价流程示意图;(b)经不同材料治疗后15 天中小鼠的个体肿瘤生长曲线、(c)相对肿瘤体积变化曲线和(d)体重变化趋势。
进一步研究小鼠体内免疫响应的效果发现,FDNG/cGAMP治疗组小鼠脾脏中的CD8+ T细胞分布最多(图5a),免疫抑制型Treg细胞分布最少(图5b),且CD8+/CD4+比例最高(图5c)。同时,FDNG/cGAMP治疗组小鼠的肿瘤部位的CD8+ T 细胞浸润(图5d)和M1型巨噬细胞分布也最多(见原文补充数据)。小鼠血清的ELISA结果也显示FDNG/cGAMP治疗后,相应抗肿瘤细胞因子TNF-α(图5e)、IFN-γ(图5f)、IL-6(图5g)和IFN-β(图5h)含量最高。

图5. 15天体内实验周期结束后不同实验组小鼠脾脏中(a)CD8+ T细胞和(b)Tregs、(c)CD8+/CD4+比例以及(d)肿瘤中CD8+ T细胞比例;治疗结束后小鼠血清中(e)TNF-α、(f)IFN-γ、(g)IL-6和(h)IFN-β的ELISA检测结果;(i)荷瘤小鼠静脉注射FDNG-Cy5.5/cGAMP和Cy5.5后不同时间点的体内荧光成像结果和(j)72小时后主要器官和肿瘤的离体荧光图像以及(k)平均辐射率(1:心脏;2:肝脏;3:脾脏;4:肺脏;5:肾脏;6:肿瘤)。
论文链接:https://doi.org/10.1021/acsmaterialslett.3c01426
- 东华大学沈明武研究员/史向阳教授团队 AFM:仿生外泌体伪装的pH响应型树状大分子纳米凝胶作为疫苗通过重编程多种细胞类型治疗胰腺癌 2026-02-20
- 东华大学沈明武研究员/史向阳教授团队:不对称含磷树状大分子递送菠萝蛋白酶用于骨关节炎的抗炎和软骨保护治疗 2025-06-13
- 东华大学史向阳教授团队:外泌体包裹的响应性树状大分子纳米凝胶可实现急性肺损伤的免疫调节和抗氧化联合治疗 2025-05-15
- 华科大李子福教授 Nat. Commun.:相变纳米凝胶赋能生物医学新突破 2025-12-22
- 山东大学栾玉霞教授团队 Nat. Nanotech.:发现解决CAR-T细胞疗法实体瘤疗效受限的有效方法 2025-05-20
- 东华大学史向阳/沈明武团队 Acta Biomater.:仿生含铜纳米凝胶用于磁共振成像引导的肿瘤化疗-化学动力学治疗-免疫治疗 2024-10-03
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
