细胞疗法,指将特定细胞作为活性试剂注入体内以替代受损组织、调节生物功能和抵御疾病,是一种极具前景的新型治疗策略,在近年来引起了广泛关注。为了充分发挥细胞疗法的效果,细胞递送策略至关重要。传统的全身性给细胞策略可一次性注射大量细胞,但其靶向性差,递送途中绝大部分细胞会遗失而无法到达目标病灶,导致细胞疗法效率很低,甚至还可能因脱靶细胞而引发严重后遗症。因此,开发安全、高效的细胞靶向递送策略对细胞疗法的开发意义重大。
微型机器人技术的兴起为靶向细胞递送提供了新的可能。由于尺寸小、运动主动、灵活度高的特性,微型机器人能够在常规医疗手段难以到达的狭小闭塞区域运动,有望作为一种细胞载具,主动高效地将细胞递送至目标病灶。在已开发的众多种类的微型机器人中,磁控微型机器人因其驱动磁场易调制、对生物组织穿透性强且无危害,在细胞递送领域得到了广泛研究。其往往采用微纳制造和化学合成的方法制备负载细胞的支架结构,再通过表面蒸镀磁性薄膜或内部掺杂磁性颗粒,从而构建可响应外部磁场控制的主动式细胞递送微型机器人。但是,微型机器人的细胞功能和磁控功能存在一个不容忽视的矛盾。为了适应生物体内复杂动态的生物环境,微型机器人的运动和控制能力要足够强,这就需要在微型机器人中添加大量的磁性材料来实现。过度的磁性掺杂一方面会明显影响其细胞活性,甚至导致细胞无法黏附,另一个方面则会造成体内滞留过量磁性材料,引发潜在的生物毒性。假如微型机器人只添加少量磁性物质而满足其递送细胞的细胞功能性和生物安全性,其在生物体内的可控导航则成为了一个巨大难题。因此,目前亟需开发兼具优异磁控驱动能力和生物医学功能的细胞递送微型机器人。


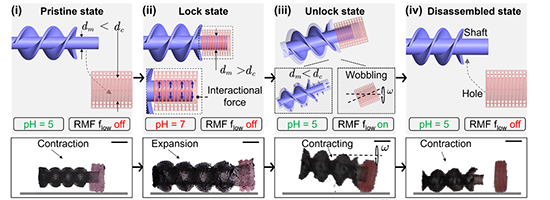
图3. 模块化微型机器人的可控组装与拆卸

原文链接:https://www.science.org/doi/10.1126/sciadv.adj0883
- 浙大杨赓研究员 Adv. Mater.:机器学习增强的模块化离子皮肤实现人机交互的宽谱多模态解耦 2025-07-26
- 哈佛医学院Y. Shrike Zhang教授团队 PNAS:闭环模块化精确控氧多器官芯片系统 2024-11-15
- 北京大学韩梦迪教授团队 Sci. Adv.:三维柔性模块化的电子皮肤 2024-08-23
- 西安交大唐敬达课题组《ACS AMI》: 三相态磁驱动微型机器人 2024-01-25
- 哈工大李天龙、郑大张伟伟《Small》:受变形虫启发的毒液微型机器人 2023-07-03
- 斯坦福赵芮可教授《Nat. Commun.》:人体内的体操高手 - 无线两栖送药机器人 2022-06-17
