高尿酸血症(hyperuricemia)是指由嘌呤代谢紊乱(或)尿酸排泄障碍所导致血尿酸增高,细胞外液尿酸盐呈现超饱和的状态。长期尿酸过高会引发痛风,增加心脑血管疾病、代谢综合征及肾脏疾病病人的死亡率,同时血尿酸水平与动脉粥样硬化、高血压、脑卒和糖尿病等的发生率呈正相关关系。目前治疗或缓解高尿酸血症的药物较少,主要包括:1)促进尿酸排泄药物—通过干扰肾小管对尿酸的吸收而增加尿酸排泄,常见药物包括苯溴马隆、丙璜舒、磺吡酮等;2)阻断尿酸合成类药物—通过抑制黄嘌呤氧化酶的活性,阻断尿酸的产生路径,从而使嘌呤分解的产物以黄嘌呤和次嘌呤形式排出,具体药物包括别嘌呤醇、非布索坦、托匹司他等。但上述药物仍存在一定程度的副作用,包括药物不良反应和累积的肝脏毒性等。
尿酸酶(UOX)是一种高效的氧化酶,其可以特异性催化尿酸(UA)转化为水溶性更高且更易排出的尿囊素。目前基于UOX的治疗策略是治疗高尿酸血症的有效方法。但是UOX具有许多固有的缺点,如稳定性差、直接施用易被体内系统清除等。另外尿酸降解过程中有毒中间体(H2O2)的积累会导致严重的毒副作用。目前人们探索出许多递送尿酸酶的方案来克服上述限制(如PEG、脂质体、聚两性离子聚合物等),然而这些策略并不能保证外源性UOX在体内持久而快速地发挥效能。

图1. 基于血红细胞和MOF-级联酶(UOX-CAT)的人工生物杂化体用于治疗高尿酸血症的示意图
针对以上挑战,华南理工大学生物科学与工程学院朱伟教授团队基于纳米粒子模块化组装的思想,开发出了全新的血红细胞药物载体用于高尿酸血症的治疗(图1)。以功能纳米颗粒作为构筑基元,通过模块化组装方式将其可控组装于血红细胞表面形成全新装甲红细胞生物杂化体。除了通过纳米材料模块化组装来增强红细胞抵抗性,封装在ZIF-8纳米颗粒中的级联酶(UOX-CAT)也可以快速且持久地降低血液尿酸水平。当静脉注射装甲红细胞生物杂化体后,血液中的尿酸小分子可以接触到红细胞表面,并在UOX-CAT级联催化反应中进行有效降解,而红细胞的周围高氧环境可以进一步加速UA降解。同时,受益于 ZIF-8 的封装和对红细胞的搭便车效应,封装的UOX将避免体内蛋白酶的快速降解和系统清除,从而有效保持其内在活性,实现持久催化。

图2. 血红细胞和MOF-级联酶的人工生物杂化体提升UOX的稳定性

图3. 血红细胞和MOF-级联酶的人工生物杂化体保持有红细胞原有结构和功能
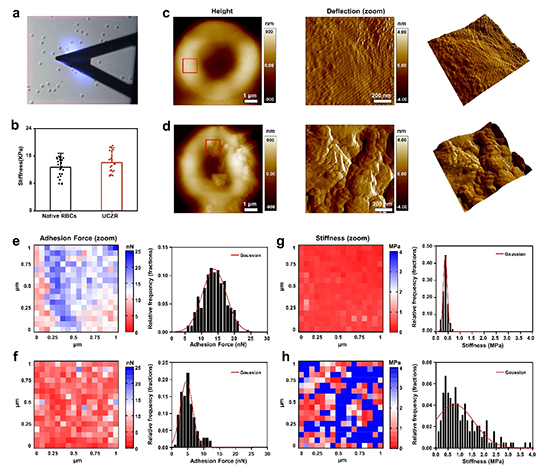
图4. 血红细胞和MOF-级联酶的人工生物杂化体机械性能表征
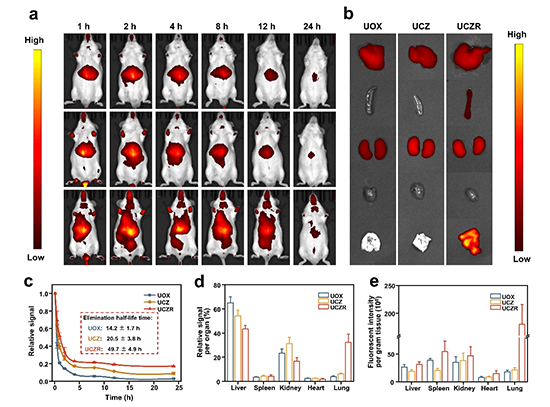

图6. 血红细胞和MOF-级联酶的人工生物杂化体的体内药效和毒性的评估
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202305126
- 吉林大学钱虎军教授团队 PRL:单链纳米粒子突破高分子材料“强度-韧性-加工性”三难困境 2025-10-15
- 浙江大学王立教授、俞豪杰教授团队 JCIS:用于安全磁共振成像和刺激响应药物递送的纳米粒子 2025-09-09
- 华工殷盼超/广工尹家福团队 Nano Lett.:软纳米粒子多时空动力学解析 2025-08-21
- 中科院宁波材料所陈涛、张佳玮研究员:基于动态硼酸酯键的水凝胶的模块化组装和智能形变 2019-05-05
- 四川大学何斌/蒲雨吉 ACS Nano:高分子化丁酸纳米平台治疗肠炎 2023-12-24
- 长期有效 | 西南交大周绍兵教授团队诚招博士、推免硕士 - 材料、生物医学工程 2023-09-23
- 浙大姚克教授团队《Adv. Drug Deliver. Rev.》综述:纳米药物载体在眼病治疗中的研究现状与展望 2023-03-17
