发生于深创口、大范围创面或特殊人群(如糖尿病患者等)上的由细菌造成的严重伤口感染是临床上经常需要应对的情况,一般采用抗生素对其进行治疗。然而,由于抗生素耐药性不断上升、新抗生素研发困难、许多抗生素对格兰氏阴性菌效果较差等诸多因素,抗生素效果不足的情况愈发普遍,因此我们迫切需要开发新的抗菌策略来应对这些挑战。抗菌拟肽(AMPM)因具有广谱抗菌活性、极好的蛋白酶稳定性、容易大规模合成且不易产生耐药性等特点而被广泛关注。然而,抗菌拟肽由于其非选择性破膜机制所带来的细胞毒性问题,目前鲜少被应用于临床实验中。
湖南大学白玉罡教授课题组此前通过引入额外的原核靶向DNA结合机制及调节抗菌拟肽的交替两亲性显著提高了抗菌拟肽的抗菌性能及选择性杀灭能力。

为了进一步提高抗菌拟肽的血液相容性,这项研究提出了一种新策略:两亲性掩蔽策略,即使用另一种被FDA批准的功能聚合物Pluronic F-127(PF127)与已建立的AMPM(PT-b1)复合,以部分和可逆地“中和”AMPM的膜破坏能力,从而提高其治疗指数(TI)。该策略对具有多重抗菌机制的AMPMs极为有用,因为PF127只减弱AMPM造成真核细胞毒性的破膜机制,而不抑制该AMPM的其他抗菌机制。此外,PF127 与PT-b1复合后可以形成可注射和可吸收的温敏抗菌水凝胶,该水凝胶可以有效促进伤口愈合并抑制细菌感染引发的炎症。相关工作以” Improving the Hemocompatibility of Antimicrobial Peptidomimetics through Amphiphilicity Masking Using a Secondary Amphiphilic Polymer”为题发表在《Advanced Healthcare Materials》杂志上。

图1 PT-b1的抗菌机理、耐药性及拯救哺乳动物细胞效果测试
这项研究基于喷他脒丁类似结构设计合成了一系列寡聚脒。由于喷他脒丁能与DNA的小凹槽结合来抑制DNA的合成,并通过各种方法干扰DNA中的关键功能,因此该喷他脒丁类似结构的寡聚物库中的抗菌拟肽不仅可以通过静电与疏水相互作用对细菌膜造成损伤(图1a),还能选择性只结合细菌DNA,而不对哺乳动物细胞造成损伤(图1d和图1e)。同时,由于以上两种选择性机制使得PT-b1可在细菌体内产生较多的ROS,而在细胞体内则几乎检测不到(图1g)。通过多重抗菌机理结合杀菌,使得细菌对PT-b1的耐药性很难产生(图1h)。这种抗耐药性及选择性杀灭的优势同样也体现在细菌和 NIH/3T3 细胞的共培养模型中(图1i和图1j),若在感染过程中未使用抗菌剂或仅使用已产生耐药性的抗菌剂庆大霉素进行治疗,A. baumannii-1可在24小时内快速繁殖,并最终杀死几乎所有细胞(细胞活力 <20%)。然而,当使用8 μg/mL PT-b1对感染细菌的细胞进行治疗时,所有细菌都被杀死且细胞可以维持其正常形态,同时也能使细胞的存活率提高至约60%。

图2 PF127可以掩蔽PT-b1的两亲性并提高其血液相容性
为了找到一种更加通用而不是基于结构修饰的方法来进一步提高抗菌拟肽的血液相容性,作者将PT-b1与二级两亲性功能聚合物PF127复合得到了一种对温度敏感的水凝胶PF127-PT-b1,并对其血液相容性及体内外抗菌性能进行了一系列的表征(图2)。实验结果表明,PF127的复合作用可以部分掩盖PT-b1的两亲性,降低其对细胞膜的破坏作用,而对PT-b1的抗菌活性没有影响,从而提高了PT-b1的治疗指数。
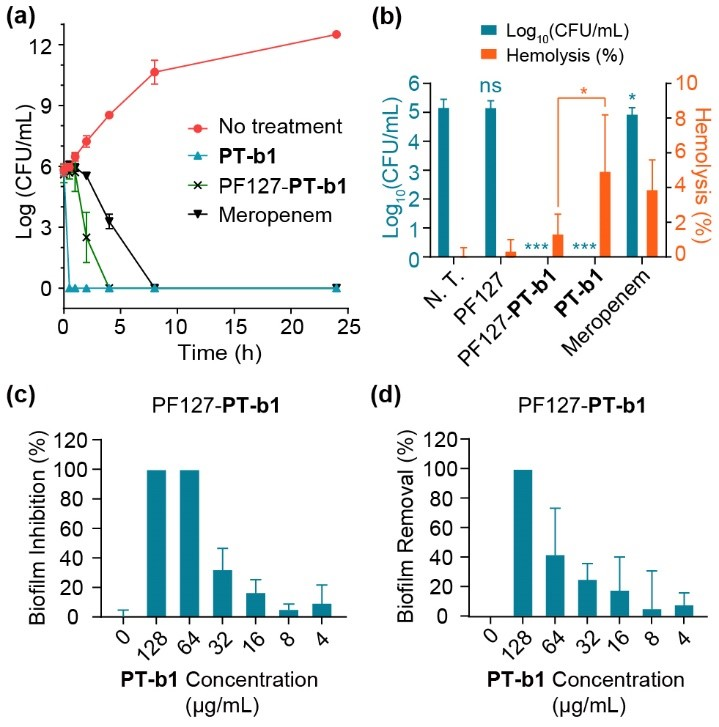
图3 PF127-PT-b1的杀菌动力学、拯救血细胞效果及抗生物膜效果测试
PT-b1和PF127-PT-b1具有快速的杀菌动力学。虽然PF127-PT-b1的杀菌速度在一定程度上被两亲性分子PF127减慢了,但与传统抗生素美罗培南相比,该水凝胶体系仍具有一定的优势(图3a)。在菌血症模型中,PF127-PT-b1可选择性杀死全部的耐药细菌A. baumannii-1,而几乎不造成血细胞裂解(图3b),相较于PT-b1引起5%的溶血率有很好的提升,这在实际应用到体内模型中时可能会造成较大影响。并且,PF127-PT-b1在与PT-b1可以抑制生物膜形成,甚至对已形成生物膜也有较好的清除作用(图3c和图3d)。由于PF127-PT-b1的HC5 > 1000 μg/mL,而PT-b1的HC5低至66 μg/mL,因此PF127与PT-b1的复合物在此研究中表现出更明显的优势。
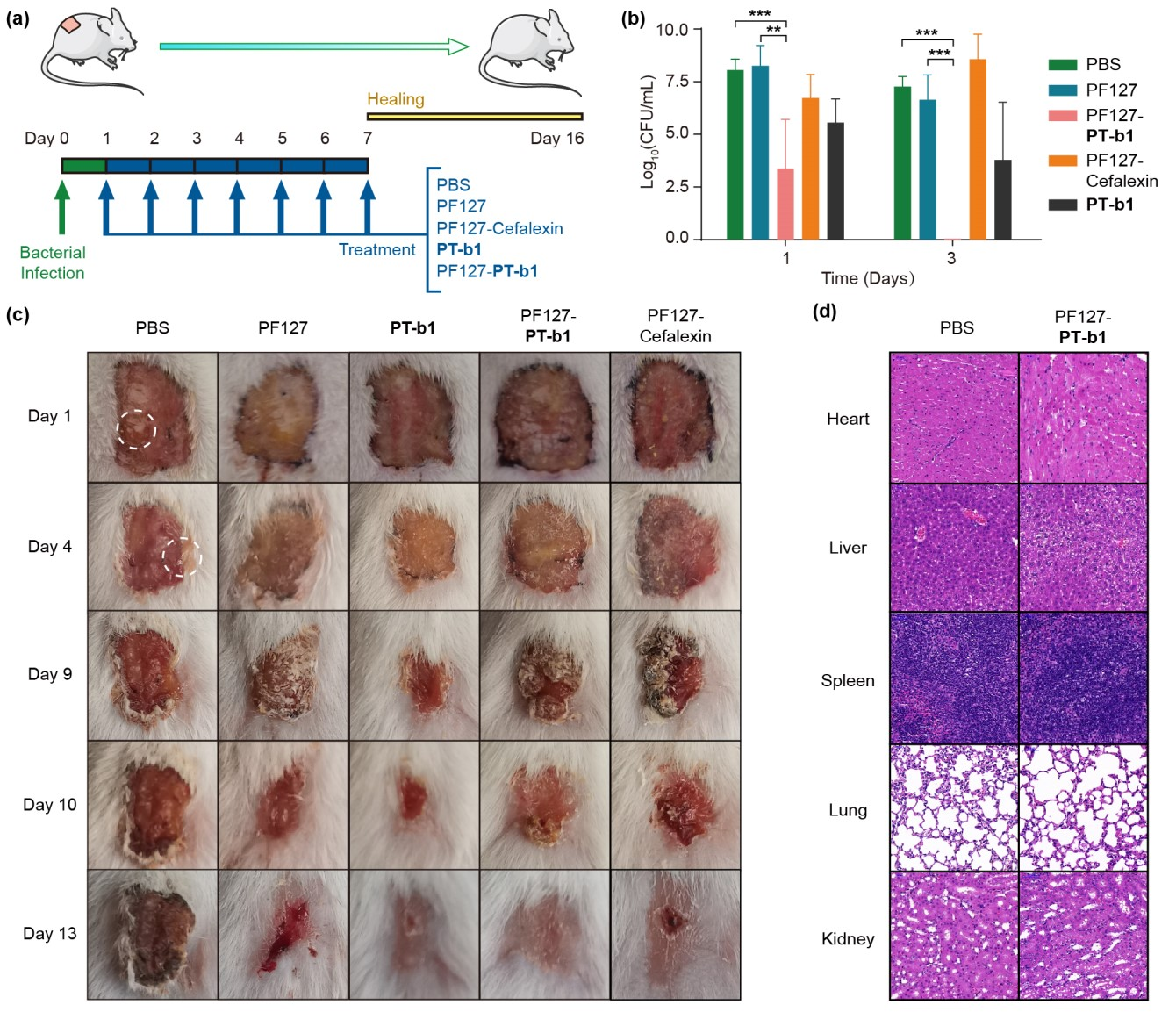
图4 PF127-PT-b1促进MRSA感染的小鼠表皮伤口愈合
最后,作者进一步建立了MRSA感染的小鼠表皮伤口模型,评价了PF127-PT-b1在活体动物上使用的安全性及对小鼠创面愈合的实际促进作用。实验表明,PF127 和 PT-b1 的组合明显更有优势:在前 3 天的持续细菌定量研究中,PF127-PT-b1 的小鼠伤口区域的细菌残存量最低,且与 PBS 组相比细菌剩余量可降低 5 -7个数量级(图 4b)。 此外,PF127-PT-b1 治疗促进了伤口愈合过程,在13天内伤口实现完全愈合,这比本实验中任何其他治疗组的愈合速率都快(图 4c)。值得注意的是,仅经 PF127-PT-b1组药物处理小鼠的免疫学组织切片中未观察到PF127-PT-b1对小鼠的显著毒性,表明PF127-PT-b1药物治疗组对小鼠的生物安全性较好(图 4d)。综上所述, PT-b1与功能聚合物PF127的复合不仅带来了更好的治疗效果,而且为伤口敷料的制备提供了新思路。
原文链接:https://doi.org/10.1002/adhm.202200546
- 中科院长春应化所栾世方/殷敬华/石恒冲研究员团队 Angew VIP:模拟维生素U结构和高选择性的抗菌肽及其应对MRSA细菌感染 2023-12-26
- 华南理工大学贾永光、王琳 ACS AMI:发展非肽类面两亲构型的阳离子胆酸聚合物用于耐药菌感染治疗 2023-07-24
- 兰州大学王凯荣教授课题组 ACS Nano:一种由天然抗菌肽和ADP构建的多功能水凝胶 2022-05-14
- 港中大(深圳)唐本忠院士团队 ACS Nano:可注射NIR-II水凝胶实现荧光成像引导的肥胖局部精准治疗 2026-05-24
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 复旦大学俞麟教授 AFM:可注射的热疗水凝胶通过调节炎症和细胞外基质代谢来抑制椎间盘退变 2026-04-05
- 武汉大学常春雨教授课题组 AFM:高强度、各向异性矿化甲壳素可吸收螺钉 2026-06-04
