东华大学何创龙教授团队《Adv. Funct. Mater.》:仿生骨微环境的多级结构生物活性支架增强血管化骨再生
2022-02-16 来源:高分子科技
由于骨植入物早期血管新生的延迟和较弱的成骨活性,骨缺损的再生修复难以获得较好的成效。骨重塑是一个持续而复杂的过程,其中血管生成和骨生成紧密相连,而血管网络的形成为组织的存活提供了适当的物质基础。工程化的微通道网络可以改善氧气扩散和营养物质输送,并能加速血管的形成,但如何在骨修复支架内部快速有效地构筑结构良好的血管网络仍然面临着巨大的挑战。

图1 DBM/GP支架的制备流程图及其生物功能示意图

图2体外药物释放与生物相容性表征
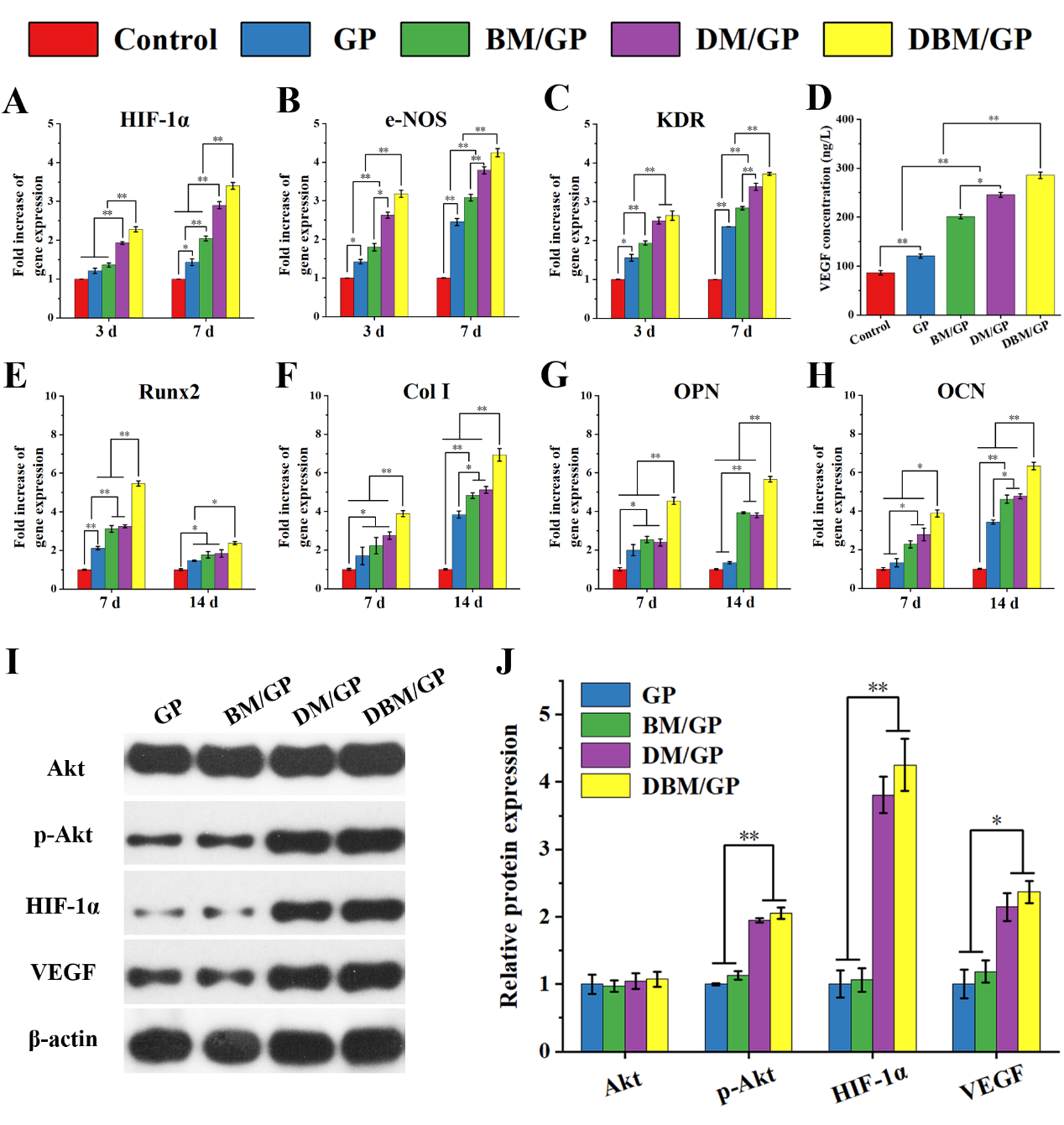
图3 体外成血管和成骨性能分析

图4 体内血管化和骨再生性能评价
该工作以“Bone Microenvironment-Mimetic Scaffolds with Hierarchical Microstructure for Enhanced Vascularization and Bone Regeneration”为题发表在《Advanced Functional Materials》期刊上,论文的通讯作者为东华大学何创龙教授和周小军博士,第一作者为东华大学硕士研究生哈玉杰和上海市第一人民医院马小军副主任医师。该工作得到国家自然科学基金、上海市自然科学基金等项目的资助。
原文链接:https://doi.org/10.1002/adfm.202200011
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 西工大黄维团队官操教授 AM:数字化制备三维液态金属水凝胶 2026-05-28
- 中国科大/伍伦贡大学 AFM 封面:基于面投影光固化技术的仿生梯度抗冲击结构材料 2026-04-17
- 南林刘承果教授团队 Adv. Sci.:用于3D打印的高性能、可循环生物基光敏聚合物 2026-03-28
- 郑州大学申长雨院士和刘春太教授团队:水辅助热致相分离法制备聚合物疏水微球 2020-08-24
- 浙江大学聚合物分离膜表面工程研究室在热致相分离制膜上取得进展 2014-07-16
- 东华大学何创龙教授团队 Chem. Eng. J.:抗菌生物活性支架发挥本征刺激与免疫调节活性共同促进血管化骨再生 2024-11-18
- 东华大学何创龙教授团队 AHM:集成荧光和磁共振成像技术的生物活性支架用于“可视化”骨组织工程 2023-11-28
