人胰岛淀粉样多肽(hIAPP)的错误折叠与聚集可对胰岛β细胞产生毒性,是2型糖尿病的重要诱因。因此,发展有效阻止hIAPP聚集的抑制剂能够作为治疗2型糖尿病的潜在药物。肽类药物与小分子比较具有高活性和生物安全性,并且能够特异性识别淀粉样蛋白,因此成为有发展潜力的候选药物。然而,多肽抑制剂通常疏水性强,水溶性低以及稳定性较差,并且目前一些肽类抑制剂仅在接近化学计量比甚至更高浓度时才有效。因此急需发展一种能够高效增强肽类抑制剂抑制效率的策略。

前期罗亮、孟凡玲团队首次报导了具有多酚特征的酪氨酸寡肽作为hIAPP的有效抑制剂。它们可以通过酚-hIAPP 相互作用阻止 hIAPP 聚集。然而,含有过多酪氨酸单元(大于 3)的寡聚酪氨酸由于其增加的疏水性和强烈的自聚集倾向无法抑制淀粉样蛋白生成。针对上述问题,罗亮团队与合作者在这项研究中合作发展了一种逐级增强寡聚酪氨酸效果的策略。由于其序列可编程性、构象特异性以及互补决定区 (CDR) 与抗原的高亲和力,纳米抗体成为增强寡聚酪氨酸抑制效果的有效策略。四聚酪氨酸 YYYY (4Y) 被嫁接到纳米抗体的第三互补决定区 (CDR3) 以构建纳米抗体 N4Y,从而固定4Y的构象,增强其与 hIAPP 的结合亲和力,初步增强4Y的抑制效果。接下来将 N4Y 与聚合物N,N-二甲基乙二胺改性的聚(丙烯酸)(PAA-DMA, or PD)偶联,形成多价聚合物-纳米抗体偶联物 PAA-DMA-N4Y (PDN4Y), 以通过多价效应实现对4Y 的二次活化(图1)。
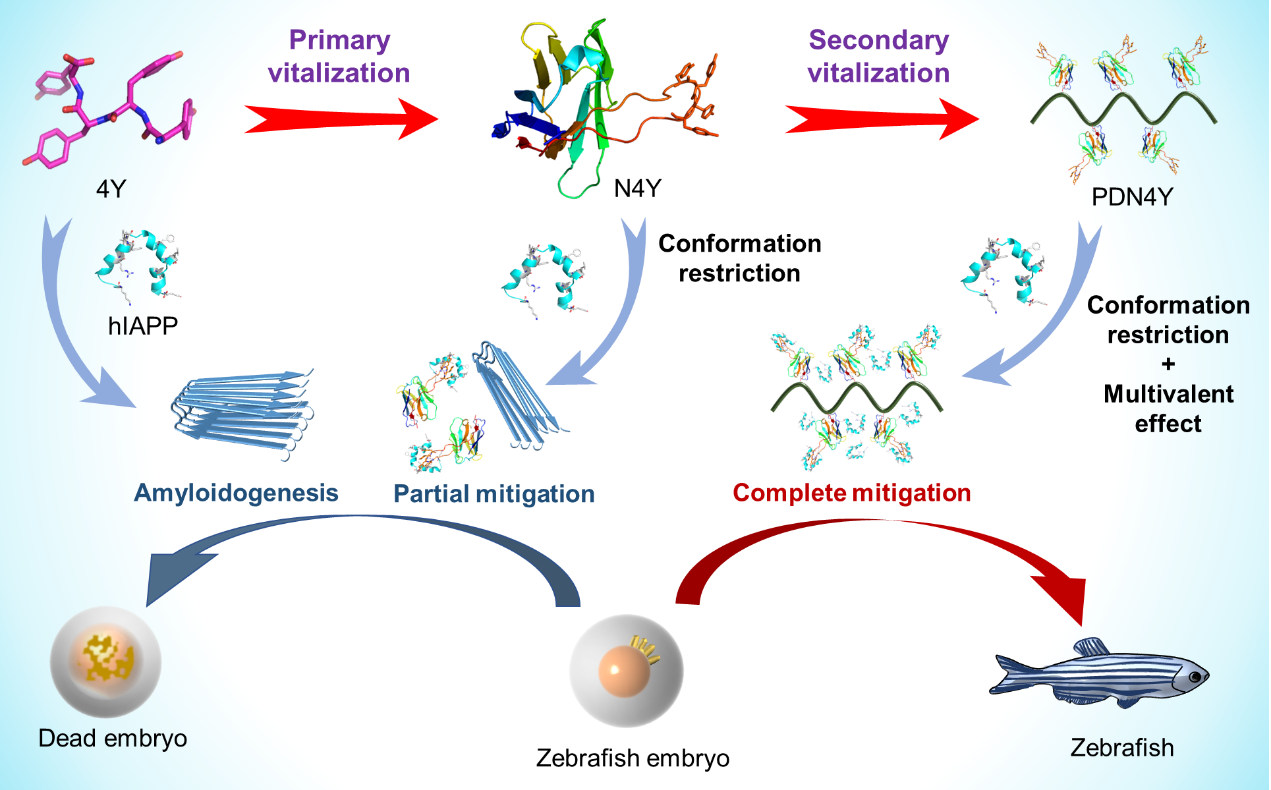
图1. 纳米抗体 N4Y 和多价大分子 PDN4Y 逐级增强IAPP聚集抑制效率的策略
研究者利用分子动力学模拟以及ELISA实验证实了4Y 片段与 hIAPP 之间的相互作用通过N4Y的构象受限以及 PDN4Y 的多价效应分级增强(图2-3)。ThT荧光动力学和TEM等生化实验结果表明在非常低的化学计量浓度下,4Y 未能抑制 hIAPP 聚集,而 N4Y 有效地延迟了 hIAPP 聚集并部分减轻了 hIAPP 淀粉样蛋白的生成。然而,PDN4Y 能够通过构象限制和多价的协同作用完全抑制 hIAPP 的聚集和淀粉样蛋白生成(图4)。

图 2. (A) 4Y的构象。(B) 4Y和hIAPP之间的结合。(C) N4Y模型,其中四个Y残基沿CDR3的一侧对齐。(D)N4Y和hIAPP之间的结合模式,其中4Y残基(红色)向外突出并通过疏水相互作用和 π-π 相互作用与hIAPP(绿色)相互作用。
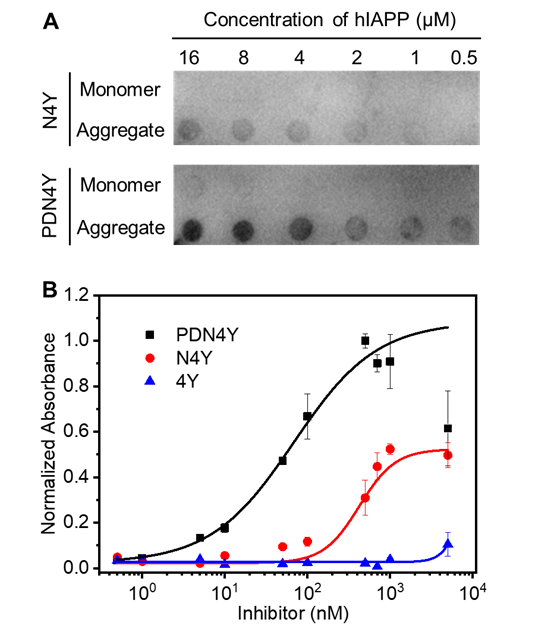
图3. 免疫印迹(A)和ELISA(B)分析hIAPP 与不同抑制剂之间的结合活性。

图4. 4Y、N4Y和PDN4Y在不同摩尔比下对hIAPP淀粉样蛋白生成的抑制作用。(A, B) 通过 ThT检测hIAPP淀粉样蛋白原纤维组装的动力学。hIAPP: 抑制剂摩尔比分别为 20:1 (A) 和 40:1 (B)。(C) hIAPP 动力学实验在不同抑制剂存在下的滞后期时间。(D) hIAPP在动力学实验结束时的TEM图像。
研究者在细胞水平上验证了这种策略对hIAPP寡聚体诱导的细胞毒性的分级缓解。结果显示hIAPP与大鼠胰岛细胞共孵育产生50%的细胞毒性,加入4Y之后细胞活力没有提升,加入N4Y细胞活力提升到60%,而加入PDN4Y之后细胞活力被挽救到80%以上(图5)。

图5. 在hIAPP:抑制剂摩尔比分别为20:1 (A)和40:1 (B) 的情况下,通过 MTT 评估在不同抑制剂对hIAPP细胞毒性的分级缓解作用。
迄今为止,大多数关于抑制人胰岛淀粉样蛋白纤维化的研究主要是在细胞水平或体外实验中进行的。最近,斑马鱼已被用作淀粉样变性研究的体内模型。研究者最后使用斑马鱼胚胎来评估不同抑制剂在体内减轻 hIAPP 淀粉样变性诱导的毒性方面的功效。结果显示多价大分子PDN4Y能够通过构象限制和多价的协同作用有效减轻 hIAPP 介导的毒性和斑马鱼胚胎中活性氧 (ROS) 的产生。

图6. 斑马鱼胚胎毒性和活性氧 (ROS) 生成的体内检测。(A-B)毒性测定(A)和ROS生成测定(B)的斑马鱼实验设计示意图。(C) 72 hpf时存活和死亡胚胎的数量。 (D) DCF检测ROS生成。 (E)健康和死亡胚胎的代表性图像。(F)通过荧光显微镜检查胚胎ROS生成。
综上,本研究利用结构、生化、细胞和斑马鱼模型,成功地发展了一种能够分级增强寡聚酪氨酸抑制 hIAPP 淀粉样蛋白生成的策略,同时也发展了一种针对hIAPP聚集的高效抑制剂,对2型糖尿病预防与治疗具有巨大的临床应用潜力。本研究对其它以淀粉样蛋白沉积为靶点的退行性疾病也提供了一种全新的治疗与预防思路。
上述研究成果在《ACS Nano》在线发表,题为“Hierarchical Vitalization of Oligotyrosine in Mitigating Islet Amyloid Polypeptide Amyloidogenesis through Multivalent Macromolecules with Conformation-Restrained Nanobody Ligands”。华中科技大学博士生辛彦儒和汪盛副教授为论文共同第一作者,华中科技大学罗亮教授和孟凡玲副教授为论文共同通讯作者。该研究得到了国家自然科学基金、国家基础研究计划、湖北省自然科学基金和中央高校基本科研业务费专项基金的资助。
论文链接:https://doi.org/10.1021/acsnano.1c03083
- 陕西师范大学杨鹏教授团队 JACS:α-螺旋介导的蛋白粘附 2023-08-03
- 上海科技大学钟超课题组《Sci. Adv.》:开发出功能可编程淀粉样蛋白涂层材料 2020-05-21
- 陕西师大杨鹏教授课题组:基于蛋白质类淀粉样聚集的抗污涂层 2020-05-06
- 东华大学陈志钢教授团队 AFM:钙离子输送的自泵式Janus膜用于糖尿病伤口愈合 2026-04-26
- 黄维团队杨震课题组 ACS Nano:超声“开关”调控水凝胶 - 实现糖尿病伤口的逆境重塑 2025-10-17
- 东华大学毛吉富、张倩 AFM:纳米互锁增强电活性敷料 - 电磁感应促进糖尿病伤口愈合和伤口微环境监测 2025-08-08
