近日,陕西科技大学生物质与功能材料研究所王学川教授/刘新华副教授与四川大学郭俊凌教授联合团队报道了一种多功能明胶基柔性导电皮肤支架,该材料兼具自修复、促进组织愈合以及运动传感性能等。相关研究成果发表于国际顶级期刊Biomaterials上。

图1 多功能电子皮肤支架的构建思路
电刺激能够显著促进组织再生,将其应用于伤口治疗过程能有效促进伤口愈合。本文设计了一种具有一定机械强度、电活性和自修复性能的水凝胶支架(MESGel),可用于电刺激加速伤口愈合和运动传感。MESGel具有优异的生物相容性和多功能特性,包括柔韧性、自愈合性能、生物降解性和生物电活性。综合生物实验证明,MESGel电子皮肤支架能通过电刺激作用,积极促进仓鼠肺上皮细胞的增殖,从而诱导皮肤创伤愈合,为全层皮肤缺损模型提供了一种有效的治疗策略。此外,MESGel还可作为一种新型柔性电子皮肤传感器实时记录伤口愈合过程的运动信号,有望实现伤口治疗-实时监测一体化。
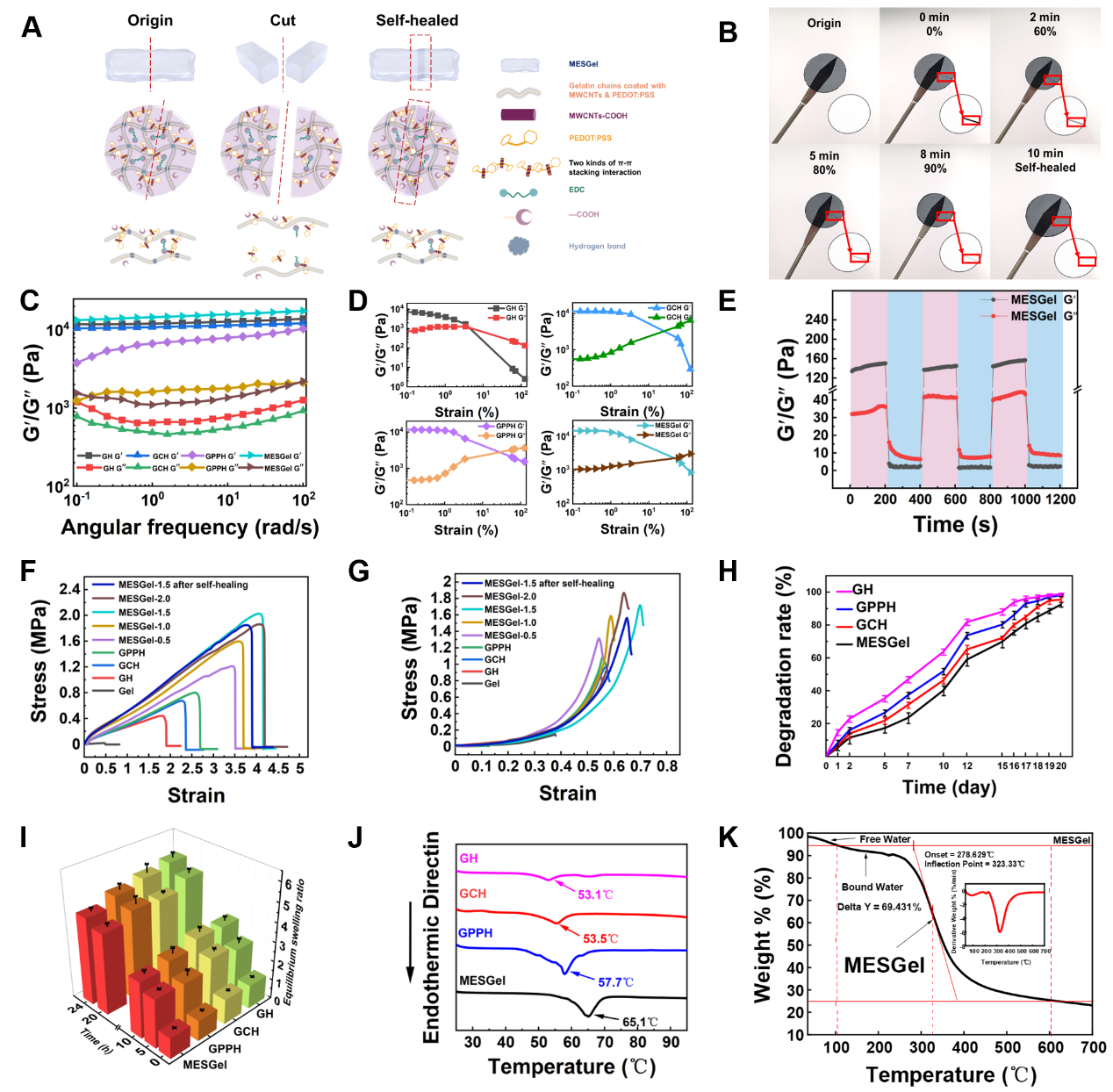
图2 MESGel电子皮肤支架的结构及力学性能表征
自修复实验证实,MESGel具有优异的自修复性能,且主要原因是MESGel电子皮肤支架内含有大量的氢键作用、静电相互作用和π-π堆积作用(图2 A)。从图2 B可以看出,被切割后的MESGel可以在2分钟内自修复至60%,在10分钟内达到完全愈合。在交替应变扫描试验中(图2 E),通过储能模量(G'')和损耗模量(G″)的测定,考察了MESGel的流变性能。在0.1 rad/s到100 rad/s的频率范围内,G''占主导地位。其中,MESGel的G''最高,表明其机械强度最高。用高应变(200%)破坏水凝胶分子链的缠结网络结构,并用低应变(10%)研究凝胶的自修复性能。在三个断裂和恢复循环中,MESGel断裂的内部结构能够快速恢复(图2 E)。这种特性对支架应对细胞增殖过程中组织应力引起的微裂纹至关重要。同时,MESGel支架具有良好的力学性能,能够承受高达425%的拉伸应变和71%的压缩应变。

图3 MESGel电子皮肤支架的传感性能表征
图3 阐明了MESGel电子皮肤支架传感器的构建方法及性能。通过对人体关节运动的监测,包括关节(图3 B)、肘部(图3 C)、手部(图3 D)和手腕(图3 E),结果表明MESGel电子皮肤支架传感器的响应时间(RT)仅为100 ms,具有较高灵敏度(图3 C)。当压缩应变从20%增加到80%时,相对电阻变化率(?R/R0)从14.8%增加至26.0%,GF为18.35(图3 F)。当拉伸应变从120%增加到200%时,?R/R0从19.6%增加至33.7%,GF为18.6(图3 G)。以上实验结果表明,MESGel可以作为一种电子皮肤传感器,用于运动损伤的实时监测。
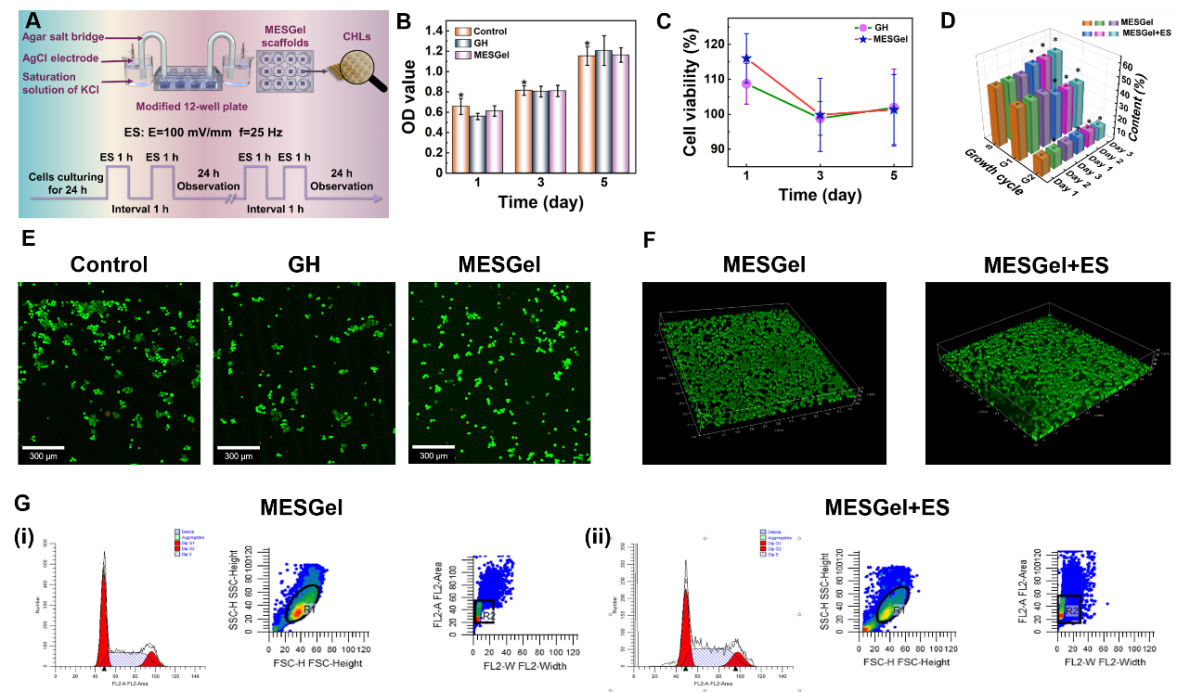
图4 MESGel电子皮肤支架的生物相容性及促进细胞生长繁殖的性能
为了验证MESGel电子皮肤支架在电刺激作用下对细胞增殖的促进作用,在与仓鼠肺上皮细胞(CHL)的共培养实验中,通过外加电源对MESGel电子皮肤支架进行电刺激。结果表明,CHL细胞在支架上生长均匀,电刺激5天之后,细胞死亡数量较少(图4 F)。通过流式细胞仪检测CHL细胞的细胞形态及增殖能力,实验表明MESGel+电刺激组细胞的侧向散射(SSC)值更高,即细胞内的颗粒度更大。且前向散射(FSC)值也相似,因此细胞大小没有差异(图4 G)。较高的细胞增殖指数(CPI)意味着大多数细胞处于DNA复制期,进入G2期,并逐渐进入有丝分裂期(图4 D)。也就是说,电刺激作用对CHL细胞增殖有显著的正效应。
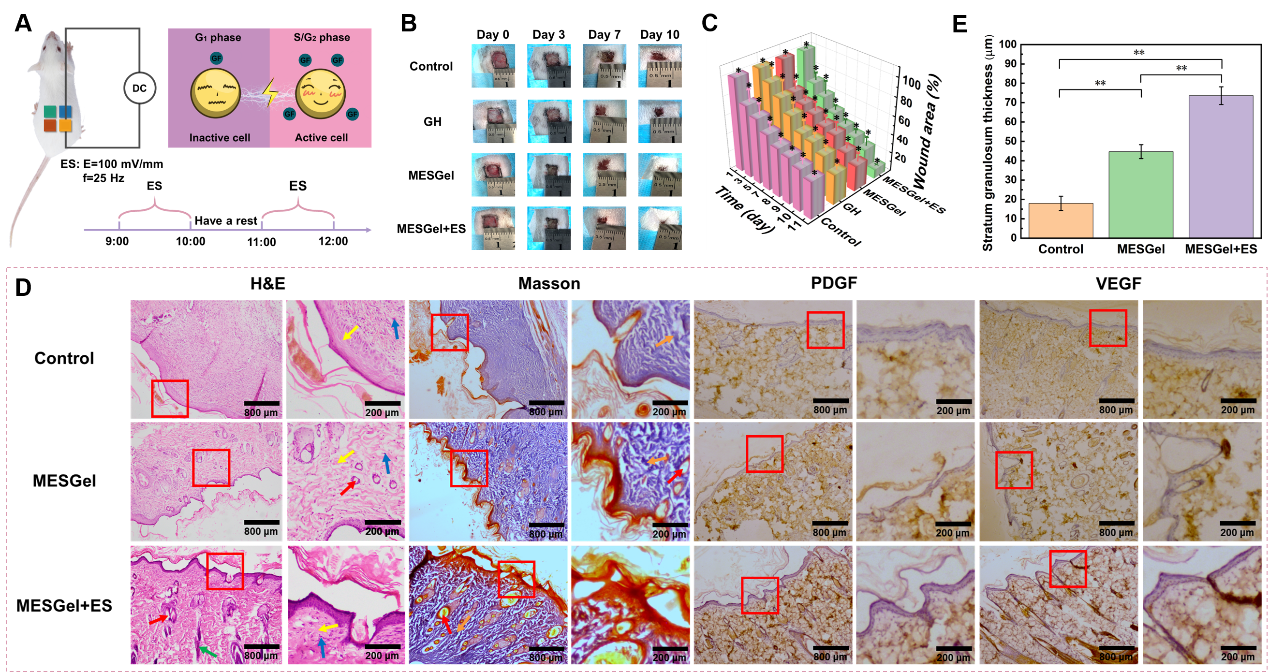
图5 SPF大鼠全层皮肤缺损模型及免疫分析
采用SPF大鼠全层皮肤缺损模型对MESGel在电刺激作用下对伤口愈合影响进行评价(图5 )。结果表明,电刺激作用下电活性MESGel电子皮肤支架促进创面愈合作用更为明显。进一步病理学结果表明,在MESGel+电刺激组治疗的创面伤口切片中可以观察到丰富的新生毛囊和血管,较厚的新表皮层和较为完整的组织结构,且PDGF和VEGF的表达更为显著,表明电刺激作用下MESGel可加速成纤维细胞和角质形成细胞增殖、肉芽组织形成和上皮化过程,从而促进伤口愈合。
相关成果以“Skin-Inspired Gelatin-Based Flexible Bio-Electronic Hydrogel for Wound Healing Promotion and Motion Sensing”为题发表在Biomaterials(Biomaterials, 2021, 121026, DOI: 10.1016/j.biomaterials.2021.121026)上。陕西科技大学博士研究生郑漫辉为本论文的第一作者,通讯作者为陕西科技大学王学川教授、刘新华副教授与四川大学郭俊凌教授。感谢国家自然科学基金(21808133,21804084)、咸阳市/温州市科学技术项目(2018k02-28/2019Y1073)、国家“海外高层次人才”计划、国家双一流重点建设学科计划、制革清洁技术国家工程中心(四川大学)对本工作的大力支持!
原文链接:https://doi.org/10.1016/j.biomaterials.2021.121026
- 浙大王立教授/俞豪杰教授团队Carbohyd. Polym.:用于促进伤口愈合和骨再生的多巴胺功能化硫酸软骨素/明胶基复合水凝胶 2025-07-26
- 浙大王征科课题组《Macromol. Rapid Commun.》: 泥鳅粘液-甲基丙烯酰化明胶超润滑水凝胶 2025-06-30
- 郑州大学睢晓洁 AHM:可便捷用于伤口修复的干细胞低温保存平台 2025-01-12
- 中国林科院林化所张猛/悉尼大学程文龙/南昆大宋平安 Adv. Mater.:含磷/氮及π-共轭联苯结构单元实现弹性体高强、高韧、阻燃及自修复 2026-06-01
- 俞书宏/何振团队 Nat. Commun.: 牙釉质启发兼具高力学和自修复性能的仿生纳米复合材料 2026-05-19
- 北化刘军/冯岸超/张玮峰团队联合王中林团队 AM:打造“六边形战士”柔性材料 - 集自修复、粘附、发电于一身 2026-05-12
- 东华大学陈志钢教授团队 AFM:钙离子输送的自泵式Janus膜用于糖尿病伤口愈合 2026-04-26
