在传统的酶传感器中,局限于生物酶本身的脆弱性、酶与底物远距离导致的弱催化性,使得生物酶与电极集成的酶簇电化学传感器信号识别敏感性差。为了进一步提高电化学生物传感器的灵敏性,引入具有高比表面积、高催化活性位点和纳米有三维多孔结构的金属-有机框架材料(MOFs)作为纳米酶,与生物酶复合,从而提高稳定性和灵敏性。
针对现有生物酶催化活性低、灵敏性差等问题,浙江大学黄小军团队基于中空纤维膜(HFM)膜材料高比表面积的结构设计,通过可控的物理包埋方法将纳米酶-天然酶杂化纳米体系有效的组装到导电梯度膜电极上。如图1所示,将三价铁离子掺杂到代表性的MOFs中,铁离子的引入赋予了MOFs粒子类过氧化物酶性质。通过静电吸附作用将MOFs与氧化酶耦合,构建尺寸为300 nm左右的MOF-酶杂化纳米体系,赋予其级联催化性能。在HFM载体上原位合成导电聚苯胺纳米颗粒(PANI NPs),并通过物理包埋方法将MOFs-酶杂化纳米体系组装在膜孔的受限空间中。HFM中的大量微孔空间促进了受限微孔空间中MOFs-酶的更高密度堆积。此外,HFM对复杂的流体(例如血液)显示出良好的分离性能。导电互连网络的纳米结构充当与级联催化MOFs-酶体系接触的锚点,从而大大提高信号传导和生物传感器信号收集的能力。
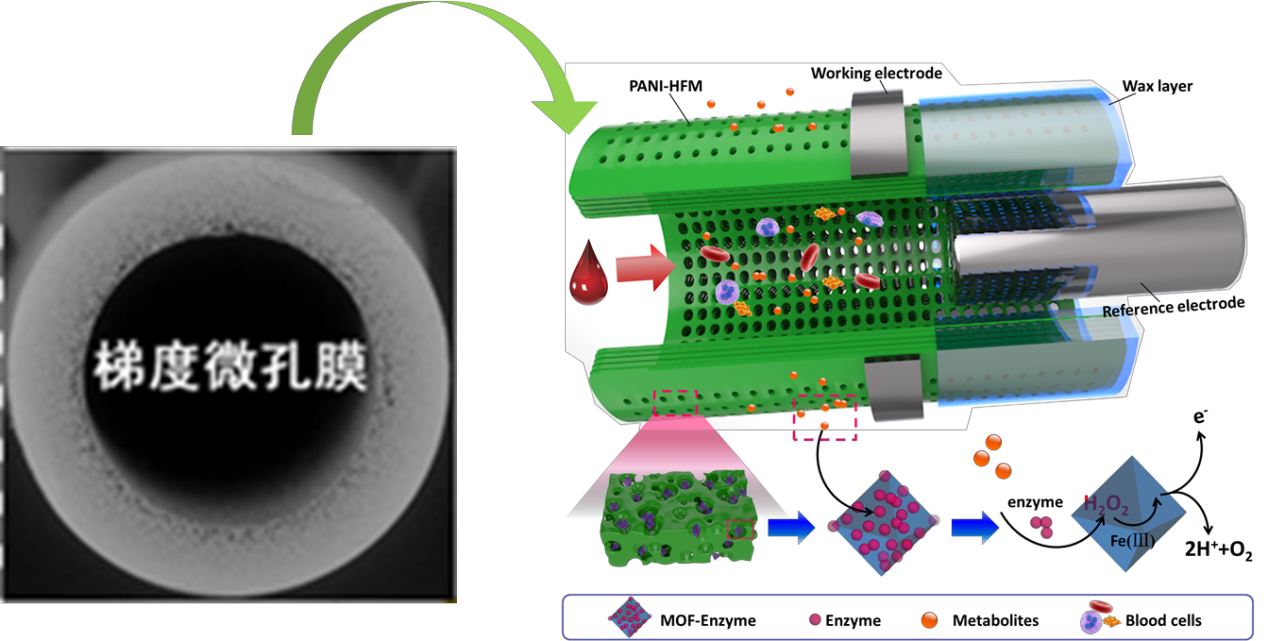
图1 基于导电中空纤维膜的MOFs-酶膜生物传感器制备及工作原理
如图2所示,由MOFs-酶杂化纳米催化体系、梯度多孔载体和纳米结构的导电网络集成的酶膜传感器可以拓展成多通路阵列传感设备。构建PDMS基底,并在基底上组装不同生物酶种类的酶膜传感器,可用于对各种微量分析物进行同步即时检测,为未来复杂标志物的智能化、一体化检测提供了新思路。
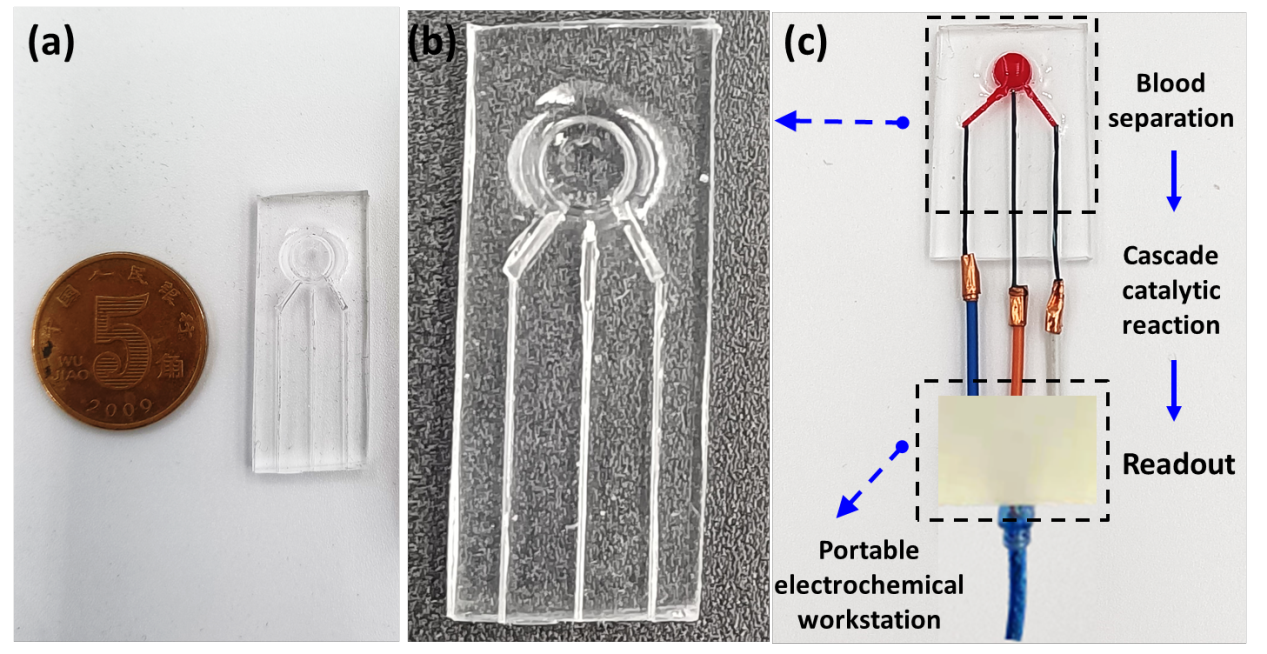
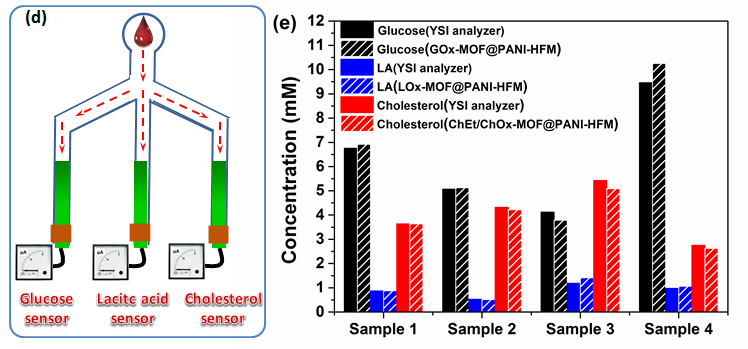
图2 基于导电梯度中空纤维膜的MOFs-酶膜生物传感阵列
相关成果以“MOF-enzyme hybrid nanosystem decorated 3D hollow fiber membranes for in-situ blood separation and biosensing array”为题发表在高水平期刊Biosensors and Bioelectronics (IF=10.257)。论文的第一作者为浙江大学高分子科学与工程学系黄小军副教授团队的博士研究生吴慧敏;通讯作者为浙江大学高分子科学与工程学系黄小军、仝维鋆副教授、杭州师范大学医学院陈大竞教授。该项工作得到了国家自然科学基金、浙江省自然科学基金等项目的资助。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S0956566321004504
- 宁波材料所刘富研究员团队《JMCA》:中空纤维膜助力光热转化 2020-11-16
- 中科院过程工程所曹宏斌研究员团队提出新型聚四氟乙烯中空纤维膜制备方法 2019-10-14
- 中科院大连化物所曹义鸣研究员团队PTFE中空纤维膜接触器技术成功应用于高氨氮废水处理项目 2019-01-25
- 杭师大黄又举/丁彩萍团队 ACS Nano:铂基超晶格生物探针赋予生物传感器“阈值特异性”实现结核性脑膜炎准确评估 2026-02-10
- MSU林少挺、TAMU吴承霖 Sci. Adv.:组织粘附的水凝胶-MXene生物传感器 为原位口腔生物监测提供新方案 2026-01-17
- 微电子所罗庆/半导体所王丽丽 Adv. Mater.:基于铁电隧道结与生物传感器集成的人工神经系统 2024-08-25
