mRNA技术在肿瘤、感染性疾病和遗传病治疗中展现出广阔前景,但其临床应用高度依赖安全、高效的递送系统。脂质纳米颗粒(LNPs)是目前比较成熟的mRNA递送平台,其核心成分可电离脂质通过酸性条件下带正电荷的特性,实现mRNA的包载和内涵体逃逸。然而,现有LNPs在系统给药后主要富集于肝脏,限制了其在肺、脾、脑以及肿瘤等肝外组织疾病治疗中的应用。尽管已有研究通过修饰靶向配体或新型脂质改善器官选择性,但这些策略存在工艺复杂、稳定性差或免疫原性等问题。相比之下,通过调控递送组分/配方的比例实现器官选择性,具有更强的模块化特征与临床兼容性。然而,目前多数研究局限于单变量优化,难以解析配方参数之间的协同与二阶交互效应,导致“试错式”筛选效率低下,亦难以形成可预测的设计原则。此外,由于体外结果与体内递送表现相关性有限,大规模体内筛选几乎不可避免,但动物实验成本高、资源消耗大,进一步制约了多维配方空间的系统探索。

本研究引入I-optimal实验设计(DoE)策略,在显著减少体内实验数量的同时,高效探索多维递送载体配方空间并建立高精度回归模型。
2026年2月27日,研究成果以“Engineering Polymer–Lipid Integrated Nanoparticles with Quantitative Design Principles for Organ-Selective mRNA Delivery”为题在JACS上在线发表。澳科大汪沁博士、中科大陈珊珊博士和李港博士生为该论文共同第一作者,中科大王育才/蒋为教授、苏州大学刘庄教授为本文共同通讯作者。
本研究构建了聚合物-脂质整合纳米颗粒(polymer-lipid integrated nanoparticle, PLIN)平台。PLIN由生物相容性的两亲性嵌段共聚物mPEG-b-PLGA、永久阳离子脂质DOTAP及可电离脂质SM-102组成。围绕三项关键连续变量进行系统设计:(i)mPEG-b-PLGA摩尔比例(polymer mol%);(ii)DOTAP与SM-102的摩尔比;(iii)脂质与mRNA的氮磷比(N/P比)。在二阶多项式回归模型假设下,纳入主效应、二次项及双因素交互项,并采用I-optimal设计筛选出15个代表性配方(PLINA1–PLINA15),在保证设计空间内均匀分布的同时最小化预测方差。在小鼠体内对这15种mLuc-PLINs进行评估后,结合回归建模定量描绘了载体配方参数与器官表达之间的多维关系,从而能够构建预测性回归模型(R2 > 0.96),理性筛选出具有肺部或脾脏偏向性的配方。进一步对模型预测的最优条件进行体内实验验证发现该模型指导的优化使PLINs在肺部和脾脏的选择性分别高达91%和96%。机制研究表明,特定配方参数通过调控蛋白冠组成及其介导的受体识别路径,驱动器官选择性mRNA表达。在功能验证层面,基于PLIN的mRNA平台在三个体内模型中展现出良好通用性:实现报告基因小鼠的特定靶细胞基因编辑、在急性肺损伤模型中递送细胞因子mRNA,以及构建抗原特异性肿瘤mRNA疫苗。通过多组分比例的调控,本研究建立了一种基于回归模型指导的器官选择性设计框架,为构建安全、高效、可预测的mRNA递送系统提供了新的思路。
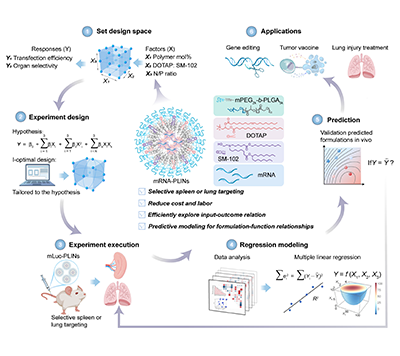
图1、采用I-optimal实验设计框架构建模块化聚合物-脂质整合纳米颗粒(PLIN)平台,用于实现器官特异性mRNA递送的整体示意图。
论文链接 https://pubs.acs.org/doi/abs/10.1021/jacs.5c22504
