光动力疗法(PDT)作为一种有效的治疗模式,由于其非手术治疗,能够选择性地根除病变组织,同时尽量减少对正常组织的损伤,引起了科学家的广泛关注。然而,有限的可见光穿透深度限制了PDT主要用于表皮层治疗。虽然近红外(NIR)激光增强了组织穿透性,但合成方面的挑战和光动力效率较低限制了近红外光敏剂的发展,其中大多数主要用于生物成像。此外,光纤植入术也应用于临床深层PDT。然而,这种需要微创手术的方法存在感染风险,并且与PDT的非侵入性相矛盾 (表1)。因此,突破PDT中可见光穿透深度的限制仍然是医学和材料科学领域面临的巨大挑战。

表 1. 一些先进的增强光组织穿透深度的技术汇总
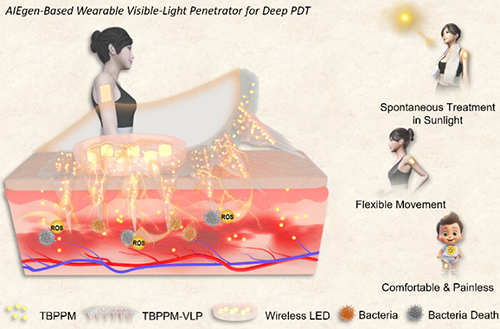
图1. 基于AIEgen的可见光穿透器用于深层组织感染的光动力治疗工作原理图
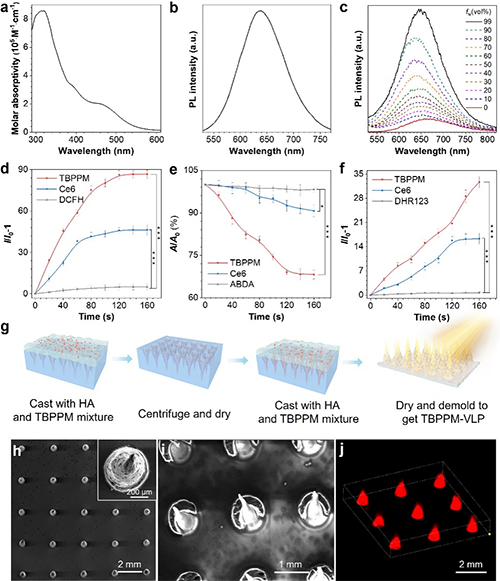
图2. a-f AIEgen TBPPM的光学性质表征及活性氧性能测试; g-j 具有光动力效果的可见光穿透器TBPPM-VLP的制备过程及形貌表征

图3 在贴附光穿透器(VLP)前后白光LED通过皮肤组织的辐照度以及透过率变化。

图4 光在皮肤模型中的传播路径。a, b无光穿透器贴片;c, d 贴附光穿透器贴片。黄色虚线为皮肤模型的轮廓。
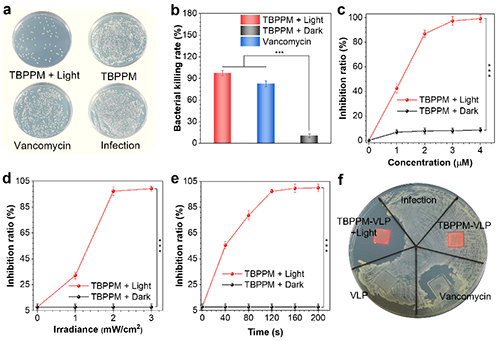
图5. TBPPM及TBPPM-VLP的体外光动力抗菌性能
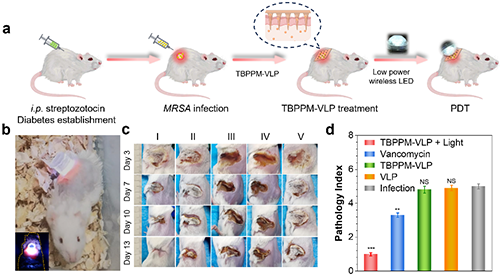
图6. 基于AIEgen的可见光穿透器贴片的光动力治疗效果图。I:TBPPM-VLP光照组;II:万古霉素治疗组;III: TBPPM-VLP无光照组;IV: 空白VLP组;V: 未处理的感染组。
原文链接 https://pubs.acs.org/doi/10.1021/acsnano.4c10452
- 港中大(深圳)唐本忠教授、赵征教授/港科大林荣业教授团队 Matter: 基于立体异构AIEgens在动态信息防伪与加密的应用 2025-07-28
- 中山大学顾林课题组 CEJ:在无需外加AIEgens的情况下,利用商业化聚酰胺固化剂的簇发光性质实现环氧涂层自主损伤检测 2024-09-26
- 温州医科大学沈贤/南开大学齐迹 AFM:纳米催化剂协同放大增强AIEgen的光诊疗性能用于癌症免疫治疗 2024-02-22
- 深圳大学领衔,织物领域最新 AM:突破“光热即黑”局限 - 王元丰/陈剑铭/王训该教授等合力打造“无色扰”光功能织物 2026-03-25
- 可见光“强化”胶黏剂!安徽大学宣俊/陈松团队 AFM:成功破解可拉伸电子器件界面失效难题 2026-02-21
- 北京师范大学邹应全教授团队《Macromolecules》:适用于互穿聚合物网络制备的芘基咪唑类可见光引发剂 2026-01-15
- 南邮周晖/西工大胡文博/山东大学崔基炜/高丽大学 Jong Seung Kim JACS:逃避免疫清除 - 实现可重复光动力治疗 2026-03-18
