糖尿病影响着全球超5亿人的生命健康。其中,超过20%的糖尿病患者需要外源性胰岛素治疗。然而,现有的胰岛素制剂通常经皮下注射给药,吸收后进入外周血液循环。胰岛素的治疗指数窄,导致胰岛素给药后患者低血糖频发,严重时会危及生命。而健康胰腺中的β细胞能感应血糖水平,精准智能调控胰岛素分泌。其分泌的胰岛素先经肝门静脉进入肝脏,发挥核心降糖作用,随后分布至外周,使得人体能够高效安全地控制血糖水平。因此,模拟人体胰岛素分泌机制,改变胰岛素给药方式,优化其外周起效的特点,对于胰岛素治疗具有重要意义。

图1:糖响应性胰岛素胶束制剂的形成及糖响应释放胰岛素示意图
该研究中,团队合成了一种两亲性聚合物(命名为PPF),其亲水端为两性离子型聚甜菜碱,疏水端为4-羧基-3-氟苯硼酸(FPBA)修饰的聚2-氨基乙基甲基丙烯酸酯。胶束制剂由PPF与胰岛素-锌离子六聚体自组装形成。其独特的蠕虫状结构、较小的粒径以及两性离子表面,促进胰岛素在肠道内高效吸收,并在肝脏形成糖响应的胰岛素储库。
在正常血糖条件下,制剂中的胰岛素缓慢释放,有效维持基础血糖的稳定。而在高血糖状态下,葡萄糖会与FPBA结合形成苯硼酸酯键,降低聚合物疏水端的正电荷密度及疏水性,刺激胰岛素快速释放。实验结果表明,在向小鼠灌胃荧光标记的胶束后,可于小鼠腹部及肝脏区域清晰观察到荧光分布。该制剂首先将胰岛素释放至肝脏组织,形成从肝脏到外周组织逐渐降低的浓度梯度,因此可显著减少低血糖事件的发生。
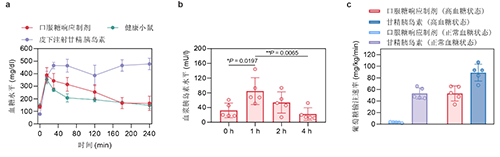
图2:a, b,糖尿病小鼠在葡萄糖耐量实验中的血糖变化和血浆胰岛素水平变化情况。c,小鼠血糖钳夹实验中,不同给药组别所需的葡萄糖输注速率。
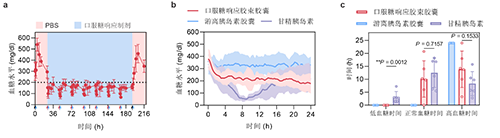
图3:a,糖尿病小鼠在连续给予口服制剂后的血糖水平变化(蓝色箭头表示食物供给,红色箭头表示口服糖响应制剂灌胃,黑色箭头表示PBS灌胃)。b,糖尿病小猪口服制剂胶囊后的血糖水平变化。c,糖尿病小猪在治疗后,低血糖、正常血糖和高血糖状态的持续时间。
相关论文信息:https://doi.org/10.1038/s41565-024-01764-5
- 可口服,可用于血液透析急性排铅!武汉大学邓红兵/陈朝吉教授团队AFM:固定了高生物安全性酿酒酵母的纳米纤维气凝胶用于人体综合除铅 2023-02-13
- 华东理工刘润辉教授课题组 JACS:双胍基化聚噁唑啉-胰岛素复合物在小型猪中实现长效葡萄糖响应性胰岛素释放 2025-10-25
- 吉林大学林权教授团队 CEJ:葡萄糖响应性水凝胶优化芬顿反应以根除多重耐药细菌促进感染型糖尿病伤口愈合 2024-04-14
- 浙大王立教授和俞豪杰教授团队 ACS AMI:用于糖尿病治疗的静电作用增强的葡萄糖响应胰岛素递送微针贴 2024-02-09
- 历时五年攻关,胰岛素无损透皮给药成果登 Nature! 2025-11-20
- 浙江大学王立教授、俞豪杰教授团队 Carbohyd. Polym.:基于糖敏水凝胶的智能长效胰岛素递送微针贴 2024-11-21
- 浙大王立教授和俞豪杰副教授团队 ACS AMI:用于模拟一日三餐血糖控制的葡萄糖响应纳米粒子及其微针贴 2023-07-08
