聚合物纳米自组装体作为药物递送系统在癌症治疗中受到越来越多的关注,因为它们可以规避小分子药物的一些药理学限制,例如水溶性差、非特异性分布、全身毒性等。此外,刺激响应性聚合物纳米组装体通过响应内源刺激(如pH变化、氧化还原梯度、酶等)或外源刺激(如光、温度变化、超声波、磁场)可以控制药物的释放,从而进一步提高药物的生物利用度。 这些刺激源中,光刺激由于其方便的远程控制和出色的时空分辨率而受到格外的关注。然而,光响应的聚合物纳米自组装体的抗肿瘤应用往往受限于光的弱组织渗透性,这会导致药物释放的不完全。这项工作旨在将可用作光动力疗法(PDT)的钌金属配位化合物与含硫醚的聚类肽通过配位作用进行结合,得到的含钌的两亲性聚类肽通过纳米沉淀形成纳米自组装体。这些纳米组装体在红光的照射下会裂解,释放金属配合物,同时增强活性氧的产生,此协同效应可以用于提高光动力疗法和光响应药物释放化疗的效率 (见图1)。


图 1. (A)各种化合物的结构。(B) 红光 (625 nm) 照射下的 PolyRu 胶束和囊泡。
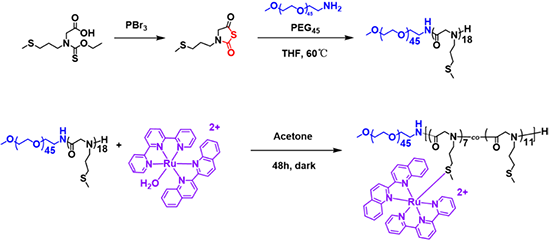
图 2. PEG45-b-PMeSPG18以及 含Ru 配位化合物的 PEG45-b-PMeSPG18 (PolyRu) 的合成路线。
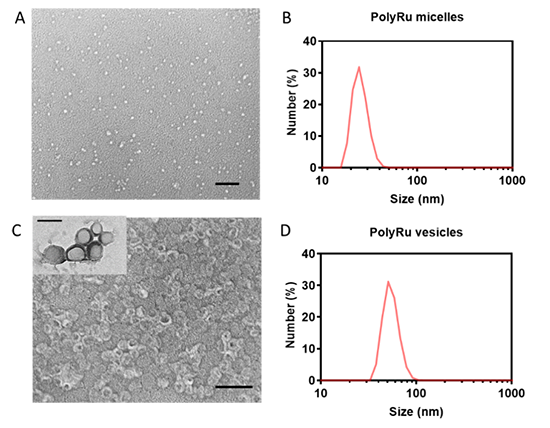
图 3. PolyRu 纳米自组装体的表征。使用 DMF 作为有机共溶剂可以形成的 PolyRu纳米胶束,平均水合粒径为 21± 1 nm 。 使用 THF/丙酮 = 1/1 作为有机共溶剂可以形成的PolyRu 纳米囊泡,平均水合粒径为59 ± 2 nm。
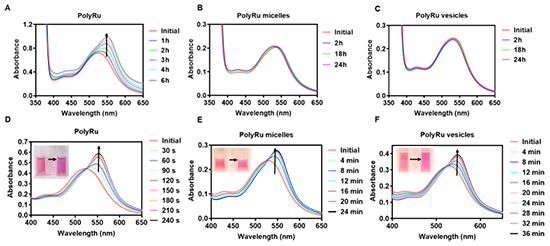
图 4. 通过紫外-可见吸收光谱进行PolyRu 嵌段聚合物和 PolyRu 纳米自组装体中 Ru-S 配位键的稳定性与光裂解特性分析。图 4A, 4B 与4C是在无光暗条件下得到的,其表明自组装体增强了 PolyRu 共聚物中 Ru 部分的暗稳定性,这可以解释为水不易进入聚合物胶体的疏水核或层。图 4A, 4B 与4C是在625 nm光照射下得到的,其表明在PolyRu胶束和囊泡中也观察到典型的金属-配体电荷转移带( MLCT )的红移。然而, PolyRu 胶束和囊泡达到最大红移的时间比 PolyRu 长得多。

图 5. DCFH 检测红光照射下样品中 ROS 的产生以及光诱导胶束与囊泡的结构破裂研究。红光照射 24 分钟后,PolyRu 胶束和囊泡中的 DCF发射强度达到游离 Ru 配位化合物的两倍 (图5B,C,D,E)。并且随着光照时间的变化,胶束与囊泡的尺寸与粒子浓度不断降低(图5F)。PolyRu自组装体具有更强的 ROS 产生效率,这可能与硫醚基团氧化导致 PolyRu组装体发生的破裂有关。由于Ru均匀地分布在疏水层或核中,在破裂过程中囊泡和胶束里出现的高比表面积的多孔结构可以提高氧的吸收并促进氧与钌基光敏剂的接触,进一步提高ROS的产生效率。
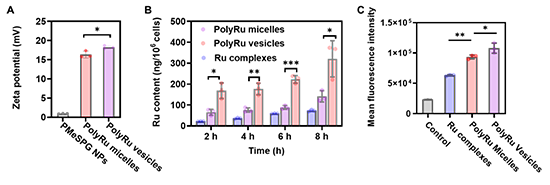
图 6. PolyRu 胶束和囊泡的细胞摄取和细胞内 ROS 检测。(A). ζ 电位测试表明PolyRu 胶束和囊泡呈现这可能是由于具有较大的正 ζ 电位,有利于其细胞摄取。(B). Ru在细胞内被有效检测到。PolyRu胶束和囊泡与细胞孵化后,测得的细胞内Ru含量均高于单独Ru配位化合物与细胞孵化后测得的数据,这可能由于纳米颗粒的内吞途径不同所致。(C). 流式细胞仪检测红光照射 30分钟后细胞内 PolyRu 胶束、囊泡、 Ru 配位化合物产生的 ROS,DCFH氧化成的DCF为荧光探针。PolyRu 胶束和囊泡产生的 ROS明显多于Ru 配位化合物。
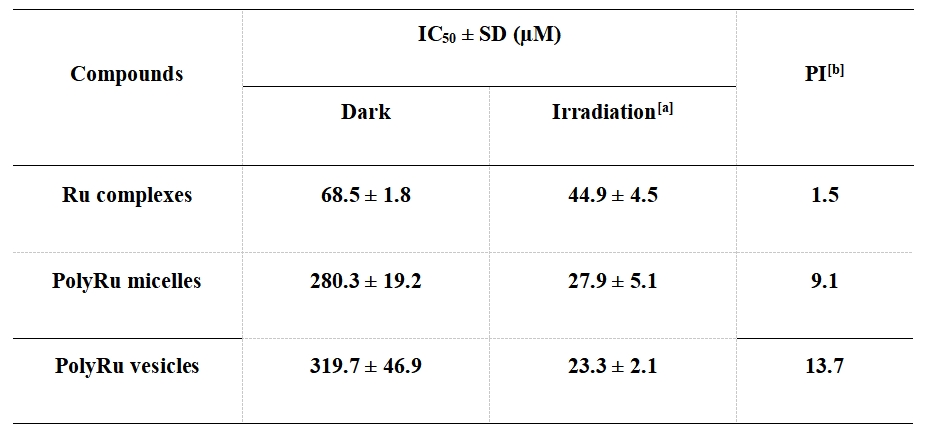
表1.PolyRu 纳米胶束和囊泡的细胞毒性测定。
这项工作以“Red-Light-Responsive Polypeptoid Nanoassemblies Containing a Ruthenium(II) Polypyridyl Complex with Synergistically Enhanced Drug Release and ROS Generation for Anticancer Phototherapy”为题发表在《Biomacromolecules》(DOI: 10.1021/acs.biomac.3c00949 )期刊上。法国巴黎文理大学巴黎高科化学学院博士生马燕东为第一作者,李敏慧教授为通讯作者。该工作得到了 CNRS的MITI 跨学科项目,广州菁英计划留学基金以及中国国家留学基金委的资助与支持。
原文链接:https://pubs.acs.org/doi/10.1021/acs.biomac.3c00949
- 红光响应的含钌高分子抗癌试剂 2016-12-28
- 吉大陈学思院士、孙静教授团队 JACS:聚类肽辅助因子精准调控熊果酸螺旋纳米纤维原位动态组装实现协同肿瘤增效治疗 2025-05-13
- 北科大姜乃生教授《ACS Macro Lett.》:侧链支化对受限聚类肽薄膜多级晶体结构的影响 2022-08-25
- 北科大姜乃生、LSU张东辉等《JACS》:通过侧链支化调节嵌段共聚类肽的溶液自组装 2021-05-08
- 国科大屈小中教授课题组 Angew:在高分子-蛋白多层次结构纳米组装体制备和应用研究中取得进展 2024-02-27
- 四川大学张新星教授、西工大杨勇教授 AFM:具有动态物理网络的强韧化自修复弹性体 2022-10-21
- 陕科大白阳团队《ACS AMI》:超分子聚合物纳米组装体用于增强化学动力学治疗 2022-09-23
