近红外二区(NIR-II)有机光诊疗试剂在活体组织中具有较低的组织吸收、散射和自发荧光干扰,可以大大提升荧光成像的组织穿透深度和分辨率,在生物医学中具有广阔的应用前景。在已报道的NIR-II有机光诊疗试剂中,常用的分子设计策略是基于扩大π共轭长度或增强D-A作用来实现,但这类分子通常具有较差的水溶性,利用基质封装技术形成聚集体纳米粒子(NPs)是增强其生物相容性和水溶性的普遍策略。然而,在封装过程中有效调控分子堆积方式构建NIR-II有机光诊疗试剂的设计策略未见文献报道,如能顺利实现则为NIR-II有机光诊疗试剂的构建提供了更为便捷和有效的方法。
近日,香港中文大学(深圳)唐本忠院士、内蒙古大学王建国教授团队在Angewandte Chemie International Edition (Angew. Chem. Int. Ed. 2022, e202212673)上发表题为“A Facile Structural Isomerization-Induced 3D Spatial D-A Interlocked Network for Achieving NIR-II Phototheranostic Agents”的研究论文。作者通过深入研究分子结构与分子堆积方式之间的关系,首次提出了一种结构异构化诱导三维空间D-A互锁网络策略(图1),在纳米封装过程中调控分子堆积方式,设计了一种具有优异的光热稳定性、高光热转换效率和活性氧生成能力的NIR-II有机光诊疗试剂。

图1 近红外二区有机光诊疗试剂的分子设计策略
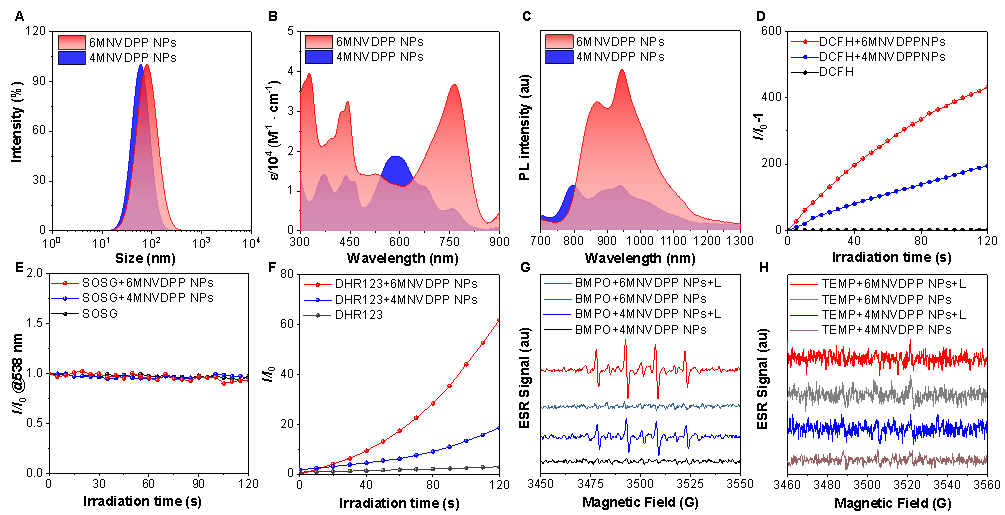

图3 光热性能测试
理论计算和单晶结构表明(图4和图5),由于6MNVDPP具有较大的表面静电势差,在6MNVDPP的晶体中,同层相邻分子通过萘环氢原子和DPP羰基之间的氢键形成双重分子间D-A相互作用;层间相邻分子通过强π-π相互作用同样形成双重分子间D-A相互作用。在三维D-A相互作用的驱动下,6MNVDPP形成了紧密的三维空间D-A互锁网络堆积。而在4MNVDDP的晶体中,无论层内还是层间均只存在单重D-D相互作用,分子堆积形成了二维D-D型J聚集。因此,6MNVDPP NPs表现出了更长的吸收波长、更大的摩尔消光系数以及更强的光热转换效率。鉴于6MNVDPP NPs优异的光物理性能,作者将6MNVDPP NPs经尾静脉注射到荷瘤小鼠体内,利用实体瘤的高通透性和滞留效应(EPR效应),对肿瘤组织实现了NIR-II荧光成像引导的光动力/光热协同治疗(图6)。

图4 理论计算结果

图5 单晶结构分析

图6 荷瘤小鼠肿瘤治疗结果
综上,这种由结构异构化诱导三维空间D-A互锁网络策略为NIR-II有机光诊疗试剂的设计、开发提供了一种新的思路,在抗癌研究中具有潜在的生物医学应用价值。
论文信息
A Facile Structural Isomerization-Induced 3D Spatial D-A Interlocked Network for Achieving NIR-II Phototheranostic Agents
Lina Feng, Chunbin Li, Lingxiu Liu, Xin Chen,Guoyu Jiang,* Jianguo Wang,* and Ben Zhong Tang*
论文链接:https://doi.org/10.1002/anie.202212673
