基于嵌段共聚物胶束纳米蚀刻技术( block copolymer micelle nanolithography, BCMN),作者成功制备了纳米间距梯度变化的金点阵列。选择内皮细胞、平滑肌细胞作为代表性细胞,发现梯度变化的 RGD 纳米间距对内皮细胞的取向和迁移的引导效果并不明显,但是可以显著诱导平滑肌细胞的取向,并且使得平滑肌细胞向较小 RGD 纳米间距的区域定向迁移。两种细胞对梯度变化的 RGD 纳米间距的响应差异为将来的细胞筛选、促伤口愈合的细胞选择性材料的表面修饰提供了新的思路。
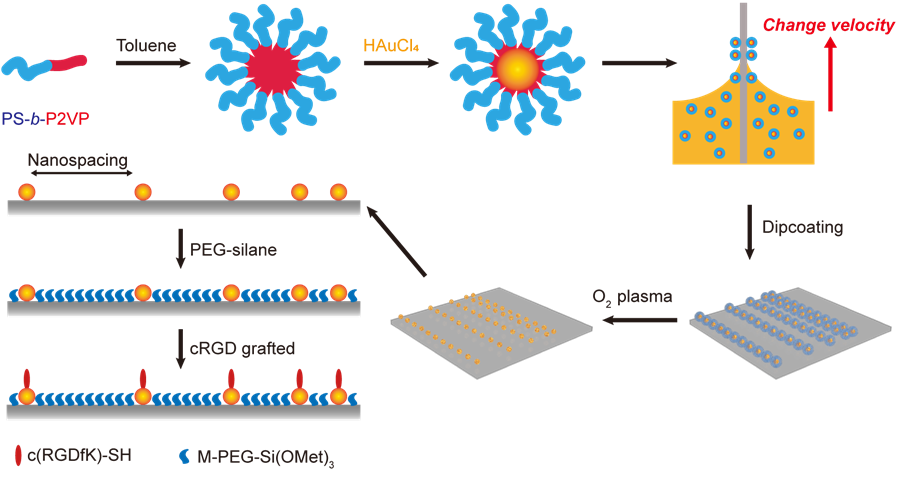
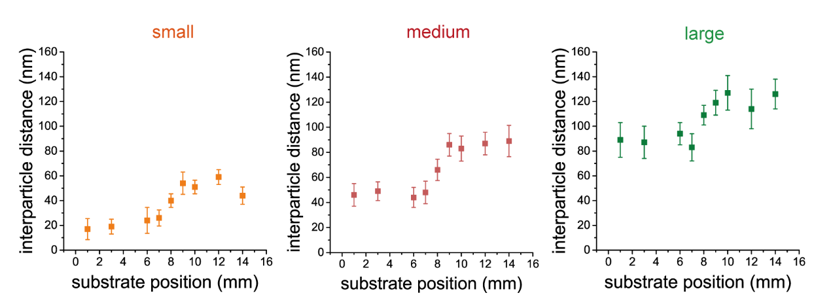
图1 梯度纳米图案的设计和制备 (A) BCMN法制备了梯度纳米图案材料流程示意图;(B) 基底各位置纳米间距的统计结果
复旦大学丁建东团队设计的梯度纳米阵列夹在两个均匀的纳米阵列当中,这样可以更好地控制整个图案。他们制备了三种图案,各自在两侧具有不同的纳米间距的范围,如图1所示;同时,中间短的梯度相仿,均约为每毫米20 nm或者每50微米1 nm。通过在纳米图案表面培养人脐静脉内皮细胞(HUVEC或EC)和人动脉平滑肌细胞(HASMC或SMC),发现细胞在某些条件在可以感知到这种纳米尺度下的微小的梯度变化。

图2 RGD纳米间距诱导细胞取向 (A) HUVEC和HASMC在中梯度纳米图案上的荧光图像;(B)分别计算HUVEC和HASMC的Max Y Length / Max X Length,分析细胞取向
作者统计了两类细胞在梯度纳米区域中迁移时在各个时刻x、 y 方向上的平均位移。对于内皮细胞和平滑肌细胞,在中等RGD 纳米间距起始范围的梯度纳米图案对两类细胞的定向迁移产生了选择性。
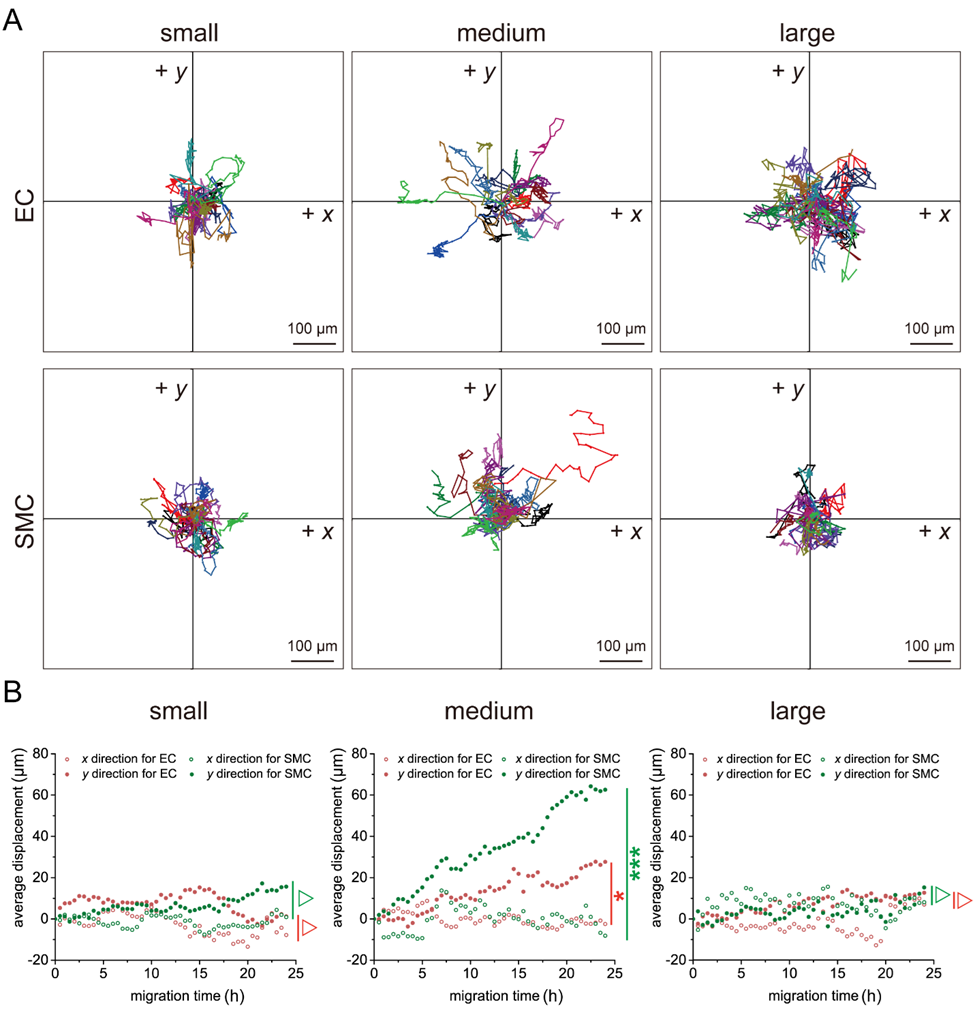
根据课题组之前的研究, 70nm 是一个临界纳米间距。一旦 RGD 纳米间距大于这个数值,特异性细胞黏附显著减弱。由此作者推测:当 RGD 纳米间距的梯度变化跨越 70 nm 时,细胞对其自身前后端的纳米间距变化将最为敏感。其中medium 组别跨越了70 nm ,黏附面积的剧烈变化带来的黏附能力差异很有可是造成细胞在这个跨度下发生明显细胞取向与定向迁移的原因。然而,对于内皮细胞,在跨 70 nm 的梯度变化下,黏附面积的变化没有平滑肌细胞显著(在梯度变化的两侧,平滑肌细胞黏附面积下降到了小间距部分的 47.1%,而内皮细胞只下降到 60.6%) ,这也可能是其细胞取向与定向迁移相较于平滑肌细胞不明显的原因所在。
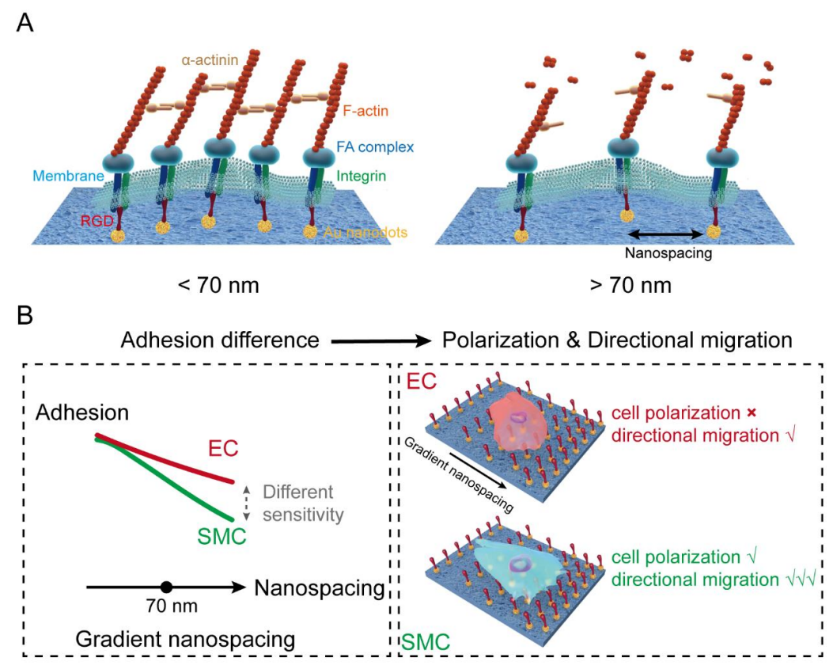
材料表面的活性配体RGD 纳米间距的梯度可以选择性地调控细胞的取向和迁移。这一发现给新一代生物材料的设计带来一定的启示。
作者团队简介:
论文以复旦大学何俊豪硕士生为第一作者,其导师丁建东教授为通讯作者。丁建东教授为复旦大学高分子科学系教授、聚合物分子工程国家重点实验室主任。其课题组主要从事生物医用材料研究,包括细胞与材料相互作用的基本科学问题、组织再生材料和先进医疗器械、药物缓释载体以及医美材料的基础研究和临床转化。
原文链接:
Junhao He, Runjia Shen, Qiong Liu, Shuang Zheng, Xinlei Wang, Jingming Gao, Qunsong Wang, Jiale Huang, and Jiandong Ding*, RGD nanoarrays with nanospacing gradient selectively induce orientation and directed migration of endothelial and smooth muscle cells.ACS Appl. Mater. Interfaces
https://pubs.acs.org/doi/10.1021/acsami.2c10006
- 华东理工刘润辉教授课题组《Adv. Mater.》:多肽模拟聚合物实现内皮细胞选择性功能 2022-09-02
- 上海交大傅德皓教授团队 ACS Nano: 仿生纳米囊泡逆转骨髓内皮细胞分泌表型治疗骨质疏松症 2022-07-13
- 四川大学王云兵教授团队Biomaterials:仿生内皮细胞功能涂层用于促进血管愈合 2022-04-01
