南丹麦大学吴昌柱教授团队《Nat. Commun.》:基于大肠杆菌化学修饰而成的人工孢子实现高效的界面生物催化
自然界中,生物体为了抵御环境中的不利因素,进化出了各自的防御机制。这其中,细菌孢子可以抵御多种环境压力,包括紫外光照射及化学试剂毒害,显示了其在生物合成领域的潜力。但自然的孢子多处于休眠状态,且其中的酶活性较低。为了解决这些问题,研究人员开发了人工孢子,即以保护性材料将细菌包裹于其中,保护细菌与酶的活性,有效提高生物催化效率,并拓展其在不对称合成及生物燃料制造等领域的应用。目前的人工孢子构建主要基于天然细菌及其本身自带的酶,这便大大限制了其在生物催化领域的应用范围。而相比之下,大肠杆菌作为最通用的重组酶表达平台,则没有在人工孢子化方面取得较大的进展。
在此背景下,吴昌柱教授及其博士后孙志永(目前就职于浙江工业大学)受自然界中细菌孢子可以抵御多种环境压力(紫外光照射及化学试剂毒害)的启发,利用聚多巴胺的良好生物相容性及保护性,包裹大肠杆菌的表面构建人工孢子。该孢子体系可以有效抵御紫外光、高温、有机溶剂、有机-水两相界面张力的影响,维护细菌的代谢活性。同时,其内部可以表达多种酶,并应用于单酶及多酶的界面催化过程(图1)。此外,该孢子可以负载化学催化剂,并成功构建起化学-酶偶联催化体系,进一步丰富了细胞工厂的应用。相关工作近日以“Artificially Sporulated Escherichia coli Cells as a Robust Cell Factory for Interfacial Biocatalysis”为标题发表于《Nature Communications》。
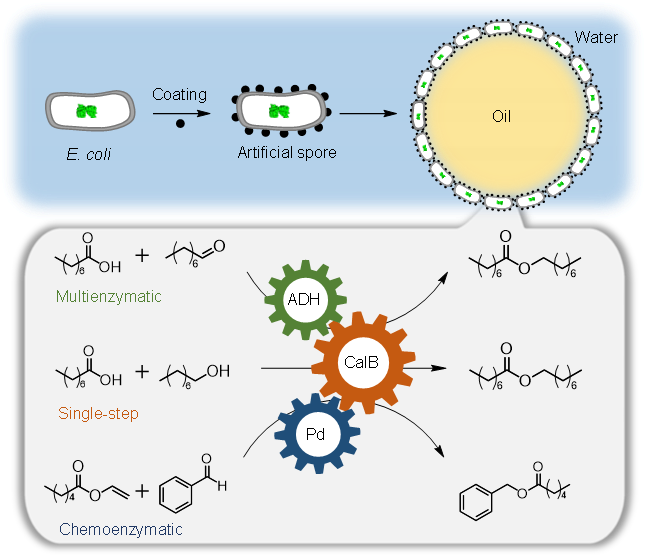
图1. 包裹大肠杆菌构建人工孢子应用于界面生物催化的示意图。
人工孢子的表征
他们首先利用透射电镜(TEM)和扫描电镜(SEM)对人工孢子进行了直观的表征,并以原始的大肠杆菌作为对照。在TEM图像中,可以看到细胞外的包覆层(图2e,2f),而原始细菌外则没有。SEM表征中,可以直观看到颗粒状的包裹物和粗糙的表面(2g),而原始细菌的表面相对光滑。综合SEM和TEM,人工孢子的形成得到了有力的证实。

图2. 人工孢子的表征。b-d:原始细菌。e-g:人工孢子。
生物相容性表征
之后,他们对包裹过程的生物相容性进行了验证。在细菌活/死实验中,通过与原始细菌对比(图3a),可以看到人工孢子有着较高的存活率(图3b,绿色)。此外,人工孢子的繁殖能力也与原始细菌相当(图3c)。

图3.生物相容性评价。a: 原始细菌。b:人工孢子。c:生长曲线。
保护性
为了研究人工孢子对各种环境压力的抵御能力,他们分别施加紫外光、温度、有机溶剂以及有机-水两相界面张力等外界压力。在细菌的死/活实验以及酶活稳定性实验中,人工孢子的表现均大大优于原始细菌(图4)。例如,在紫外光照射下,原始细菌几乎全部失去活性,而人工孢子则有超过85%的存活率(图4b,4c)。此外,人工孢子中的酶活性也几乎是原始细菌的2倍(图4d)。在其他压力环境下,人工孢子也有着相似的存活率和酶活性。

图4.保护性评价。a-d: 原始细菌和人工孢子在紫外光照射下存活率以及酶活性。e-h: 原始细菌和人工孢子在两相界面处存活率以及酶活性。
乳液表征
此后,他们通过对包裹材料组分的优化,成功构建了人工孢子稳定的皮克林乳液体系。利用两种不同的染料分别标记有机相与水相,证实他们得到了水包油型乳液(图5d)。此外,通过表达绿色荧光蛋白于细胞内,可以看到人工孢子分布于有机-水两相的界面上(图5f, 5g),该发现也通过SEM得到了直观的证实(图5h)。

图5.基于人工孢子的乳液的研究。
单步界面生物催化反应研究
他们首先表达酯酶CalB于大肠杆菌中,随后进行表面包裹,构建人工孢子。通过优化人工孢子表面亲疏水性、乳液体系的有机相-水相比例及人工孢子用量,该乳液体系的催化效率远高于其他两组对照试验(图6c)。此外,该人工孢子在重复多次利用的情况下,仍保持着较好的活性与催化效率(图6d)。由于大肠杆菌是一种广泛适用的酶表达平台,他们又在其他两种酶体系中进行了界面催化的拓展,同样显示出远远优于对照试验的结果(图6f,6h)。值得注意的是,由于人工孢子始终保持着代谢活性,使其在涉及辅酶再生的反应中,可以依靠自身的代谢路径完成辅酶再生而无需其他辅助。这将大大降低反应体系的复杂性和催化过程的成本,显示了该体系独特的应用优势。

图6.单步酶催化反应的研究。a-d:基于脂肪酶CalB的乳液体系优化、对比及重复利用。e-f:酶BAL的界面催化研究。g-h:酶ADH-a的界面催化的研究。
多酶界面生物催化的研究
在单酶反应证实过可行性后,他们进一步将反应体系拓展到多酶催化。为此,他们以2种多酶耦联催化反应为研究对象,如图7所示,证明了在界面催化体系中的反应效率都远高于对照实验。

图7.多酶催化反应的研究。a-b:基于ADH-ht和CalB的多酶界面催化。c-d: 基于ADH-ht和BAL的多酶界面催化。
化学-酶耦联界面生物催化的研究
随后,他们进一步以人工孢子为载体,负载了金属催化剂钯,并通过TEM进行了钯纳米颗粒的分布表征(图8b,8c)。值得注意的是,金属催化剂的负载并没有影响人工孢子的繁殖能力(图8d)和乳化能力(图8f)。此外,他们设计了化学-酶偶联催化体系(图8g),并进一步证明了界面催化体系的优越性(图8h)。

图8.化学-酶耦联催化反应的研究。a-d:负载钯纳米颗粒的人工孢子表征及其生长曲线。e-h: 负载钯纳米颗粒的人工孢子的乳液研究及其界面化学-酶耦联催化研究。
他们利用生物相容性的聚多巴胺包裹大肠杆菌,构建了可以抵御环境压力的人工孢子,并通过在其内部表达多种不同的酶,使其作为细胞工厂应用于单酶、多酶以及化学-酶耦联的界面生物催化过程。鉴于该细胞工厂的通用性以及化学催化剂的多样性,可以展望,以人工孢子为基础构建的界面催化体系将为二者的结合提供更多的可能性,并有望应用于解决合成工业上的难题。文章第一作者为孙志永博士,通讯作者为吴昌柱教授,通讯单位为南丹麦大学。
原文链接:https://www.nature.com/articles/s41467-022-30915-2
课题组介绍:
南丹麦大学化学系的吴昌柱教授课题组致力于酶催化及绿色化学的研究; 其研究重点是通过对酶及细胞的化学修饰获得new-to-nature的生物催化应用。详情请参见:https://www.wugroup.sdu.dk/
希望对该组研究方向感兴趣的研究人员与他们取得联系。该课题组现在资金充足、年轻、有活力,具有较好的发展前景;目前招聘多个全奖的博士和博士后位置;丹麦的博士生、博士后的质量和待遇享誉全球。
孙志永博士目前就职于浙江工业大学生物工程学院,任独立PI。课题组长期招募有机合成、生物催化或自组装等研究背景的青年教师及博士后,欢迎有兴趣的研究人员与他们联系。详见:http://www.homepage.zjut.edu.cn/szy/cbb/
更多关于该工作的细节,请参考原文 DOI:10.1038/s41467-022-30915-2








