皮肤粘合剂在伤口护理、生物电子器件固定、及用于健康监测或疾病治疗的透皮贴剂等领域应用十分广泛。然而,传统的超强皮肤粘合剂在移除时通常会对皮肤造成一定拉扯、疼痛等不适感,尤其面向皮肤娇嫩的婴幼儿或皮肤脆弱的糖尿病患者时,超强粘合剂的剥离过程可能会造成皮肤二次损伤、炎症反应等严重问题。虽然此前研究中报道了多种基于不同刺激的响应性可逆粘附水凝胶,如电刺激、紫外光照、化学溶液等,但这些刺激条件限制了其在婴幼儿或者糖尿病患者等特殊人群皮肤上的使用。因此,设计一种具有足够粘附强度,并能够实现无痛剥离以避免造成皮肤疼痛和创伤的可逆皮肤粘合剂至关重要。
针对以上问题,西南交通大学鲁雄教授及中国海洋大学韩璐教授团队提出了一种基于多酚-蛋白质络合策略制备具有体温触发快速粘附及无损伤按需剥离的水凝胶的策略。首先,通过碱性氧化预聚方式,形成了富含酚基和醌基的多酚预聚物(PGA);其次,在双键化明胶(GelMA)成胶过程中利用多酚基团的多重相互作用,打破GelMA分子链间的氢键作用,调节GelMA链的缠结密度,使得GelMA网络具有体温响应性,实现在体温条件下保持稳定性的同时分子链流动性增强的特性。当该水凝胶与人体皮肤接触后,体温触发其发生相转变实现高效快速粘附且能长时间保持粘附稳定。对水凝胶表面简单的降温后,网络中的GelMA分子链间重新生成氢键,水凝胶粘附力降低,实现无损伤剥离。另外,PGA的引入调整了GelMA网络的交联方式,在GelMA网络内引入了可牺牲的非共价键交联,从而赋予PGA-GelMA水凝胶与皮肤组织匹配的机械柔韧性和高延展性,避免了水凝胶在皮肤表面剥离时被拉扯造成的伤害。此外,该PGA-GelMA水凝胶还表现出优异的抗炎、抗氧化、抗过敏等生物活性,能够有效避免传统皮肤粘合剂在长期与皮肤接触中导致的皮肤刺激或过敏现象。
该水凝胶贴片能够作为柔性自粘附生物电子界面,助力刚性电子器件在柔软皮肤表面的长期无刺激稳定固定,实现长时间生理信号监测。同时,该水凝胶在伤口部位还具有良好的粘附性,并能够通过调节伤口部位免疫微环境,加速糖尿病皮肤伤口愈合。综上,该PGA-GelMA水凝胶的设计能够助力专门应用于婴幼儿或者糖尿病患者等特殊人群皮肤的新型皮肤粘合剂及皮肤敷料的研发。
相关研究以 “Infant skin friendly adhesive hydrogel patch activated at body temperature for bioelectronics securing and diabetic wound healing”为题发表在《ACS Nano》。西南交通大学博士研究生姜亚楠和硕士研究生张新、张玮为论文的共同第一作者。西南交通大学鲁雄教授和中国海洋大学的韩璐教授为通讯作者。该工作得到了四川省重点研发计划项目、国家自然科学基金等项目的支持。
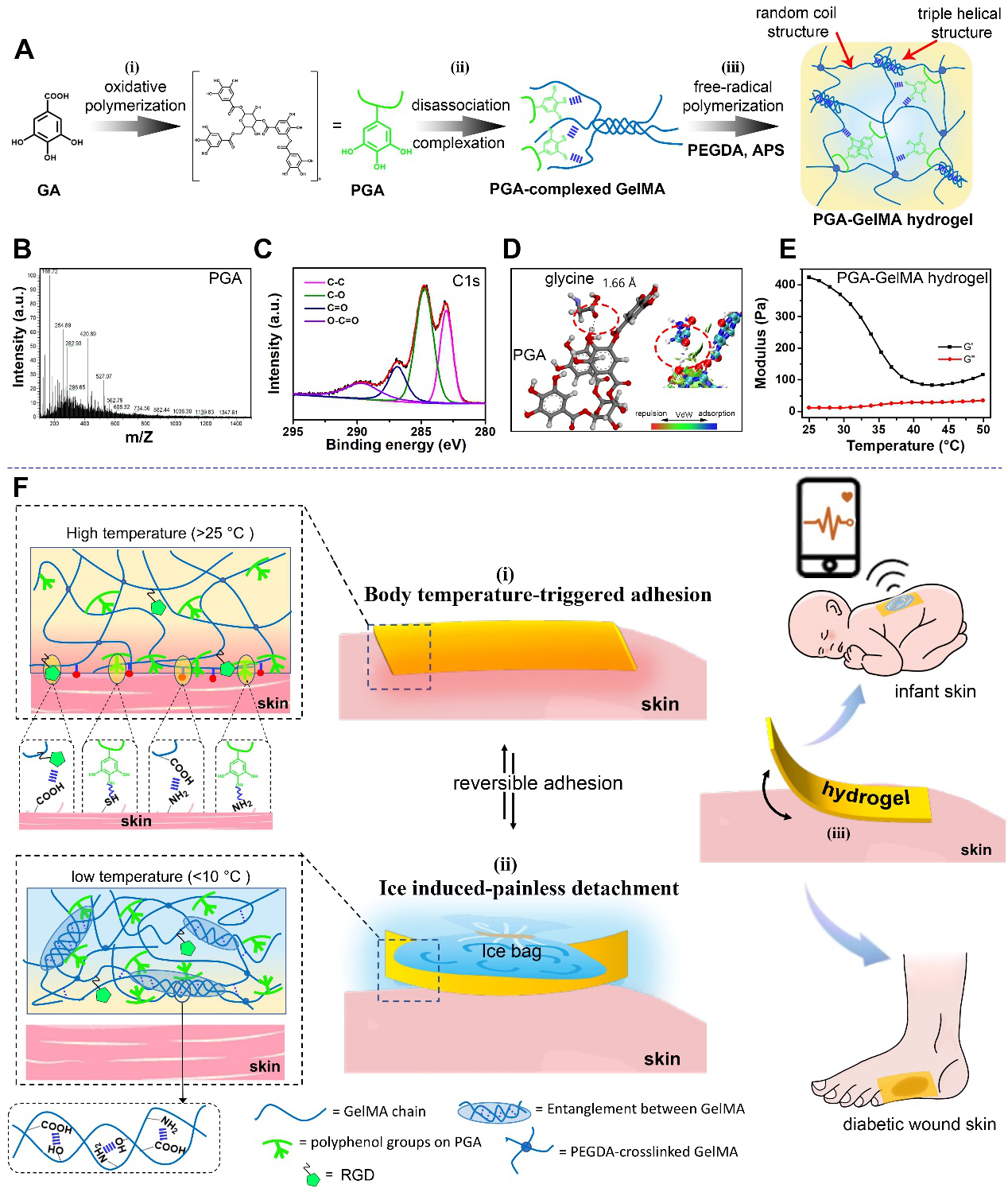
图1. 体温触发快速粘附及无损伤按需剥离的皮肤友好型水凝胶贴片设计策略。

图2. 通过体温触发实现粘附和降温实现无损剥离的PGA-GelMA水凝胶。可用于生物电子器件在皮肤表面的温和无刺激固定,也可用于皮肤伤口的保护。
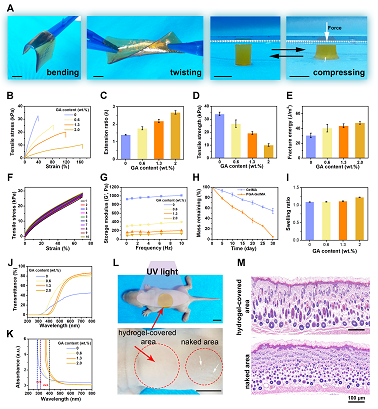
图3. PGA-GelMA 水凝胶的物理性质。PGA的引入赋予了水凝胶优异的柔韧性、耐疲劳等力学性能,同时还赋予水凝胶良好的可见光透过性及紫外光屏蔽特性,可用于抗紫外伤口敷料。

图4. PGA-GelMA 水凝胶的细胞亲和力的评估。PGA-GelMA水凝胶具有良好的细胞亲和性,有利于成纤维细胞在其表面的铺展,并促进细胞伪足和丝状伪足的生长,从而促进细胞的增殖和迁移。

图5. PGA-GelMA水凝胶抗氧化、抗炎、抗过敏能力的体外评价。PGA-GelMA水凝胶具有良好的活性氧清除能力,抗炎活性,及免疫调节能力,从而避免对在粘附过程中对对皮肤刺激或引起皮肤过敏反应。
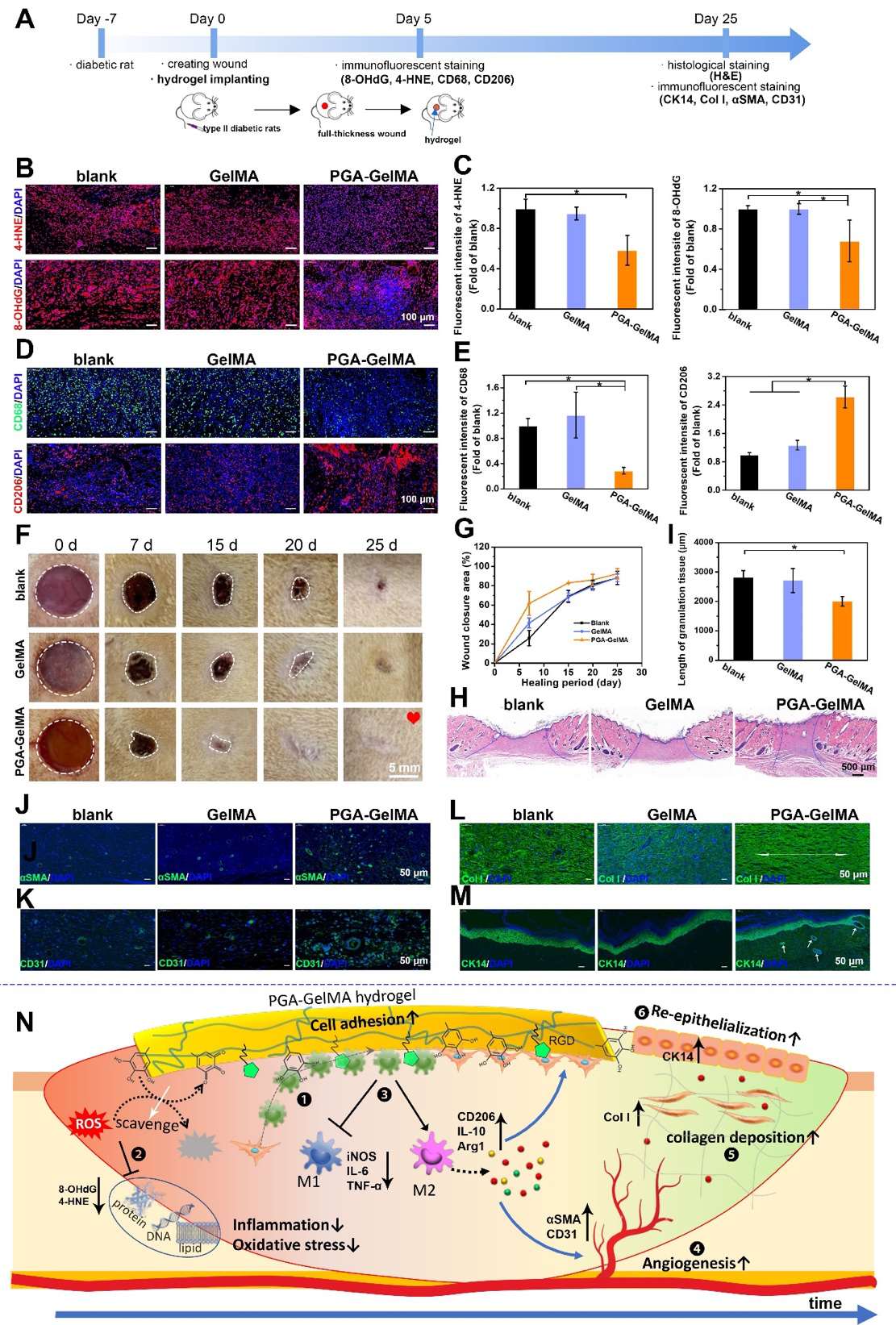
图6. PGA-GelMA 水凝胶促进糖尿病大鼠伤口愈合和再生。在植入伤口部位后,水凝胶能够清除受损炎症部位的活性氧自由基,抑制促炎性细胞因子的分泌,促进免疫细胞分泌具有免疫调节/再生活性的生物活性分子,从而减轻伤口处炎症反应。同时,多酚功能团良好的细胞亲和性,修饰局部环境并激活内源性的前体细胞分泌多种细胞因子,加速糖尿病皮肤等慢性伤口组织修复和再生。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.2c00662
- 中科院兰州化物所3D打印摩擦器件团队《Small》:体温触发的结构化水凝胶传感器 2025-01-10
- 西南交大邓维礼/杨维清教授团队 CEJ:体温触发粘合离子导电水凝胶 2024-09-03
- 南京理工大学傅佳骏/姜炜教授 AFM:强韧并可快速粘附的水下胶黏剂 2023-09-24
- 华南理工大学马春风教授 AFM:自增强按需剥离海洋防污涂层 2025-06-04
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 南通大学孙文旭/张雷团队 AFM:仿生界面工程设计兼具高拉伸与高灵敏度的双纳米复合水凝胶 2026-05-29
