炎症性肠病 (IBD) 是一种慢性炎症综合症,并会导致许多并发症,如肠梗阻、慢性腹泻、直肠出血和结直肠癌。IBD是全球第三大常见疾病,目前全球有超过500万人罹患炎症性肠病。对于IBD的治疗,常规策略依赖于抗生素和免疫抑制剂。然而,由于缺乏靶向递送能力和低的生物利用度,需要通过大剂量给药来维持肠道炎症区域的有效药物浓度,这也将导致严重的副作用和耐药性。口服给药时遇到的强胃酸环境会影响药物的稳定性和药效。尽管通过直肠给药可以提供有效的药物浓度,但这种方法总是伴随着剧烈疼痛。因此,急需开发一种肠道炎症靶向给药系统,能够实现胃酸耐受和可控释放,以最大限度地提高治疗效果并减少副作用。
近年来,智能微凝胶作为药物载体,不仅能实现药物的可控释放,还能提高负载药物对恶劣环境的耐受性。其中,壳聚糖因其优异的生物相容性已被FDA批准用于生物医学应用。此外,作为自然界中唯一的阳离子多糖,壳聚糖具有出色的抗菌和抗炎功能。其次,因其具有粘膜粘附特性,可以通过与肠上皮分泌的粘蛋白形成氢键来实现肠道靶向递送。目前,一些pH响应的微凝胶已经被设计用于肠道区域的可控药物释放。令人遗憾的是,这些智能载体无法更精准地识别和响应肠道炎症区域。新型的智能载体不仅需要具有靶向递送,还应该能够精准识别炎症区域并释放药物(Nat. Rev. Mater., 2022, 7:39-54),从而增强治疗效果和减少毒副作用。
在最近的工作中,Bel等人发现肠道病原体可以破坏细胞功能,从而导致肠腔内异常分泌溶酶菌来抵抗细菌入侵(Science, 2017, 357:1047-1052)。根据炎症性肠道特异性微环境,德国亚琛工业大学Andrij Pich教授团队、东华大学史向阳教授团队和浙江工业大学大学苏为科教授团队开发了一种电荷反转和生物降解的壳聚糖基微凝胶,可用于口服抗生素递送和特异性响应肠道炎症微环境的药物释放(图1)。首先,将不同含量的苯胺接枝到壳聚糖,形成聚苯胺接枝的壳聚糖。接着,通过反相微乳液法,利用戊二醛交联得到壳聚糖基微凝胶。该微凝胶用 NaCl 溶液处理之后,表现出两性电解质和电荷反转性能。制备得到带负电的微凝胶可用于负载阳离子的万古霉素,且具有较高的负载效率。值得一提的是,该载药微凝胶不仅具有胃酸抵抗性,还可以防止万古霉素在健康胃肠道中过早渗漏。与其他用于 IBD治疗的pH 响应载体相比,该载药微凝胶的关键优势在于它们能进一步特异性识别健康和发炎的肠道区域,实现抗生素在肠道炎症区域的精准释放,增强IBD的治疗效果并减少副作用。基于这些出色的性能,该研究开发的智能微凝胶可用作IBD治疗的潜在口服药物递送平台。
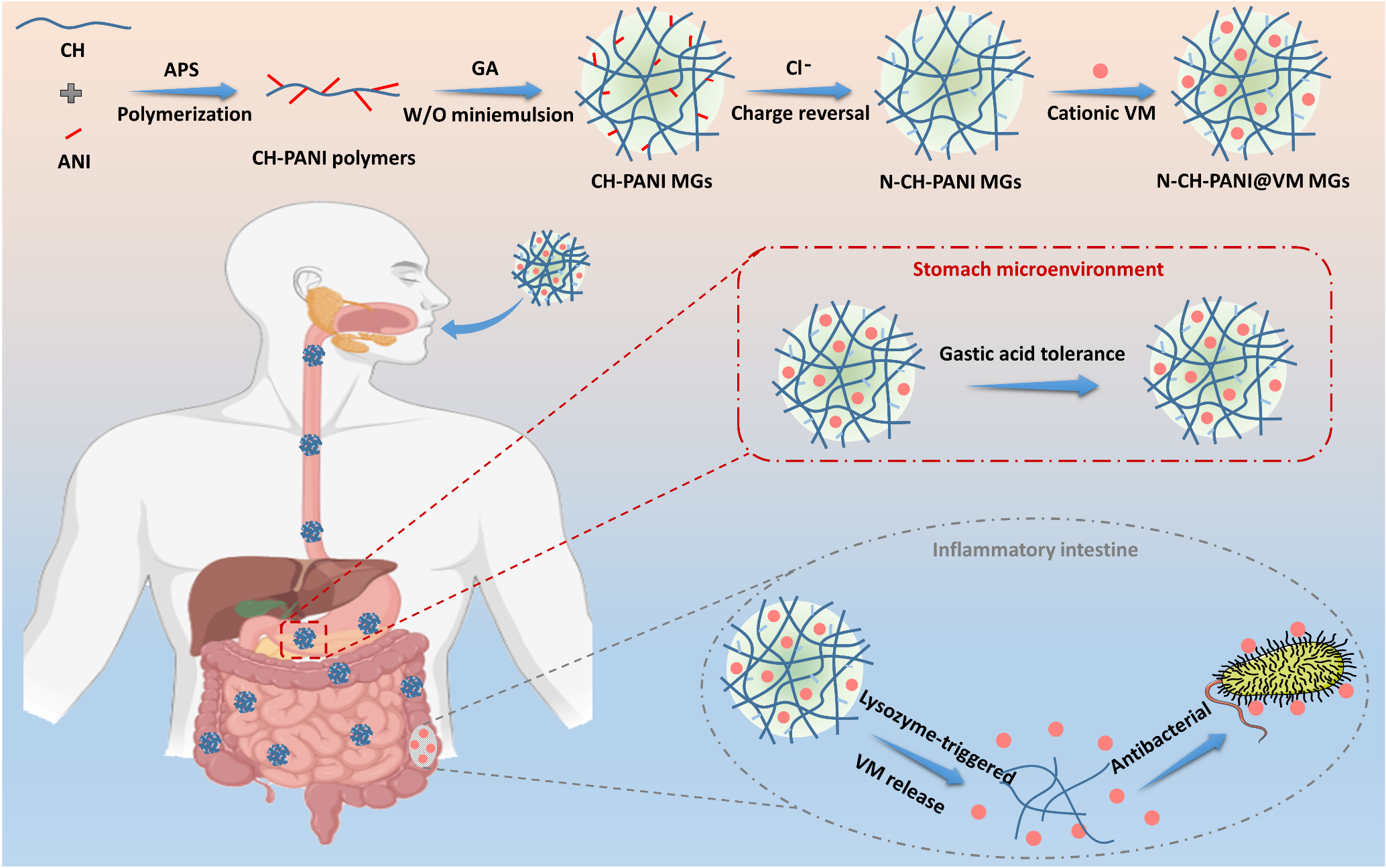
图1.电荷反转和可降解的壳聚糖基微凝胶用于溶菌酶触发的抗生素释放:高的药物负载、优异的胃酸耐受性和特异的肠道炎症响应性。
该研究成果近日以“Charge-reversible and biodegradable chitosan-based microgels for lysozyme-triggered release of vancomycin” 为题,在线发表在Journal of Advanced Research(DOI: 10.1016/j.jare.2022.02.014)上。文章第一作者为DWI-莱布尼兹交互材料研究所李鑫博士,通讯作者为DWI-莱布尼兹交互材料研究所Andrij Pich教授、东华大学史向阳教授和浙江工业大学李和霖博士。该论文得到了中德中心项目、德国科学基金会DFG和国家自然科学基金的支持。
原文链接:https://doi.org/10.1016/j.jare.2022.02.014
- 中山大学肿瘤医院杨江教授 JCR:可吸入式pH响应型电荷反转聚合物-siRNA复合物用于ALK融合阳性肺癌靶向基因治疗 2025-03-31
- 浙江大学申有青教授团队 Adv. Mater.: 酯酶响应电荷反转的季铵型类脂质分子用于提升LNP稳定性及mRNA脾脏特异性表达 2023-08-05
- 浙大申有青教授团队 Angew:具有高效肿瘤蓄积和渗透性能的氨肽酶响应电荷反转药物输送系统 2023-02-09
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
- 四川大学郭少云/李春海团队 Macromolecules:吹膜加工外场下生物降解材料PBAT结构与性能的演变机制 2026-02-11
- 四川大学何斌/成都大学高文霞 Adv. Mater.:具有无规-嵌段分子链结构的生物降解共聚物用于高性能可吸收组织结扎夹 2025-12-29
- 江南大学付少海/王冬团队 Small:原位矿化生成的双网络结构壳聚糖复合气凝胶用于替代石油基保温材料 2025-10-27
