硫化氢(H2S)在结直肠肿瘤微环境中高度富集,作为铜稳态和铜死亡的“上游”调控因子,其动态变化深刻影响着铜离子的生物利用度和细胞死亡命运。然而,现有铜死亡纳米疗法多聚焦于下游铜过载的“末端干预”,缺乏对上游H2S动态调控过程的实时解析能力,导致治疗干预始终滞后于上游调控事件,限制了精准治疗策略的发展。值得说明的是,当前主流的分析方法如光学成像、电化学检测,大多遵循“被动监测”模式,即它们能够高灵敏地报告目标分子的存在和变化,却无法主动介入并调控所监测的生物学过程。这种传感与干预功能的割裂,导致难以在同一平台上实现“边监测、边调控”的动态闭环研究,成为深入解析H2S介导铜死亡机制的重要瓶颈。
针对这一挑战,杭州师范大学黄又举教授团队成功开发了一种具有“自驱动”和“自报道”功能的花瓣状Au-Cu2O金属纳米酶,用于实时探析H2S介导的铜死亡过程。
2026年3月16日,相关研究工作以“A Self-Driving and Self-Reporting Petal-Like Au-Cu2O Metalloenzyme for Probing H2S Mediated Cuproptosis”为题发表在ACS Nano上(DOI: 10.1021/acsnano.6c01009)。
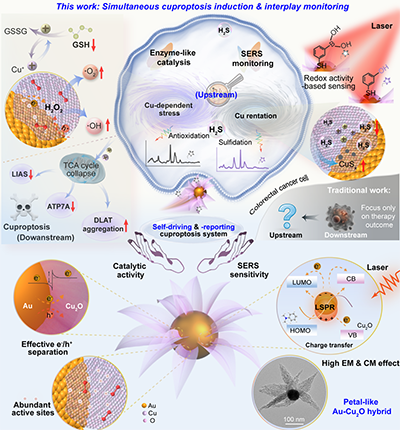
图1 花瓣状Au-Cu2O金属酶的设计及H?S介导铜死亡监测示意图
铜死亡(cuproptosis)是一种新发现的铜依赖性调节性细胞死亡方式,为靶向代谢活跃的癌症(特别是那些对传统治疗耐药的癌症)提供了新的治疗机遇。在结直肠癌中,其肿瘤微环境的独特之处在于富集了高水平的硫化氢(H2S)。H2S能与铜离子形成复合物,充当铜的生物可利用“储备库”,从而成为铜稳态的关键上游调节器。然而,H2S的动态波动与下游铜诱导的氧化还原失调之间的实时关系仍不清楚,这限制了基于铜死亡的精准治疗策略的开发。尽管已出现多种H2S响应型纳米材料用于治疗,但它们大多作为“盲目”的递送系统,无法原位动态追踪H2S的调控过程及其引发的下游氧化还原后果。表面增强拉曼光谱(SERS)技术具有分子指纹能力和单分子灵敏度,为监测细胞内事件提供了可能,但现有探针通常只具备传感功能,缺乏内在的治疗活性,造成了诱导与监测能力之间的技术空白。
针对这一挑战,研究团队设计了一种通过表面活性剂导向法生长的花瓣状Au-Cu2O异质结构。该结构通过在金纳米颗粒表面各向异性生长Cu2O纳米片,形成了富含活性Au-Cu2O结的独特形貌。与传统的核壳结构相比,这种花瓣状架构暴露了大量的活性位点,促进了有效的电子-空穴分离,并协同增强了电磁场和化学增强效应,从而显著提升了其类酶活性和SERS灵敏度。优化后的结构对亚甲基蓝的检测限低至10-10 M,增强因子高达1.55×109。
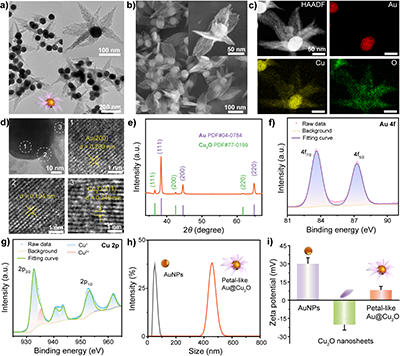
图2花瓣状Au-Cu2O的结构表征
该纳米酶展现出高效的光增强过氧化物酶样活性。在激光照射下,能催化H2O2产生大量?OH和?O2?自由基,并迅速消耗细胞内谷胱甘肽,从而破坏细胞的抗氧化防御系统,引发线粒体功能障碍和脂质过氧化,最终驱动细胞死亡。更重要的是,该平台集成了基于活性的SERS传感策略。通过修饰对活性氧(ROS)响应的拉曼探针(3-MPBA),研究人员能够利用SERS成像实时监测由纳米酶自身催化活动引发的细胞内氧化应激水平的动态变化,在4小时内观察到ROS信号显著增强,实现了“自驱动”治疗与“自报道”监测的协同。利用这一强大的工具,研究团队深入揭示了H2S在铜死亡中的双重调节作用。通过使用胱硫醚-β-合酶(CBS)的激活剂(SAM)和抑制剂(AOAA)调控细胞内H2S水平,结合SERS监测、铜含量分析和关键蛋白检测,研究发现H2S一方面可作为瞬时抗氧化剂缓冲氧化应激,另一方面通过与铜离子形成复合物,促进细胞内铜的滞留,形成一个持续的铜离子“库”。这种“铜库”能更有效地将铜递送至线粒体中的脂酰化蛋白靶点(如DLAT),从而放大下游的铜死亡执行。同时,研究还观察到该过程伴随有铁死亡通路的协同激活(如GPX4失活),共同加剧了细胞的死亡。
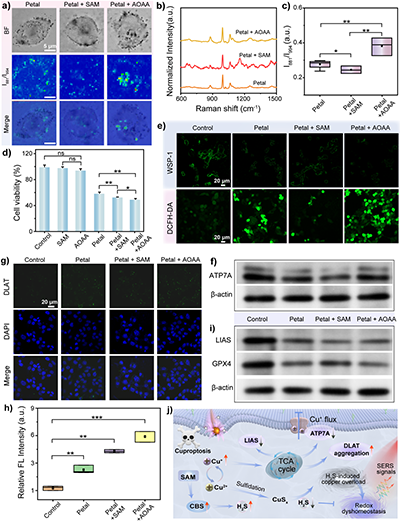
图3 H2S介导的铜滞留与铜死亡调控机制
综上,该研究成功开发了一种集催化治疗与实时SERS监测于一体的多功能花瓣状Au-Cu2O杂化平台。它不仅填补了铜死亡诱导与监测之间的技术空白,更重要的是,利用这一平台在活细胞层面直接揭示了内源性H2S作为上游关键调控因子,通过形成铜-硫化物复合物来控制铜的滞留与递送,从而精密调控铜死亡的机制。这项工作为理解金属离子介导的细胞死亡代谢动态提供了强大工具,并为靶向H2S异常的恶性肿瘤开发精准的“自反馈”治疗诊断策略奠定了坚实基础。
该工作第一作者为杭州师范大学副教授江蕾和硕士研究生卢巧怡,通讯作者为杭州师范大学黄又举教授。该工作得到了国家自然科学基金(U25A20385、22304042、52473209)和浙江省“尖兵”“领雁”项目(2025C02250、2024C03228)等项目的资助。
通讯作者黄又举教授简介

黄又举,教授,博士生导师,国家优青,杭师大材化学院副院长。2010年博士毕业于中国科学技术大学,师从李良彬教授。2010-2014年在新加坡南洋理工大学做博士后。2014-2019年在中科院宁波材料所工作,任副研究员/项目研究员。2017-2018年,在德国马普所高分子所做访问学者。2019年9月入职杭州师范大学,组建纳米生物传感器关键材料团队。以通讯作者在Science Advances,Journal of the American Chemical Society,Angewandte Chemie International Edition,Advanced Materials, Chemical Society Reviews等期刊上发表SCI论文100余篇。被引用13000余次,H因子为58。授权中国和美国发明专利35件。主持科研项目20余项,包括7项国家自然科学基金。获首届浙江省青年科技英才奖(2021年),浙江省自然科学二等奖(2023年,第一完成人)和全国"挑战杯"揭榜挂帅专项赛一等奖(2024年,指导老师)。入选浙江省海外高层次人才引进计划(2016年)和国家自然基金委优秀青年项目(2022年)。
第一作者江蕾博士简介

江蕾,杭州师范大学材料与化学化工学院副教授。2022年6月博士毕业于华东理工大学分析化学专业,师从李大伟教授;2017年6月本科毕业于安徽理工大学应用化学专业。2022年10月至2025年7月于中南大学-杭州师范大学(联合培养)从事博士后研究,导师黄又举教授。2025年8月留校任副教授。主要从事功能化贵金属纳米结构的设计合成、SERS分析平台的构建以及生物活性分子的高灵敏抗干扰分析研究。相关工作以第一作者或通讯作者在Angewandte Chemie International Edition, ACS Nano, Advanced Science, Analytical Chemistry, Biosensors& Bioelectronics等国际知名期刊发表SCI论文10余篇,获授权国家发明专利2项,曾获第十一届国际发明展览金奖(2025年,第三完成人),现主持国家自然科学基金青年科学基金项目(C类)1项,参与国家自然科学基金面上项目2项。
原文链接:https://doi.org/10.1021/acsnano.6c01009
- 中科大俞汉青/李文卫/刘武军团队 Nat. Commun.:自驱动串联醇解实现废聚碳酸酯高值化回收 2026-05-08
- 南京林业大学蔡晨阳 Matter:自驱动木材水合气凝胶解耦户外辐射制冷与持续发电 2026-02-18
- 山西师大崔小静 ACS Sensors:机器学习辅助热电水凝胶实现自驱动面部感知 2025-01-11
- 四川大学刘瑾/王军、西南交大谢超鸣 Nat. Commun.:多酚介导硫化氢气体-生物电耦合水凝胶促进糖尿病牙周组织有序再生 2024-11-01
- 澳门大学代云路课题组 Angew: 硫化氢重新编程肿瘤细胞氧代谢增强癌症放疗 2022-02-22
- 上海第九人民医院张绘莉和华侨大学陈爱政《JCR》:微流控技术构建高分子多孔微球递送硫化氢靶向治疗肺动脉高压 2020-12-06
- 宁波材料所陈涛/肖鹏团队《Adv. Mater.》: 柔性凝胶电子器件实现吸湿-解吸实时监测与智能化湿度管理 2026-02-05
