导电凝胶由于具有类组织的力学强度和高含水量特性,是构建生物活性界面的首选材料。全凝胶神经电极通过集成凝胶基导电传感层和绝缘封装层,能够最大限度地减少传统金属电极植入带来的炎症反应和胶质瘢痕生成。通常的导电凝胶需要整合导电填料(金属纳米颗粒、导电聚合物、碳纳米管等)来获得较高的导电性。但是,添加的刚性导电填料往往会降低电极的柔性并增加其力学强度,从而导致脑组织-电极界面的机械失配。此外,电极层-绝缘层、绝缘层-组织层之间的界面粘附性能直接影响神经电信号的监测质量。本研究通过双策略诱导的PEDOT:PSS相分离构建出具有超高电导率的导电凝胶材料,并获得优于金属电极材料的信噪比。进一步地,通过多酚化学介导的层间粘附,制备了具有绝缘层-传感层-屏蔽层等多层结构整合的多电极阵列,并成功应用于大鼠癫痫信号记录与电刺激加载。

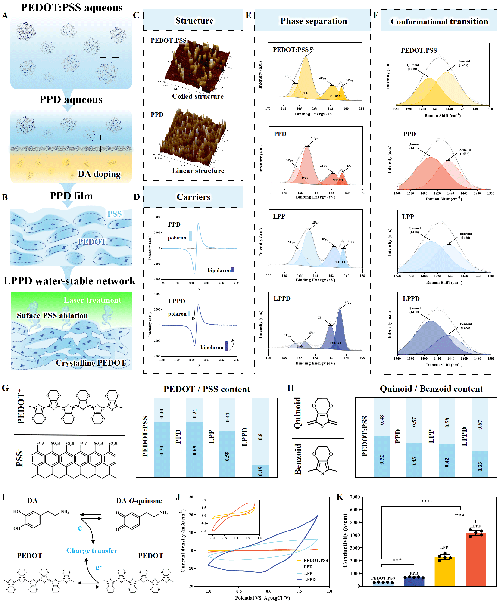
图1.激光/DA双策略诱导PEDOT:PSS相分离与构象转化,从而促进其电化学性能增强
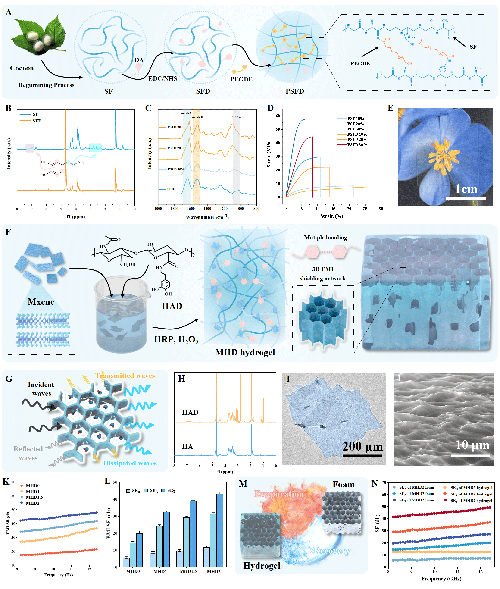
图2.封装层与电磁屏蔽层设计
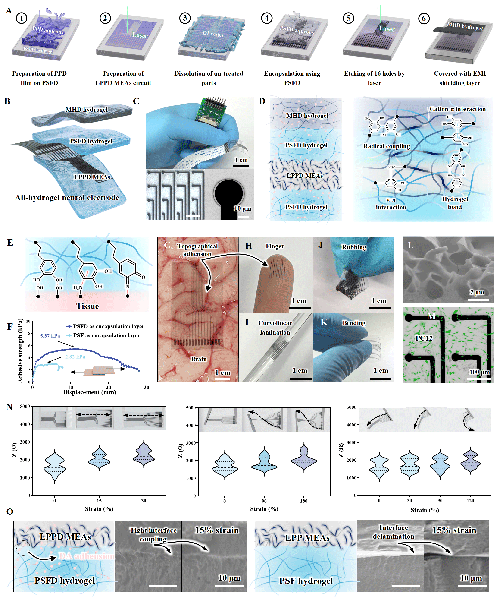
图3. 全凝胶电极的制备及表征
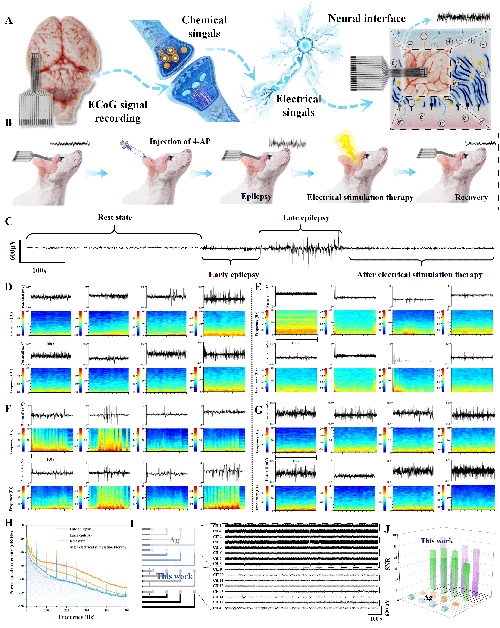
图4. 在体多通道局部场电位(LFP)监测

图5. 在体多通道动作电位(AP)监测
由于MEAs的加工精度(约15 μm)与神经元尺寸相匹配(小于100 μm),全神经电极极实现了对单个或多个神经元动作电位的精准监测。在4-AP诱导的大鼠癫痫模型中,通过阈值法进一步研究了神经元尖峰行为,发现多通道记录的动作电位几乎同时出现,与异常神经元的同步放电相关。通过计算不同记录通道相对于通道1的尖峰时间延迟,发现记录的电信号显示出明显的规律性和位置依赖性,符合癫痫持续状态的异常神经元放电特征。并且,通过电神经调节能够有效抑制癫痫样放电活动。此外,该全凝胶神经电极在颅内植入2周后未引起明显的组织损伤或炎症反应,显示出其在临床诊断、监测和治疗中的长期应用前景。
总结:该研究团队制备了一种多层集合的全凝胶神经电极,通过双策略诱导的PEDOT:PSS相分离实现传感层的超高导电性,并结合多酚化学实现稳定的层间粘附性。基于此,该神经电极获得了卓越的电化学稳定性。体内实验表明,该神经电极能精准记录癫痫大鼠的LFP信号,且能够区分两个不同神经元的尖峰信号。同时,该神经电极还能在癫痫发作期间向大鼠大脑皮层提供人工电刺激。这些结果都证明了该全凝胶神经电极在研究神经退行性疾病发展、功能及治疗中的巨大潜力。
原文链接:https://pubs.rsc.org/en/content/articlelanding/2024/mh/d4mh00939h
- 西南大学曾建兵《Macromolecules》:聚多巴胺辅助构建高性能室温自修复导电弹性体 2025-10-19
- 新疆大学吐尔逊·阿不都热依木教授团队 CEJ: 聚多巴胺-PEDOT基便携式传感器用于氯丙嗪和诺氟沙星的同步测定 2025-09-05
- 新疆大学吐尔逊·阿不都热依木教授团队 AFM:利用3D Ti3C2Tx 混合电极材料增强电化学储能 2025-07-31
- 中国林科院林化所南静娅/刘玉鹏/王春鹏 Small:具有低温适应性的柔性全凝胶超级电容器 2024-02-28
- 南京大学张晔课题组《Adv. Mater.》:开发一种类组织柔软的全凝胶电池 2021-11-01
