在常温机械灌注过程中,载氧载体对维持受体器官的生理代谢至关重要。目前常见载氧载体分为两大类:人工载氧体和天然载氧体(如红细胞)。人工载氧体(非细胞型),包括基于血红蛋白的氧载体和全氟化碳,具有存储时间长、无需交叉配型、来源丰富等优点,但它们可能引起血管收缩、肾毒性以及其他潜在的不良反应。相比之下,天然红细胞在体内循环中的寿命较长且变形性良好,但其应用受到以下限制:(1)储存时间短——红细胞在4°C下的常规储存期限仅为42天,导致血液资源的大量浪费;(2)交叉配型——红细胞表面抗原的多样性增加了异体和异种输血的交叉配血风险;(3)机械损伤——在灌注过程中,红细胞可能发生挤压变形、扭曲和破碎,导致显著的溶血;(4)血源稀缺——目前在大规模灌注过程中对血液的需求量巨大。为应对上述挑战,开发一种通用、生物安全、易于扩展且高效的红细胞工程技术以提升其常温机器灌注和输血效果具有重要意义。
生物仿生硅化技术通过在细胞内外的界面上形成纳米硅质外骨骼,为脆弱的细胞提供了具有高机械强度、化学惰性和不可降解性的二氧化硅铠甲,这种铠甲赋予了细胞化学和热稳定性,并显著提升了其抵抗恶劣环境(如高温、高湿、紫外等)的能力。在这领域,朱伟教授课题组开展了大量相关研究(参见 Nat. Rev. Bioeng. 2024, 2, 282;Angew. Chem. Int. Ed. 2024, 63, e202406110;ACS Nano 2022, 16, 2164;Nat. Commun. 2022, 13, 6265;J. Am. Chem. Soc. 2021, 143, 17, 6305 等)。然而,通过精确控制硅酸的水解形式,以可控方式实现对红细胞的改造及功能延拓的工作仍非常有限。
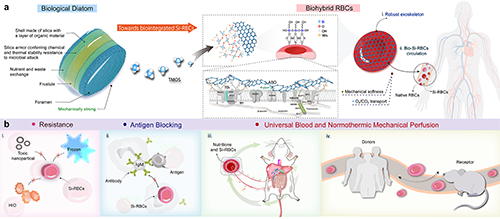
图1. 红细胞仿生硅化及功能示意图。(a) 基于自然界硅藻外骨骼启发的血红细胞生物硅化以强化红细胞结构和实现表面抗原屏蔽;(b) 生物硅化可赋予红细胞几大优势:提升对外部环境抵抗能力、实现表面抗原屏蔽、实现万能血构建及其用于同种异体或异种异体输血。
硅化红细胞具有以下优异性能:
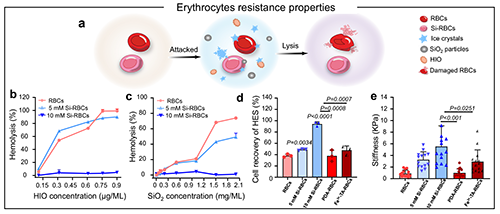
图2. 硅化红细胞和原生红细胞的环境抗性对比。 (a) 天然红细胞和硅化红细胞对恶劣环境的抵抗力示意图;溶血毒素(b)和St?ber粒子(c)对红细胞溶血的影响;(d) 低温保存后的红细胞冷冻回收效率。(e) 天然红细胞、硅化红细胞、Fe3+-TA 涂层红细胞、多巴胺涂层红细胞的硬度检测。
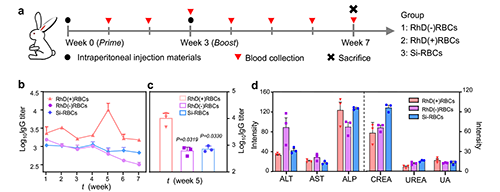
图3.硅化红细胞对模型兔的免疫激活反应和脏器生化指标的影响。
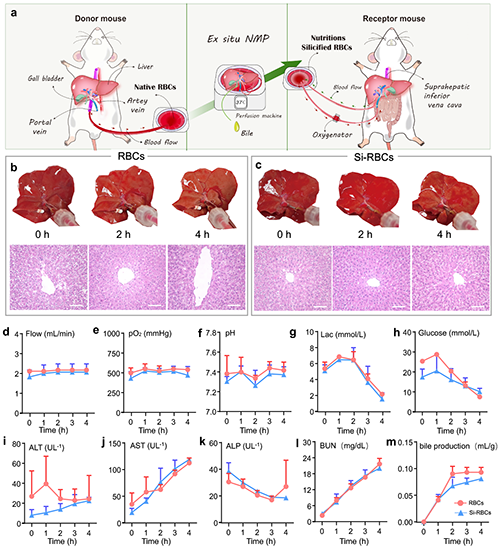
图4. 硅化红细胞用于大鼠肝脏移植的常温机械灌注(NMP)中的潜力。(a) 大鼠肝脏移植的常温机械灌注示意图;(b) 原生红细胞和 (c)硅化红细胞灌注肝脏的形态及其病理切片;肝脏灌注过程中的(d)门静脉流量,(e) 氧压,(f) pH,肝糖代谢水平:(g)乳酸水平和(h)葡萄糖水平,(i-m)NMP 期间的生化分析,包括肝功能,以及胆道功能和(m)胆汁分泌功能。
总之,在这项工作中,通过界面硅化他们首次实现了近100%的红细胞冷冻保护,通过血型屏蔽克服了同种异体血型问题,并验证了异种输血的可能。由于技术简单、可靠、易于扩展,并且具有良好的生物相容性,其未来有可能在临床上展现出重大应用价值。
原文链接:https://www.pnas.org/doi/10.1073/pnas.2322418121
