
自然界中生物体皮肤的多功能性,如温度/湿度感知、颜色变化和自愈合性能等,对人工电子皮肤材料的设计提出了更高的要求。长期以来,科学家们致力于在电子皮肤中实现生物相容性、多模态响应和自修复性能的一体化,对未来电子皮肤面向可穿戴和植入式电子设备应用具有重要意义。近年来的研究表明,通过在聚合物基材中嵌入、涂层或包裹工作电极(主要包括导电碳材料和贵金属纳米线/纳米片)是制备可拉伸双模态传感器的简便方法,但工作电极和基材之间的机械不匹配会降低多功能响应的可靠性与稳定性,且上述制备通常要求石油基材料和复杂的化学合成,对生物相容性有潜在的不利影响。因此,如何在电子皮肤中集成包括生物相容性、多模态传感和自修复性能在内的类皮肤特征,同时保持优良的机械强度和拉伸性,仍然是一个挑战。
近日,四川大学张新星教授团队在前期研究工作(ACS Nano 2022, 16, 13002; Nat. Commun. 2021, 12, 1291; ACS Nano 2020, 14, 7055)基础上,报道了一种生物衍生的衣康酸/氯化胆碱可聚合低共熔溶剂(PDES)离子弹性体,用以制备自修复双模态传感器(图1)。通过衣康酸、纤维素纳米晶和花青素等一系列生物质衍生物在超分子作用下制备了生物基离子弹性体复合材料,从而保证了自修复双模态传感器良好的生物相容性(细胞存活率超过87%)。基于聚多巴胺包覆的纤维素纳米晶(PDA@CNC)构建的物理与氢键网络的协同调控,生物衍生的PDES离子弹性体同时实现优秀的自修复效率(>90%)和卓越的机械性能(拉伸强度和韧性比纯生物衍生的PDES高2.95和69.57倍)。此外,PDES本征的离子导电性和花青素涂层的pH响应特性使该传感器能够实现对人体运动和汗液生理信息可视化(pH值在3至12的范围内)的双模态检测,为未来医学诊断和医疗保健中皮肤接触及植入式生物电子设备提供了新的视角。
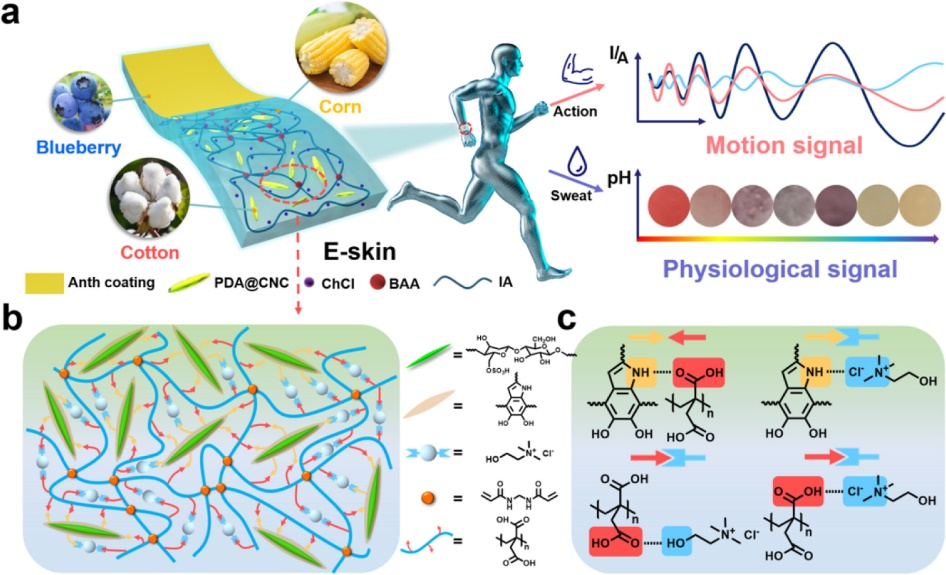
图1 材料设计示意图
由于纤维素纳米晶表面的聚多巴胺涂层和衣康酸/氯化胆碱PDES基体含有丰富的氢键给体与受体(氨基、羰基、羟基、氮正离子),纳米填料表面和聚合物基质之间构建了致密的多重氢键网络。PDA@CNC纳米填料在PDES离子弹性体中发挥物理交联位点的作用,通过物理和氢键网络的协同调控形成了更强健的非共价交联网络(图2)。
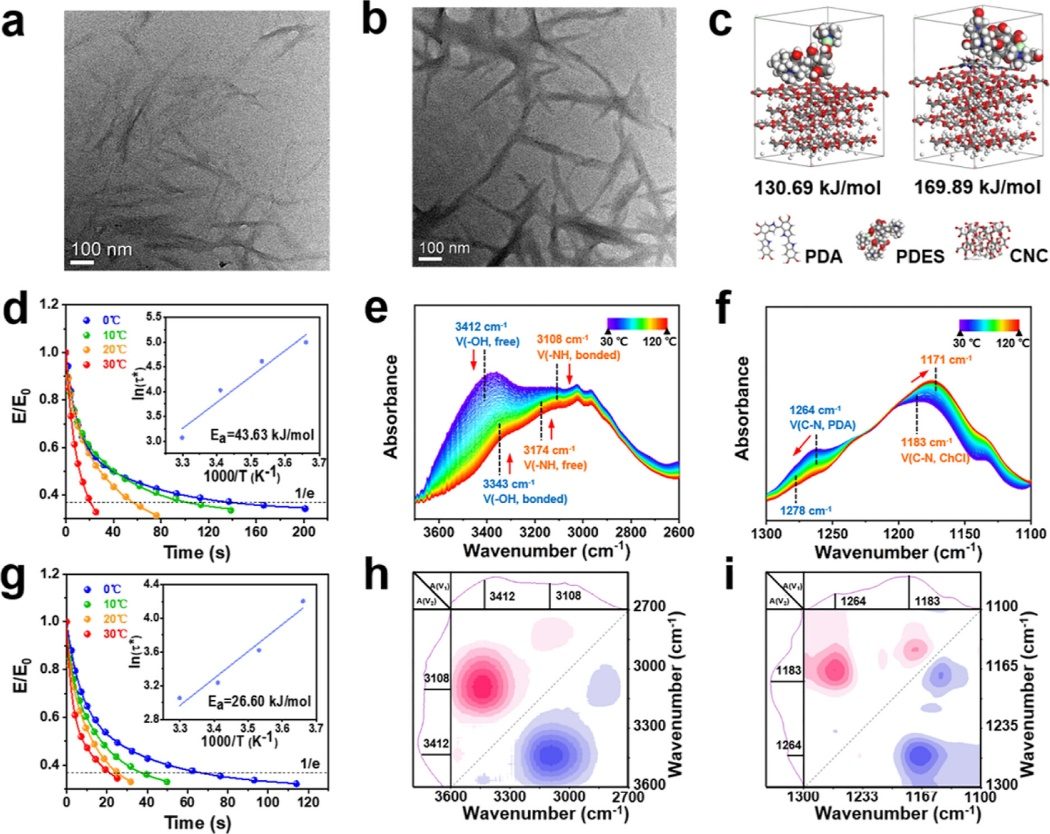
图2 纳米填料结构和多重界面氢键表征
基于致密而强健的非共价交联网络,PDA@CNC纳米填料和PDES离子弹性体之间的界面氢键大大提升了拉伸过程中材料的能量耗散能力。因此,该生物衍生的离子弹性体打破了一般生物基材料在强度和韧性方面的限制,表现出优异的机械性能以满足实际双模态监测过程中的需求(图3)。同时大量的可逆动态键赋予了PDES离子弹性体优异的自修复性能。

图3 机械和自修复性能表征
不需要额外工作电极的引入,PDES内部氯化胆碱正负离子在外加电场下的定向迁移能力赋予离子弹性体与电阻式传感器相同的力-电传感功能以检测人体运动。此外,通过花青素分子在不同pH值下酚类和醌类的结构互变异构化,实现了对人体异常碱性汗液的可视化分析(图4)。

图4 具有应变检测和汗液分析能力的双模态响应
原文链接:https://doi.org/10.1021/acs.chemmater.2c03105
- 中山大学谢庄课题组 Adv. Mater.:基于可聚合低共熔溶剂的高木质素含量网络 - 面向多功能软器件的便捷多尺度制备 2026-01-07
- 东华大学武培怡/吴慧青团队 Nat. Commun.:低共熔溶剂/烷烃界面聚合助力制备高性能聚酰胺有机溶剂纳滤膜 2025-09-26
- 苏科大叶常青教授团队连发 AFM/Small: 液态金属-聚合物体系的开发和应用方面取得系列进展 2025-01-22
- 东华大学游正伟教授、孙俊芬教授 AFM:氟氢键限域策略同步提升离子弹性体的拉伸强度、导电性能和自修复性 2025-12-17
- 上海工程技术大学宋仕强团队 AM:应变诱导离子通道排列与温度激活离子门控实现超高电导增强-打造宽温域、高韧性全固态离子弹性体 2025-11-30
- 宁波材料所茅东升/陈海明团队 Mater. Horiz.: 微相锁定自增强离子弹性体 2024-10-31
- 中国林科院林化所张猛/悉尼大学程文龙/南昆大宋平安 Adv. Mater.:含磷/氮及π-共轭联苯结构单元实现弹性体高强、高韧、阻燃及自修复 2026-06-01
